Серия Бальмера - Balmer series

В Серия Бальмера, или же Линии Бальмера в атомная физика, является одним из набора шесть названных серий описывая спектральная линия выбросы атом водорода. Ряд Бальмера рассчитывается по формуле Бальмера, эмпирический уравнение, открытое Иоганн Балмер в 1885 г.
Видимый спектр из свет из водород отображает четыре длины волн, 410 нм, 434 нм, 486 нм и 656 нм, которые соответствуют выбросам фотоны к электроны в возбужденных состояниях, переходящих на квантовый уровень, описываемый главное квантовое число п равно 2.[1] Есть несколько выдающихся ультрафиолетовый Линии Бальмера с длинами волн короче 400 нм. Количество этих линий представляет собой бесконечный континуум, поскольку он приближается к пределу в 364,6 нм в ультрафиолете.
После открытия Бальмера пять других спектральная серия водорода были обнаружены, соответствующие переходу электронов к значениям п кроме двух.
Обзор
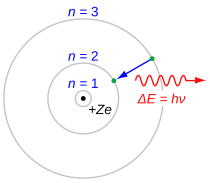
Серия Balmer характеризуется электрон переход от п ≥ 3 до п = 2, где п относится к радиальное квантовое число или же главное квантовое число электрона. Переходы последовательно называются греческими буквами: п = От 3 до п = 2 называется H-α, от 4 до 2 - H-β, от 5 до 2 - H-γ и от 6 до 2 - H-δ. Поскольку первые спектральные линии, относящиеся к этой серии, расположены в видимой части электромагнитный спектр эти линии исторически называются «H-альфа», «H-бета», «H-гамма» и так далее, где H - элемент водород.
Переход п 3→2 4→2 5→2 6→2 7→2 8→2 9→2 ∞→2 Имя H-α / Ba-α H-β / Ba-β H-γ / Ba-γ H-δ / Ba-δ H-ε / Ba-ε H-ζ / Ba-ζ H-η / Ba-η Бальмер брейк Длина волны (нм, воздух) 656.279[2] 486.135[2] 434.0472[2] 410.1734[2] 397.0075[2] 388.9064[2] 383.5397[2] 364.6 Разница энергии (эВ) 1.89 2.55 2.86 3.03 3.13 3.19 3.23 3.40 Цвет красный Аква Синий фиолетовый (Ультрафиолетовый ) (Ультрафиолет) (Ультрафиолет) (Ультрафиолет)
Хотя физики знали об атомной эмиссии до 1885 года, у них не было инструмента, чтобы точно предсказать, где должны появиться спектральные линии. Уравнение Бальмера предсказывает четыре видимые спектральные линии водорода с высокой точностью. Уравнение Бальмера вдохновило Уравнение Ридберга как ее обобщение, что, в свою очередь, привело физиков к открытию Lyman, Пашен, и Brackett серии, который предсказал другие спектральные линии водорода, обнаруженные за пределами видимый спектр.
Красный H-альфа спектральная линия бальмеровской серии атомарного водорода, являющаяся переходом из оболочки п = 3 в оболочку п = 2, один из ярких цветов вселенная. Он вносит яркую красную линию в спектры выброс или ионизационной туманности, как Туманность Ориона, которые часто H II регионы найдены в областях звездообразования. На полноцветных изображениях эти туманности имеют красновато-розовый цвет из-за комбинации видимых бальмеровских линий, которые излучает водород.
Позже было обнаружено, что при исследовании линий спектра Бальмера в спектре водорода с очень высоким разрешением они представляли собой близкорасположенные дублеты. Это расщепление называется тонкая структура. Также было обнаружено, что возбужденные электроны из оболочек с п больше 6 может перейти в п = 2 оболочки, при этом излучая оттенки ультрафиолета.

Формула Бальмера
Бальмер заметил, что одна длина волны имеет отношение к каждой линии в спектре водорода, которая находится в видимом диапазоне. свет область, край. Эта длина волны была 364.50682 нм. Когда любое целое число больше 2 возводилось в квадрат, а затем делилось само на себя в квадрате минус 4, тогда это число умножалось на 364.50682 нм (см. уравнение ниже) дала длину волны другой линии в спектре водорода. С помощью этой формулы он смог показать, что некоторые измерения линий, выполненные в его время спектроскопия были немного неточными, и его формула предсказывала линии, которые были позже обнаружены, хотя еще не наблюдались. Его число также оказалось пределом ряда. Уравнение Бальмера можно использовать для нахождения длина волны линий поглощения / излучения и первоначально был представлен следующим образом (за исключением изменения обозначений, чтобы константа Бальмера была представлена как B):
Где
- λ это длина волны.
- B - константа со значением 3.6450682×10−7 м или же 364.50682 нм.
- м равно 2
- п такое целое число, что п > м.
В 1888 г. физик Йоханнес Ридберг обобщил уравнение Бальмера для всех переходов водорода. Уравнение, обычно используемое для вычисления ряда Бальмера, является конкретным примером Формула Ридберга и следует как простая обратная математическая перестановка приведенной выше формулы (обычно с использованием обозначений м за п в качестве единственной интегральной постоянной):
куда λ - длина волны поглощенного / испускаемого света и рЧАС это Постоянная Ридберга для водорода. Видно, что постоянная Ридберга равна 4/B в формуле Бальмера, и это значение для бесконечно тяжелого ядра равно 4/3.6450682×10−7 м = 109737310,57 м−1.[3]
Роль в астрономии
Серия Бальмера особенно полезна в астрономия потому что бальмеровские линии появляются в многочисленных звездных объектах из-за содержания водорода в вселенная, и поэтому обычно видны и относительно сильны по сравнению с линиями от других элементов.
В спектральная классификация звезд, которая в первую очередь определяет температуру поверхности, основана на относительной силе спектральных линий, и серия Бальмера, в частности, очень важна. Другие характеристики звезды, которые можно определить путем тщательного анализа ее спектра, включают: поверхностная сила тяжести (в зависимости от физического размера) и состава.
Поскольку линии Бальмера обычно видны в спектрах различных объектов, они часто используются для определения лучевые скорости из-за доплеровское смещение линий Бальмера. Это имеет важное применение во всей астрономии, начиная с обнаружения двойные звезды, экзопланеты, компактные объекты, такие как нейтронные звезды и черные дыры (движением водорода в аккреционные диски вокруг них), идентифицируя группы объектов со схожими движениями и предположительно происхождением (движущиеся группы, звездные скопления, скопления галактик, и обломки от столкновений), определяя расстояния (фактически красные смещения ) галактик или квазары, и выявление незнакомых объектов путем анализа их спектра.
Линии Бальмера могут выглядеть как поглощение или же выброс линии в спектре, в зависимости от природы наблюдаемого объекта. В звезды, бальмеровские линии обычно видны в абсорбции, и они "самые сильные" у звезд с температурой поверхности около 10 000 кельвины (спектральный класс А). В спектрах большинства спиральных и неправильных галактик активные галактические ядра, H II регионы и планетарный туманности, линии Бальмера являются эмиссионными.
В звездных спектрах линия H-эпсилон (переход 7 → 2, 397,007 нм) часто смешивается с другой линией поглощения, вызванной ионизированной кальций известный как "H" ( оригинальное обозначение данный Йозеф фон Фраунгофер ). H-эпсилон отделен от Ca II H на 0,16 нм при 396,847 нм и не может быть разрешен в спектрах с низким разрешением. Линия H-дзета (переход 8 → 2) аналогичным образом смешана с нейтральным гелий линия, видимая у горячих звезд.
Смотрите также
- Астрономическая спектроскопия
- Модель Бора
- Спектральная серия водорода
- Серия Лайман
- Формула Ридберга
- Звездная классификация
- Теоретическое и экспериментальное обоснование уравнения Шредингера
Примечания
- ^ Нейв, К. Р. (2006). «Водородный спектр». Гиперфизика. Государственный университет Джорджии. Получено 2008-03-01.
- ^ а б c d е ж грамм Крамида, А., Ральченко, Ю., Ридер, Дж., И команда NIST ASD (2019). База данных атомных спектров NIST (версия 5.7.1), [онлайн]. Имеется в наличии: https://physics.nist.gov/asd [2020, 11 апреля]. Национальный институт стандартов и технологий, Гейтерсбург, доктор медицины. DOI: https://doi.org/10.18434/T4W30F
- ^ "CODATA Рекомендуемые значения фундаментальных физических констант: 2006 г." (PDF). Комитет по данным для науки и технологий (CODATA). NIST.


