Аллостерический модулятор - Allosteric modulator
В фармакология и биохимия, аллостерические модуляторы группа веществ, которые связываются с рецептор чтобы изменить реакцию этого рецептора на раздражитель. Некоторые из них, как бензодиазепины, являются наркотиками.[1] Сайт, с которым связывается аллостерический модулятор (т.е. аллостерический сайт) не то же самое, к которому эндогенный агонист рецептора будет связываться (т.е. ортостерический сайт). Модуляторы и агонисты могут называться рецепторами. лиганды.[2]
Модуляторы бывают только положительными, отрицательными или нейтральными. Положительные типы увеличивают ответ рецептора за счет увеличения вероятности связывания агониста с рецептором (т. Е. близость ), увеличивая его способность активировать рецептор (т.е. эффективность ), или оба. Отрицательные типы снижают аффинность и / или эффективность агонистов. Нейтральные типы не влияют на активность агонистов, но могут препятствовать связыванию других модуляторов с аллостерическим сайтом. Некоторые модуляторы также действуют как аллостерические агонисты.[2]
Термин «аллостерический» происходит от греческого языка. Аллос означает "другой", и стереосистемы, «твердое тело» или «форма». Это можно перевести как «другая форма», что означает конформационный изменения внутри рецепторов, вызванные модуляторами, посредством которых модуляторы влияют на функцию рецептора.[3]
Вступление
Аллостерические модуляторы могут изменять сродство и эффективность других веществ, действующих на рецептор. Модулятор может также увеличивать сродство и снижать эффективность или наоборот.[4] Близость это способность вещества связываться с рецептор. Эффективность - способность вещества активировать рецептор, выраженная в процентах от способности вещества активировать рецептор по сравнению с эндогенными рецепторами. агонист. Если эффективность равна нулю, вещество считается антагонист.[1]

Сайт, с которым связываются эндогенные агонисты, называется ортостерический сайт. Модуляторы не привязаны к этому сайту. Они привязываются к любым другим подходящим сайтам, которые называются аллостерические сайты.[2] После связывания модуляторы обычно изменяют трехмерную структуру (т.е. конформация ) рецептора. Это часто приводит к изменению ортостерического сайта, что может изменить эффект связывания агониста.[4] Аллостерические модуляторы также могут стабилизировать одну из нормальных конфигураций рецептора.[5]
На практике модуляция может быть сложной. Модулятор может работать как частичный агонист, что означает, что ему не нужен агонист, который он модулирует, для получения агонистических эффектов.[6] Кроме того, модуляция не может в равной степени влиять на сродство или эффективность различных агонистов. Если группа разных агонистов, которые должны обладать одинаковым действием, связываются с одним и тем же рецептором, некоторые модуляторы могут не модулировать их одинаково.[4]
Классы
Модулятор может иметь 3 эффекта в рецепторе. Один из них - способность или неспособность активировать рецептор (2 возможности). Два других - это аффинность и эффективность агонистов. Они могут быть увеличены, опущены или оставлены нетронутыми (3 и 3 возможности). Это дает 17 возможных комбинаций модулятора.[4] Их 18 (= 2 * 3 * 3), если также включен нейтральный тип модулятора.
По всем практическим соображениям эти комбинации можно обобщить только на 5 классов.[4] и 1 нейтральный:
- положительные аллостерические модуляторы (PAM) увеличивают аффинность и / или эффективность агонистов.[4] Клинические примеры: бензодиазепины подобно диазепам, алпразолам и хлордиазэпоксид, которые модулируют ГАМКА-рецепторы, и цинакальцет, который модулирует рецепторы, чувствительные к кальцию.[7]
- отрицательные аллостерические модуляторы (NAM) более низкое сродство к агонистам и / или эффективность.[4] Маравирок это лекарство, которое модулирует CCR5. Фенобам, несвежий и дипраглюрант экспериментальные GRM5 модуляторы.[7]
- NAM-агонисты действуют как NAM, но также как агонисты с агонистами, которые они модулируют, и без них.[4]
- нейтральные аллостерические модуляторы не влияют на активность агонистов, но связываются с рецептором и предотвращают связывание PAM и других модуляторов с одним и тем же рецептором, тем самым ингибируя их модуляцию.[4] Нейтральные модуляторы еще называют бесшумные аллостерические модуляторы (СЭМ)[6] или же нейтральные аллостерические лиганды (NAL). Примером является 5-метил-6- (фенилэтинил) пиридин (5MPEP ), а исследовательский химикат, который связывается с GRM5.[8]
Механизмы
Из-за разнообразия местоположений на рецепторах, которые могут служить сайтами для аллостерической модуляции, а также из-за отсутствия окружающих их регуляторных сайтов, аллостерические модуляторы могут действовать по самым разным механизмам.
Модулирующая привязка
Некоторые аллостерические модуляторы вызывают конформационный изменение их рецептора-мишени, которое увеличивает сродство связывания и / или эффективность агониста рецептора.[2] Примеры таких модуляторов включают: бензодиазепины и барбитураты, которые ГАМКА рецептор-положительные аллостерические модуляторы. Бензодиазепины, подобные диазепам связываются между α и γ субъединицами ГАМКА рецептор ионные каналы и увеличивайте частоту открытия канала, но не продолжительность каждого открытия. Барбитураты вроде фенобарбитал связывают β-домены и увеличивают продолжительность каждого открытия, но не частоту.[9]
Модулирующая развязка

Некоторые модуляторы действуют для стабилизации конформационных изменений, связанных с состоянием, связанным с агонистом. Это увеличивает вероятность того, что рецептор будет в активной конформации, но не мешает рецептору вернуться в неактивное состояние. С большей вероятностью оставаться в активном состоянии рецептор будет дольше связывать агонист. Рецепторы AMPA модулируется анирацетам и CX614 будет медленнее дезактивироваться и способствовать большему общему переносу катионов. Это, вероятно, достигается за счет связывания анирацетама или CX614 с задней частью «раковины моллюска», которая содержит сайт связывания для глутамат, стабилизация закрытой конформации, связанной с активацией рецептора AMPA.[5][9]
Предотвращение десенсибилизации
Общий сигнал может быть увеличен путем предотвращения десенсибилизация рецептора. Десенсибилизация предотвращает активацию рецептора, несмотря на присутствие агониста. Это часто вызвано многократным или интенсивным воздействием агониста. Устранение или уменьшение этого явления увеличивает общую активацию рецептора. Рецепторы AMPA восприимчивы к десенсибилизации из-за нарушения димерного интерфейса лиганд-связывающего домена. Циклотиазид было показано, что он стабилизирует этот интерфейс и медленную десенсибилизацию, и поэтому считается положительным аллостерическим модулятором.[5]
Стабилизация активной / неактивной конформации
Модуляторы могут напрямую регулировать рецепторы, а не влиять на связывание агониста. Подобно стабилизации связанной конформации рецептора, модулятор, который действует в этом механизме, стабилизирует конформацию, связанную с активным или неактивным состоянием. Это увеличивает вероятность того, что рецептор будет соответствовать стабилизированному состоянию и соответственно модулировать активность рецептора. Рецепторы, чувствительные к кальцию можно модулировать таким образом, регулируя pH. Более низкий pH увеличивает стабильность неактивного состояния и тем самым снижает чувствительность рецептора. Предполагается, что изменения зарядов, связанные с корректировкой pH, вызывают конформационные изменения рецептора, способствующие инактивации.[10]
Взаимодействие с агонистами
Модуляторы, которые увеличивают аффинность только частичных и полных агонистов, позволяют быстрее достичь максимума их эффективности при более низких концентрациях агонистов, т. Е. Наклон и плато кривая доза-ответ переход к более низким концентрациям.[4]
Модуляторы, повышающие эффективность, увеличивают максимальную эффективность частичных агонистов. Полные агонисты уже полностью активируют рецепторы, поэтому модуляторы не влияют на их максимальную эффективность, но несколько сдвигают их кривые ответа в сторону более низких концентраций агонистов.[4]
- % Ответа рецептора как функция от логарифмического агониста концентрация [Назад]
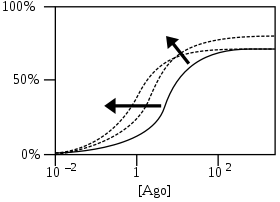
PAMs сдвиг начальной кривой ответа агониста (сплошная кривая) в сторону более низких концентраций агониста за счет увеличения аффинности и / или увеличения максимального ответа за счет увеличения эффективности. Пунктирные кривые - это 2 примера из многих возможных кривых после добавления PAM. Стрелки показывают примерное направление сдвигов кривых.[4]

PAM-агонисты работают как ПАМ, но сами являются агонистами. Таким образом, они вызывают ответ даже при минимальных концентрациях модулируемых ими агонистов.[4]

ПАМ-антагонисты увеличивают сродство к агонистам и смещают их кривые в сторону более низких концентраций, но поскольку они действуют как антагонисты, они также снижают максимальные ответы.[4]
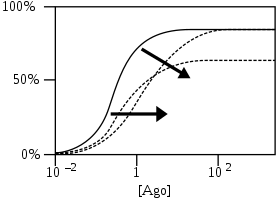
NAMs сдвигают кривые в сторону более высоких концентраций за счет уменьшения аффинности и / или более низких максимальных ответов за счет уменьшения эффективности. По сравнению с PAM эффекты NAM обратны.[4]
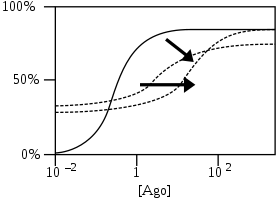
NAM-агонисты работают как NAM, но сами являются агонистами. Таким образом, они вызывают ответ даже при минимальных концентрациях модулируемых ими агонистов.[4]
Медицинское значение
Преимущества
Родственные рецепторы имеют ортостерические участки, которые очень похожи по структуре, так как мутации внутри этого участка может особенно снижаться функция рецепторов. Это может быть вредно для организмов, поэтому эволюция не часто одобряет такие изменения. Аллостерические сайты менее важны для функции рецепторов, поэтому они часто сильно различаются между родственными рецепторами. Вот почему, по сравнению с ортостерическими препаратами, аллостерические препараты могут быть очень сильными. специфический, т. е. нацелены их эффекты только на очень ограниченный набор типов рецепторов. Однако такая вариабельность аллостерических участков наблюдается также у разных видов, поэтому эффекты аллостерических препаратов сильно различаются между видами.[11]
Модуляторы не могут полностью включать или выключать рецепторы, поскольку действие модулятора зависит от эндогенных лигандов, таких как нейротрансмиттеры, которые имеют ограниченное и контролируемое производство внутри тела. Это может снизить передозировка риск по сравнению с аналогичным действием ортостерических препаратов. Это также может позволить использовать стратегию, при которой дозы, достаточно большие для насыщения рецепторов, можно безопасно принимать для продления действия лекарства.[4] Это также позволяет рецепторам активироваться в заданное время (то есть в ответ на стимул) вместо того, чтобы постоянно активироваться агонистом, независимо от времени или цели.[12]
Модуляторы влияют на существующие реакции в тканях и могут обеспечивать нацеливание лекарств на ткани. В этом отличие от ортостерических препаратов, которые, как правило, оказывают менее целенаправленное воздействие в организме на все рецепторы, с которыми они могут связываться.[4]
Также было показано, что у некоторых модуляторов отсутствует десенсибилизирующий эффект, который оказывают некоторые агонисты. Никотиновые рецепторы ацетилхолина например, быстро снижают чувствительность в присутствии агонистов, но поддерживают нормальную функцию в присутствии PAM.[13]
Приложения
Аллостерическая модуляция оказалась полезной для многих состояний, которые ранее трудно было контролировать с помощью других фармацевтических препаратов. К ним относятся:
- уменьшение «негативных» симптомов (дефицита), связанных с шизофрения используя экспериментальные mGluR5 положительные модуляторы, такие как 4-нитро-N- (1,3-дифенил-1ЧАС-пиразол-5-ил) бензамид (ВУ-29 ).[14]
- снижение тревожности за счет положительной модуляции рецепторов ГАМК.[9]
- снижение интенсивности нарушений сна за счет позитивной регуляции рецепторов ГАМК.[9]
- уменьшение депрессивных симптомов сильное депрессивное расстройство и шизофрения положительно модулируя дофаминовые рецепторы. Примеры включают DETQ, DPTQ и LY3154207, которые являются экспериментальными D1 рецептор положительные модуляторы.[15]
Смотрите также
- Аллостерическая регуляция
- Положительный аллостерический модулятор рецептора AMPA
- Положительный аллостерический модулятор рецептора ГАМК
- Аллостерический модулятор, отрицательный по рецепторам ГАМК
Рекомендации
- ^ а б Звонил HP, Риттер Дж. М., Флауэр Р. Дж., Хендерсон Дж. (2016). Фармакология Рэнга и Дейла (8-е изд.). Эльзевир. С. 6–20. ISBN 978-0-7020-5362-7.
- ^ а б c d Нойбиг Р. Р., Спеддинг М., Кенакин Т., Христопулос А. (декабрь 2003 г.). «Комитет Международного союза фармакологии по номенклатуре рецепторов и классификации лекарственных средств. XXXVIII. Обновление терминов и символов в количественной фармакологии» (PDF). Фармакологические обзоры. 55 (4): 597–606. Дои:10.1124 / пр.55.4.4. PMID 14657418.
- ^ Нельсон Д.Л., Кокс М.М. (2008). Принципы биохимии Ленингера (5-е изд.). W.H. Фримен. стр.162. ISBN 978-0-7167-7108-1.
- ^ а б c d е ж грамм час я j k л м п о п q р s т Кенакин Т.П. (2017). Фармакология в открытии и разработке лекарств: понимание реакции на лекарства (2-е изд.). Академическая пресса. С. 102–119. Дои:10.1016 / B978-0-12-803752-2.00005-3. ISBN 978-0-12-803752-2.
- ^ а б c Джин Р. и др. (2005-09-28). «Механизм действия положительных аллостерических модуляторов на рецепторы AMPA». Журнал неврологии. 25 (39): 9027–9036. Дои:10.1523 / JNEUROSCI.2567-05.2005. ISSN 0270-6474. ЧВК 6725607. PMID 16192394.
- ^ а б Стивенс Б., Гендель TM (2013). Олигомеризация и аллостерия хемокиновых рецепторов. Прогресс в молекулярной биологии и переводческой науке. 115. Академическая пресса. С. 4–5. Дои:10.1016 / B978-0-12-394587-7.00009-9. ISBN 978-0-12-394587-7. ЧВК 4072031. PMID 23415099.
- ^ а б Меланкон Б.Дж., Хопкинс С.Р., Вуд М.Р., Эммит К.А., Нисвендер С.М., Кристопулос А. и др. (Февраль 2012 г.). «Аллостерическая модуляция 7 трансмембранных рецепторов: теория, практика и возможности для открытия лекарств для ЦНС». Журнал медицинской химии. 55 (4): 1445–64. Дои:10.1021 / jm201139r. ЧВК 3349997. PMID 22148748.
- ^ Hellyer SD, Albold S, Wang T, Chen AN, May LT, Leach K, Gregory KJ (май 2018 г.). «5 аллостерических лигандов». Молекулярная фармакология. 93 (5): 504–514. Дои:10.1124 / моль.117.111518. PMID 29514854.
- ^ а б c d Арей Б.Дж. и др. (2014). Предвзятая передача сигналов в физиологии, фармакологии и терапии. Эльзевир. С. 187–189. Дои:10.1016 / B978-0-12-411460-9.00006-9. ISBN 9780124114609.
- ^ Билезикян Дж. П. и др. (2019). Принципы костной биологии (4-е изд.). Эльзевир. п. 542. Дои:10.1016 / B978-0-12-814841-9.00023-3. ISBN 9780128148419.
- ^ Лу С., Хе Икс, Ни Д., Чжан Дж. (Июль 2019 г.). "Открытие аллостерического модулятора: от интуиции до структурного дизайна". Журнал медицинской химии. 62 (14): 6405–6421. Дои:10.1021 / acs.jmedchem.8b01749. PMID 30817889. S2CID 73515780.
- ^ Ли Y и др. (10.01.2019). «Дизайн и синтез новых положительных аллостерических модуляторов α7-никотиновых ацетилхолиновых рецепторов со способностью спасать дефицит слухового прохода у мышей». Журнал медицинской химии. 62 (1): 159–173. Дои:10.1021 / acs.jmedchem.7b01492. ISSN 1520-4804. PMID 29587480.
- ^ Уильямс Д.К., Ван Дж., Папке Р.Л. (2011-10-15). «Положительные аллостерические модуляторы как подход к терапии, направленной на никотиновый ацетилхолиновый рецептор: преимущества и ограничения». Биохимическая фармакология. Никотиновые рецепторы ацетилхолина как терапевтические мишени: новые рубежи в фундаментальных исследованиях и клинической науке (спутник к собранию Общества неврологии в 2011 г.). 82 (8): 915–930. Дои:10.1016 / j.bcp.2011.05.001. ISSN 0006-2952. ЧВК 3162128. PMID 21575610.
- ^ Ayala JE, et al. (2009). «Положительные аллостерические модуляторы mGluR5 способствуют развитию LTP и LTD гиппокампа и улучшают пространственное обучение». Нейропсихофармакология. 34 (9): 2057–2071. Дои:10.1038 / npp.2009.30. ISSN 1740-634X. ЧВК 2884290. PMID 19295507.
- ^ Свенссон К.А. и др. (2019). «Положительные аллостерические модуляторы рецептора дофамина D1: новый механизм лечения нервно-психических расстройств». Нейропсихотерапия. Успехи фармакологии. 86. С. 273–305. Дои:10.1016 / bs.apha.2019.06.001. ISBN 9780128166680. ISSN 1557-8925. PMID 31378255.





