Антагонист допамина - Dopamine antagonist
| Антагонист дофаминовых рецепторов Дофаминергические блокаторы | |
|---|---|
| Класс препарата | |
 Структурная формула скелета галоперидола, а типичный антипсихотик | |
| Идентификаторы класса | |
| Использовать | Шизофрения, биполярное расстройство, тошнота и рвота, так далее. |
| Код УВД | N05A |
| Биологическая мишень | Дофаминовые рецепторы |
| внешняя ссылка | |
| MeSH | D012559 |
| В Викиданных | |
А антагонист дофамина, также известный как антидофаминергический и антагонист дофаминовых рецепторов (ДРА), является разновидностью препарат, средство, медикамент который блокирует дофаминовые рецепторы к рецепторный антагонизм. Наиболее нейролептики являются антагонистами дофамина, и поэтому они нашли применение в лечении шизофрения, биполярное расстройство, и стимулирующий психоз.[1] Несколько других дофамин антагонисты находятся противорвотные средства используется при лечении тошнота и рвота.
Рецепторная фармакология

Все дофаминовые рецепторы G-белковые рецепторы, и делятся на два класса в зависимости от того, с каким G-белком они связаны.[2] D1-подобный класс дофаминовых рецепторов связан с Gαs / olf и стимулирует аденилатциклаза производство, тогда как D2-подобный класс связан с Gαввод / вывод и, таким образом, подавляет продукцию аденилатциклазы.[2]
D1-подобные рецепторы: D1 и D5
D1-подобные рецепторы - D1 и D5 всегда находятся постсинаптически. В генах, кодирующих эти рецепторы, отсутствуют интроны, поэтому вариантов сплайсинга нет.
D1 рецепторы
- D1 рецепторы находятся в основном на нейронах прилежащее ядро[3] а также черная субстанция,[2] полосатое тело,[2] миндалина,[2] лобная кора[2] и обонятельная луковица и сетчатка[2]
- Также найдено (на нижних уровнях) в гипоталамус, таламус, мозжечок и гиппокамп[2]
- Периферически эти рецепторы были обнаружены в почечной артерии, брыжеечной артерии и селезеночной артерии, активация которых приводит к вазодилатации.[4] Кроме того, D1 рецепторы были обнаружены в почках[4]
D5 рецепторы
- Низкий уровень D5 рецепторы были найдены в гипоталамус, префронтальная кора и поясная извилина; а также области памяти, такие как гиппокамп, зубчатые извилины и энторинальная кора.[2]
- Кроме того, D5 рецепторы были обнаружены в почках[4]
D2-подобные рецепторы: D2, D3 и D4
D2-подобные рецепторы в отличие от D1-подобный класс, эти рецепторы находятся пре и постсинаптически. Гены, кодирующие эти рецепторы, имеют интроны, что приводит ко многим вариантам попеременного сплайсинга.
D2 рецепторы
- D2 рецепторы находятся в полосатом теле, черной субстанции, вентральной тегментальной области, гипоталамусе, коре головного мозга, перегородке, миндалине, гиппокампе и обонятельном бугорке.[2]
- Эти рецепторы также были обнаружены в сетчатке и гипофизе.[2]
- Периферически эти рецепторы были обнаружены в почечных, брыжеечных и селезеночных артериях, а также в коре и мозговом веществе надпочечников и в почках.[4]
D3 рецепторы
- D3 рецепторы высоко экспрессируются на нейронах островков Calleja и прилежащего ядра оболочки и слабо экспрессируются в таких областях, как компактная часть черной субстанции, гиппокамп, область перегородки и область вентральной тегментальной области.[2][3]
- Дополнительные исследования обнаружили эти рецепторы периферически в почках.[4]
D4 рецепторы
- D4 рецепторы находятся в миндалине, гиппокампе, гипоталамусе, бледном шаре, сетчатой части черной субстанции, таламусе, сетчатке и почках [2][4]
Последствия болезни
Дофаминергическая система вовлечена в различные расстройства. Болезнь Паркинсона возникает в результате потери дофаминергических нейронов в полосатом теле.[5] Более того, наиболее эффективные нейролептики блокируют D2 рецепторы, предполагая роль дофамина при шизофрении.[5][6][7] Дополнительные исследования предполагают, что нарушение регуляции дофамина связано с болезнью Хантингтона, СДВГ, синдромом Туретта, большой депрессией, маниакальной депрессией, зависимостью, гипертонией и дисфункцией почек.[5][7][8] Антагонисты дофаминовых рецепторов используются при некоторых заболеваниях, таких как шизофрения, биполярное расстройство, тошнота и рвота.[5]
- Мелатонин подавляет активность дофамина[9] как часть нормального циркадный ритм функции, хотя патологические дисбалансы были причастны к болезнь Паркинсона[10]
Побочные эффекты
Они могут включать в себя одно или несколько из следующих и продолжаться неопределенно долго даже после прекращения дофамин антагонист, особенно после длительного или высоких дозировок:
- Сердечно-сосудистые заболевания[11][12]
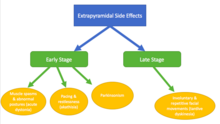
- Экстрапирамидные симптомы (EPS), связанные с типичными антипсихотическими средствами:
- Ранняя стадия - возникает в начале лечения или после увеличения дозы, пациенты выздоравливают при снижении дозы[13]
- Острый дистонии[13] - мышечные спазмы и устойчивые аномальные позы, начало которых наступает в течение нескольких дней; можно лечить холинолитиками
- факторы риска включают возраст, пол и семейный анамнез[13]
- Акатизия[14][13] - стимуляция и беспокойство, начало наступает в течение первых нескольких месяцев; можно лечить бета-блокаторы и бензодиазепины
- Паркинсонизм из-за воздействия на нигростриальный путь[14][13] - включает тремор, брадикинезию и ригидность мышц
- факторы риска включают возраст и пол[13]
- Острый дистонии[13] - мышечные спазмы и устойчивые аномальные позы, начало которых наступает в течение нескольких дней; можно лечить холинолитиками
- Поздняя стадия - возникает после длительного (месяцы-годы) лечения, симптомы сохраняются даже после снижения дозы[13]
- Поздняя дискинезия [14][13] - включает непроизвольные и повторяющиеся движения лица
- факторы риска включают возраст, расу и пол[13]
- Поздняя дискинезия [14][13] - включает непроизвольные и повторяющиеся движения лица
- Предполагается, что эти эффекты связаны с хронической блокадой D2 рецептор[14]
- Ранняя стадия - возникает в начале лечения или после увеличения дозы, пациенты выздоравливают при снижении дозы[13]
- Гиперпролактинемия из-за блокады D2 рецепторы в передней доле гипофиза, приводящие к увеличению выброса пролактина[11][15]
- Повышенный аппетит в том числе повышенная тяга и переедание, которые приводят к увеличению веса[16][11][17]
- Повышенный риск инсулин сопротивление[16]
- Сексуальная дисфункция[11][12]
- Метаболические изменения с повышенным риском ожирение и сахарный диабет 2 типа[16][11]
- Седация[11][12]
Примеры
Антипсихотики первого поколения (типичные)
Антипсихотики первого поколения используются для лечения шизофрении и часто сопровождаются экстрапирамидными побочными эффектами.[18]
- Бенперидол[18] связывает D2 и некоторые рецепторы серотонина.[19] Он очень легко впитывается и имеет высокий эффект первого прохода.[19]
- Хлорпромазин связывает D3 с наибольшим сродством, но также связывает D1, D2, D4 и D5[20][21]

- Клопентиксол[18]
- Дроперидол используется как антипсихотическое и противорвотное средство.[18]
- Галоперидол связывает D2, D3 и D4 с наибольшим сродством, но также связывает D1 и D5.[18][20][21]
- Флуфеназин связывает D2 и D3 с самым высоким сродством, но D1 и D5 также[20][18]
- Флупентиксол связывает D1, D2, D3, а D5[20] а также используется как антидепрессант.[18]
- Флуспирилен[18]
- Пенфлуридол[18]
- Перазин[18]
- Перфеназин[18]
- Пимозид связывает D2 и D3 с высоким сродством, также связывает D4 рецепторы[20][18]
- Сульпирид связывает D2 и D3[18][20] а также используется как антидепрессант.[18]
- Тиоридазин связывает D2, D3 и D4 с высоким сродством; также может связывать D1 и D5 при более высоких концентрациях[20]
Антипсихотики второго поколения (атипичные)
Эти препараты не только являются антагонистами дофамина указанного рецептора, но также действуют на рецептор серотонина 5HT.2А.[22] (Цитата несоответствующая) Эти препараты обладают меньшими экстрапирамидными побочными эффектами и с меньшей вероятностью влияют на уровень пролактина по сравнению с типичными антипсихотическими средствами. [23]
- Амисульприд связывает D2 и D3[24] и используется как нейролептик, антидепрессант, а также при биполярном расстройстве.[22] Он лечит как положительные, так и отрицательные симптомы шизофрении. [25]
- Азенапин связывает D2, D3 и D4[26] и используется для лечения биполярного расстройства и шизофрении.[27] Его побочные эффекты включают увеличение веса, но меньший риск ортостатической гипотензии и гиперпролактинемии.
- Арипипразол связывает D2 как частичный агонист, но противодействует D3.[28] Кроме того, арипипразол лечит шизофрению, биполярное расстройство (манию),[29] депрессия[22] и тиковые расстройства [28]
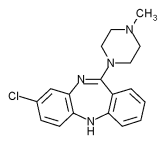
- Клозапин связывает D1 и D4 с самым высоким сродством, но все же связывает D2 и D3.[30] Клозапин уникален, потому что он назначается только в том случае, если лечение, по крайней мере, двумя другими нейролептиками не помогло из-за его очень тяжелых побочных эффектов.[31] Также требуется еженедельный подсчет лейкоцитов для отслеживания потенциальных нейтропения.[31]
- Локсапин связывает D2, D3 и D4 с высоким сродством; также может связывать D1.[32] Локсапин часто используется для лечения возбужденных и агрессивных пациентов с нервно-психическими расстройствами, такими как биполярное расстройство и шизофрения. [33]
- Немонаприд связывает D3, D4 и D5. [34]
- Оланзапин связывает все рецепторы[35] и используется для лечения положительных и отрицательных симптомов шизофрении, а также биполярного расстройства и депрессии.[36] Это было связано со значительным увеличением веса.[37]
- Кветиапин связывает D1, D2 и D3 и может связывать D4 в высоких концентрациях.[35] Он используется для лечения положительных симптомов шизофрении,[37] биполярное расстройство и депрессия.[36]
- Палиперидон связывает D2, D3 и D4 с высоким сродством; также может связывать D1 и D5.[38]
- Ремоксиприд связывает D2 рецепторы с относительно низким сродством.[35] [39][36]
- Рисперидон связывает D2, D3 и D4 рецепторы.[36][35][38] Рисперидон лечит не только положительные и отрицательные симптомы шизофрении.[37] но также лечит биполярное расстройство.[36]
- Tiapride блоки D2 и D3 и используется как антипсихотическое средство.[36] Он также часто используется для лечения дискинезий, психомоторного возбуждения, тиков, хореи Хантингтона и алкогольной зависимости.[40]
- Зипразидон блокирует D2 рецептор [41] и используется для лечения шизофрении, депрессии и биполярного расстройства.[36] Существуют разногласия по поводу того, лечит ли зипразидон негативные симптомы, и он имеет хорошо документированные побочные эффекты со стороны желудочно-кишечного тракта. [37]
Антагонисты дофамина, используемые для лечения тошноты и рвоты
- Домперидон является периферически селективным антагонистом рецептора дофамина D2, используемым в качестве противорвотного, гастропрокинетического и галактагогического средства.
- Бромоприд связывает кишечный D2 рецепторы[42] а также лечит гастропарез.[43]
- Метоклопрамид также лечит гастропарез[43]
Антагонисты используются только в исследовательских целях.
- Этиклопрайд связывает D2 и D3 с высоким сродством, но также связывает D4[44][45][46]
- Нафадотрид связывает D2 и D3[43][44][45]
- Раклопрайд связывает D2 и D3[43][44] и могут быть помечены радиоактивной меткой и использоваться в ПЭТ-визуализации для выявления прогрессирования болезни Хантингтона.[47]
Рекомендации
- ^ Болье Дж. М., Гайнетдинов Р. Р. (март 2011 г.). «Физиология, сигнализация и фармакология дофаминовых рецепторов». Фармакологические обзоры. 63 (1): 182–217. Дои:10.1124 / пр.110.002642. PMID 21303898.
- ^ а б c d е ж грамм час я j k л м Болье Дж. М., Гайнетдинов Р. Р. (март 2011 г.). «Физиология, сигнализация и фармакология дофаминовых рецепторов». Фармакологические обзоры. 63 (1): 182–217. Дои:10.1124 / пр.110.002642. PMID 21303898.
- ^ а б Соколофф П., Диаз Дж., Ле Фолль Б., Гийен О., Лериш Л., Безар Е., Гросс С. (февраль 2006 г.). «Рецептор допамина D3: терапевтическая мишень для лечения нервно-психических расстройств». Мишени для лекарств от ЦНС и неврологических расстройств. 5 (1): 25–43. Дои:10.2174/187152706784111551. PMID 16613552.
- ^ а б c d е ж Missale C, Nash SR, Robinson SW, Jaber M, Caron MG (январь 1998 г.). «Дофаминовые рецепторы: от структуры к функции». Физиологические обзоры. 78 (1): 189–225. Дои:10.1152 / Physrev.1998.78.1.189. PMID 9457173.
- ^ а б c d Болье Дж. М., Гайнетдинов Р. Р. (март 2011 г.). «Физиология, сигнализация и фармакология дофаминовых рецепторов». Фармакологические обзоры. 63 (1): 182–217. Дои:10.1124 / пр.110.002642. PMID 21303898.
- ^ Seeman P (август 2006 г.). «Ориентация на дофаминовый рецептор D2 при шизофрении». Мнение эксперта о терапевтических целях. 10 (4): 515–31. Дои:10.1517/14728222.10.4.515. PMID 16848689.
- ^ а б Missale C, Nash SR, Robinson SW, Jaber M, Caron MG (январь 1998 г.). «Дофаминовые рецепторы: от структуры к функции». Физиологические обзоры. 78 (1): 189–225. Дои:10.1152 / Physrev.1998.78.1.189. PMID 9457173.
- ^ Иверсен С.Д., Иверсен Л.Л. (май 2007 г.). «Дофамин: 50 лет в перспективе». Тенденции в неврологии. 30 (5): 188–93. Дои:10.1016 / j.tins.2007.03.002. PMID 17368565.
- ^ Зисапель Н. (декабрь 2001 г.). «Взаимодействия мелатонина и дофамина: от базовой нейрохимии до клинических условий». Клеточная и молекулярная нейробиология. 21 (6): 605–16. Дои:10.1023 / А: 1015187601628. PMID 12043836.
- ^ Уиллис ГЛ (2008). «Болезнь Паркинсона как нейроэндокринное нарушение циркадной функции: дисбаланс дофамин-мелатонин и зрительная система в генезе и прогрессировании дегенеративного процесса». Обзоры в неврологии. 19 (4–5): 245–316. Дои:10.1515 / revneuro.2008.19.4-5.245. PMID 19145986.
- ^ а б c d е ж Молодой С.Л., Тейлор М., Лори С.М. (апрель 2015 г.). ""Сначала не навреди. «Систематический обзор распространенности и лечения побочных эффектов антипсихотических препаратов». Журнал психофармакологии. 29 (4): 353–62. Дои:10.1177/0269881114562090. PMID 25516373.
- ^ а б c Арана GW (2000). «Обзор побочных эффектов, вызванных типичными антипсихотическими средствами». Журнал клинической психиатрии. 61 (Дополнение 8): 5–11, обсуждение 12–3. PMID 10811237.
- ^ а б c d е ж грамм час я Divac N, Prostran M, Jakovcevski I, Cerovac N (2014). «Антипсихотики второго поколения и побочные экстрапирамидные эффекты». BioMed Research International. 2014: 656370. Дои:10.1155/2014/656370. ЧВК 4065707. PMID 24995318.
- ^ а б c d Missale C, Nash SR, Robinson SW, Jaber M, Caron MG (январь 1998 г.). «Дофаминовые рецепторы: от структуры к функции». Физиологические обзоры. 78 (1): 189–225. Дои:10.1152 / Physrev.1998.78.1.189. PMID 9457173.
- ^ Надаль Р. (2001). «Фармакология атипичного антипсихотического ремоксиприда, антагониста дофаминового рецептора D2». Обзоры препаратов для ЦНС. 7 (3): 265–82. Дои:10.1111 / j.1527-3458.2001.tb00199.x. ЧВК 6741677. PMID 11607043.
- ^ а б c Дэн Ц. (сентябрь 2013 г.). «Влияние антипсихотических препаратов на аппетит, вес и инсулинорезистентность». Клиники эндокринологии и метаболизма Северной Америки. 42 (3): 545–63. Дои:10.1016 / j.ecl.2013.05.006. PMID 24011886.
- ^ Мортимер AM (март 2004 г.). «Как выбирать между атипичными нейролептиками? Преимущества амисульприда». Международный журнал нейропсихофармакологии. 7 Приложение 1 (5): S21-5. Дои:10.1017 / S1461145704004134. PMID 14972081.
- ^ а б c d е ж грамм час я j k л м п о Болье Дж. М., Гайнетдинов Р. Р. (март 2011 г.). «Физиология, сигнализация и фармакология дофаминовых рецепторов». Фармакологические обзоры. 63 (1): 182–217. Дои:10.1124 / пр.110.002642. PMID 21303898.
- ^ а б Leucht S, Hartung B (апрель 2005 г.). «Бенперидол от шизофрении». Кокрановская база данных систематических обзоров (2): CD003083. Дои:10.1002 / 14651858.CD003083.pub2. ЧВК 7017029. PMID 15846648.
- ^ а б c d е ж грамм час Соколофф П., Диаз Дж., Ле Фолль Б., Гийен О., Лериш Л., Безар Е., Гросс С. (февраль 2006 г.). «Рецептор допамина D3: терапевтическая мишень для лечения нервно-психических расстройств». Мишени для лекарств от ЦНС и неврологических расстройств. 5 (1): 25–43. Дои:10.2174/187152706784111551. PMID 16613552.
- ^ а б Missale C, Nash SR, Robinson SW, Jaber M, Caron MG (январь 1998 г.). «Дофаминовые рецепторы: от структуры к функции». Физиологические обзоры. 78 (1): 189–225. Дои:10.1152 / Physrev.1998.78.1.189. PMID 9457173.
- ^ а б c Болье Дж. М., Гайнетдинов Р. Р. (март 2011 г.). «Физиология, сигнализация и фармакология дофаминовых рецепторов». Фармакологические обзоры. 63 (1): 182–217. Дои:10.1124 / пр.110.002642. PMID 21303898.
- ^ Надаль Р. (2001). «Фармакология атипичного антипсихотического ремоксиприда, антагониста дофаминового рецептора D2». Обзоры препаратов для ЦНС. 7 (3): 265–82. Дои:10.1111 / j.1527-3458.2001.tb00199.x. ЧВК 6741677. PMID 11607043.
- ^ Соколофф П., Диаз Дж., Ле Фолль Б., Гийен О., Лериш Л., Безар Е., Гросс С. (февраль 2006 г.). «Рецептор допамина D3: терапевтическая мишень для лечения нервно-психических расстройств». Мишени для лекарств от ЦНС и неврологических расстройств. 5 (1): 25–43. Дои:10.2174/187152706784111551. PMID 16613552.
- ^ Мортимер AM (март 2004 г.). «Как выбирать между атипичными антипсихотиками? Преимущества амисульприда». Международный журнал нейропсихофармакологии. 7 Приложение 1 (5): S21-5. Дои:10.1017 / S1461145704004134. PMID 14972081.
- ^ Стоунер С.К., Пейс HA (май 2012 г.). «Азенапин: клинический обзор антипсихотика второго поколения». Клиническая терапия. 34 (5): 1023–40. Дои:10.1016 / j.clinthera.2012.03.002. PMID 22494521.
- ^ Scheidemantel T, Коробкова I, Rej S, Sajatovic M (2015-12-04). «Азенапин при биполярном расстройстве». Психоневрологические заболевания и лечение. 11: 3007–17. Дои:10.2147 / NDT.S78043. ЧВК 4675633. PMID 26674884.
- ^ а б Ян К.С., Хуанг Х., Чжан Л.Л., Чжу ЧР, Го Ц. (июль 2015 г.). «Арипипразол для лечения тиков у детей: систематический обзор и метаанализ». BMC Psychiatry. 15: 179. Дои:10.1186 / s12888-015-0504-z. ЧВК 4518630. PMID 26220447.
- ^ Браун Р., Тейлор М.Дж., Геддес Дж. (Декабрь 2013 г.). «Арипипразол отдельно или в комбинации при острой мании» (PDF). Кокрановская база данных систематических обзоров (12): CD005000. Дои:10.1002 / 14651858.CD005000.pub2. PMID 24346956.
- ^ Соколофф П., Диаз Дж., Ле Фолль Б., Гийен О., Лериш Л., Безар Е., Гросс С. (февраль 2006 г.). «Рецептор допамина D3: терапевтическая мишень для лечения нервно-психических расстройств». Мишени для лекарств от ЦНС и неврологических расстройств. 5 (1): 25–43. Дои:10.2174/187152706784111551. PMID 16613552.
- ^ а б Мортимер AM (март 2004 г.). «Как выбирать между атипичными антипсихотиками? Преимущества амисульприда». Международный журнал нейропсихофармакологии. 7 Приложение 1 (5): S21-5. Дои:10.1017 / S1461145704004134. PMID 14972081.
- ^ Попович Д., Нусс П., Виета Е. (01.04.2015). «Пересмотр локсапина: систематический обзор». Анналы общей психиатрии. 14: 15. Дои:10.1186 / s12991-015-0053-3. ЧВК 4391595. PMID 25859275.
- ^ Резюме Поллака (июль 2016 г.). «Ингаляционный локсапин для неотложного лечения острого возбуждения, связанного с шизофренией или биполярным расстройством». Текущие медицинские исследования и мнения. 32 (7): 1253–60. Дои:10.1185/03007995.2016.1170004. PMID 27121764.
- ^ Missale C, Nash SR, Robinson SW, Jaber M, Caron MG (январь 1998 г.). «Дофаминовые рецепторы: от структуры к функции». Физиологические обзоры. 78 (1): 189–225. Дои:10.1152 / Physrev.1998.78.1.189. PMID 9457173.
- ^ а б c d Соколофф П., Диаз Дж., Ле Фолль Б., Гийен О., Лериш Л., Безар Е., Гросс С. (февраль 2006 г.). «Рецептор допамина D3: терапевтическая мишень для лечения нервно-психических расстройств». Мишени для лекарств от ЦНС и неврологических расстройств. 5 (1): 25–43. Дои:10.2174/187152706784111551. PMID 16613552.
- ^ а б c d е ж грамм Болье Дж. М., Гайнетдинов Р. Р. (март 2011 г.). «Физиология, сигнализация и фармакология дофаминовых рецепторов». Фармакологические обзоры. 63 (1): 182–217. Дои:10.1124 / пр.110.002642. PMID 21303898.
- ^ а б c d Мортимер AM (март 2004 г.). «Как выбирать между атипичными нейролептиками? Преимущества амисульприда». Международный журнал нейропсихофармакологии. 7 Приложение 1 (5): S21-5. Дои:10.1017 / S1461145704004134. PMID 14972081.
- ^ а б Корена-Маклеод М (июнь 2015 г.). «Сравнительная фармакология рисперидона и палиперидона». Лекарства в исследованиях и разработках. 15 (2): 163–74. Дои:10.1007 / s40268-015-0092-х. ЧВК 4488186. PMID 25943458.
- ^ Надаль Р. (2001). «Фармакология атипичного антипсихотического ремоксиприда, антагониста дофаминового рецептора D2». Обзоры препаратов для ЦНС. 7 (3): 265–82. Дои:10.1111 / j.1527-3458.2001.tb00199.x. ЧВК 6741677. PMID 11607043.
- ^ Dose M, Lange HW (январь 2000 г.). «Бензамид тиаприд: лечение экстрапирамидных моторных и других клинических синдромов». Фармакопсихиатрия. 33 (1): 19–27. Дои:10.1055 / с-2000-7964. PMID 10721880.
- ^ Шталь С.М., Шаеган Д.К. (2003). «Психофармакология зипразидона: рецептор-связывающие свойства и реальная психиатрическая практика». Журнал клинической психиатрии. 64 Дополнение 19: 6–12. PMID 14728084.
- ^ Тонини М., Чиполлина Л., Полуцци Е., Crema F, Corazza GR, De Ponti F (февраль 2004 г.). «Обзорная статья: клинические последствия блокады кишечных и центральных рецепторов D2 антидофаминергическими желудочно-кишечными прокинетиками». Пищевая фармакология и терапия. 19 (4): 379–90. Дои:10.1111 / j.1365-2036.2004.01867.x. PMID 14871277.
- ^ а б c d Болье Дж. М., Гайнетдинов Р. Р. (март 2011 г.). «Физиология, сигнализация и фармакология дофаминовых рецепторов». Фармакологические обзоры. 63 (1): 182–217. Дои:10.1124 / пр.110.002642. PMID 21303898.
- ^ а б c Соколофф П., Диаз Дж., Ле Фолль Б., Гийен О., Лериш Л., Безар Е., Гросс С. (февраль 2006 г.). «Рецептор допамина D3: терапевтическая мишень для лечения нервно-психических расстройств». Мишени для лекарств от ЦНС и неврологических расстройств. 5 (1): 25–43. Дои:10.2174/187152706784111551. PMID 16613552.
- ^ а б Missale C, Nash SR, Robinson SW, Jaber M, Caron MG (январь 1998 г.). «Дофаминовые рецепторы: от структуры к функции». Физиологические обзоры. 78 (1): 189–225. Дои:10.1152 / Physrev.1998.78.1.189. PMID 9457173.
- ^ Мартель JL, Надер MA (2008). «Обзор открытия, фармакологической характеристики и поведенческих эффектов антагониста дофаминовых D2-подобных рецепторов этиклоприда». ЦНС нейробиология и терапия. 14 (3): 248–62. Дои:10.1111 / j.1755-5949.2008.00047.x. ЧВК 2753830. PMID 18801115.
- ^ Пагано Дж., Никколини Ф., Политис М (июнь 2016 г.). «Текущее состояние ПЭТ-визуализации при болезни Хантингтона». Европейский журнал ядерной медицины и молекулярной визуализации. 43 (6): 1171–82. Дои:10.1007 / s00259-016-3324-6. ЧВК 4844650. PMID 26899245.
внешняя ссылка
- Допамин + антагонисты в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)

