Кортистатины - Cortistatins
 | |
| Имена | |
|---|---|
| Название ИЮПАК (1р,2р,3S,5р, 8β, 17β) -3- (Диметиламино) -17- (изохинолин-7-ил) -5,8-эпокси-9,19-цикло-9,10-секоандроста-9 (11), 10-диен-1 , 2-диол | |
| Другие имена Кортистатин А | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C30ЧАС36N2О3 | |
| Молярная масса | 472.629 г · моль−1 |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
В кортистатины группа стероидные алкалоиды впервые изолирован в 2006 г. от морская губка Corticium simplex.[1] Кортистатины были впервые обнаружены при поиске природных соединений, которые ингибируют пролиферацию эндотелиальных клеток пупочной вены человека (HUVEC ), причем кортистатин А является наиболее мощным соединением в классе.[2]
Группа Шаир из Гарварда вместе с сотрудниками показала, что кортистатин А является сильнодействующим и селективным ингибитором CDK8 и CDK19, киназы, которые связаны с комплексом медиатора.[3] Из 386 оцененных киназ кортистатин А ингибировал только CDK8 и CDK19, показывая, что он является одним из наиболее селективных ингибиторы киназ. Также было показано, что кортистатин А сильно подавляет рост острый миелоидный лейкоз клеток и AML в двух моделях мышей in vivo. Идентификация доминантных устойчивых к лекарственным средствам аллелей CDK8 и CDK19 демонстрирует, что эти киназы опосредуют активность кортистатина А в клетках AML. Таким образом, ингибирование CDK8 и CDK19 - это новый терапевтический подход к AML. Кортистатин А вызывал избирательную и непропорциональную регуляцию супер-энхансер -ассоциированные гены в клетках AML, которые способствовали его противолейкемической активности. Эта работа показала, что CDK8 и CDK19 являются негативными регуляторами генов, ассоциированных с суперэнхансерами, при AML.
Дигидрокортистатин А подавляет вирусная репликация в клетках, инфицированных ВИЧ через привязку к Tat белок.[4]
Кортистатин А был синтезирован Шаиром,[5] Майерс, Баран[6] и Николау лаборатории.
Химические структуры

Кортистатин А

Кортистатин B

Кортистатин С
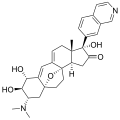
Кортистатин D

Кортистатин E
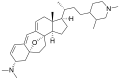
Кортистатин F

Кортистатин G

Кортистатин H

Кортистатин J
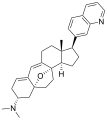
Кортистатин К

Кортистатин L
Рекомендации
- ^ Аоки, S; Ватанабэ, Й; Санагава, М; Сетиаван, А; Котоку, Н; Кобаяши, М. (2006). "Кортистатины A, B, C и D, антиангиогенные стероидные алкалоиды, от морской губка Corticium simplex ». Журнал Американского химического общества. 128 (10): 3148–9. Дои:10.1021 / ja057404h. PMID 16522087.
- ^ Аоки, S; Ватанабэ, Й; Танабэ, Д; Араи, М; Суна, Н; Миямото, К; Цудзибо, H; Tsujikawa, K; Ямамото, Х (2007). «Взаимосвязь структура-активность и биологические свойства кортистатинов, антиангиогенных губчатых стероидных алкалоидов». Биоорганическая и медицинская химия. 15 (21): 6758–62. Дои:10.1016 / j.bmc.2007.08.017. PMID 17765550.
- ^ Пелиш, Генри Э .; Liau, Brian B .; Нитулеску, Иоана I .; Тангпирачайкул, Анупонг; Poss, Zachary C .; Сильва, Диого Х. Да; Карузо, Бриттани Т .; Арефолов Александр; Фадей, Олугбеминии (2015). «Ингибирование медиаторной киназы дополнительно активирует гены, ассоциированные с суперэнхансером, при ОМЛ». Природа. 526 (7572): 273–276. Дои:10.1038 / природа14904. ЧВК 4641525. PMID 26416749.
- ^ Mousseau, G .; Clementz, M. A .; Bakeman, W. N .; Nagarsheth, N .; Cameron, M .; Shi, J .; Баран, П .; Fromentin, R.M .; Chomont, N .; Валенте, С. Т. (2012). «Аналог природного стероидного алкалоидного кортистатина, который эффективно подавляет Tat-зависимую транскрипцию ВИЧ». Клеточный хозяин и микроб. 12 (1): 97–108. Дои:10.1016 / j.chom.2012.05.016. ЧВК 3403716. PMID 22817991.
- ^ Ли, Хон Мён; Ньето-Оберхубер, Кристина; Шаир, Мэтью Д. (17 декабря 2008 г.). «Энантиоселективный синтез (+) - кортистатина А, мощного и селективного ингибитора пролиферации эндотелиальных клеток». Журнал Американского химического общества. 130 (50): 16864–16866. Дои:10.1021 / ja8071918. ISSN 0002-7863. PMID 19053422.
- ^ Шенви, Райан А .; Герреро, Карлос А .; Ши, Джун; Ли, Чжуан-Чжуан; Баран, Фил С. (2008). «Синтез (+) - кортистатина А». Журнал Американского химического общества. 130 (23): 7241–7243. Дои:10.1021 / ja8023466. ЧВК 2652360. PMID 18479104.











