Растрепанный - Dishevelled
| Растрепанный конкретный домен | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||
| Идентификаторы | |||||||||||
| Символ | Растрепанный | ||||||||||
| Pfam | PF02377 | ||||||||||
| ИнтерПро | IPR003351 | ||||||||||
| PROSITE | PDOC50841 | ||||||||||
| |||||||||||
Растрепанный (Dsh) - это семья белки участвует в канонических и неканонических Wnt сигнальные пути. Dsh (Dvl у млекопитающих) является цитоплазматический фосфопротеин который действует непосредственно после завитый рецепторы.[1] Он получил свое название от своего первоначального открытия в мухи, где наблюдалась мутация в растрепанном гене, вызывающая неправильную ориентацию волос на теле и крыльях.[2] У рыбок данио есть гомологи позвоночных, Xenopus (Xdsh), мышей (Двл1, -2, -3) и люди (ДВЛ-1, -2, -3). Dsh передает сложные сигналы Wnt в тканях и клетках в нормальном и ненормальном контексте.[2] [3] Считается, что он взаимодействует с новым белком, SPATS1, при регулировании пути передачи сигналов Wnt.[4]
Растрепанный играет важную роль как у эмбриона, так и у взрослого человека, начиная от клеточная дифференциация и полярность клеток к социальному поведению.[2]
Члены
Есть три человеческих гена, которые кодируют растрепанные белки:[5]
Функция
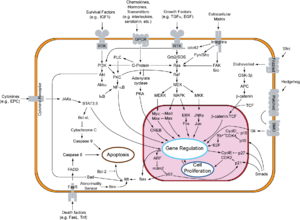
DVL является неотъемлемой частью канонического пути Wnt (зависимого от β-катенина) и неканонического пути (независимого от β-катенина).[2] В любом из них DVL действует ниже рецептора Frizzled, хотя пути различаются.[6]
Wnt канонический путь
Канонический путь Wnt, также известный как путь Wnt / β-catenin, активируется во время развития, регуляции, дифференцировки клеток и пролиферации.[7] Канонический путь Wnt перемещает DVL между цитоплазмой и ядром посредством консервативной ядерной экспортной последовательности (NES) и последовательности ядерной локализации (NLS), которые необходимы для правильного функционирования.[3] Связывание Wnt с рецепторами Frizzled помогает рекрутировать DVL на мембрану, обеспечивая место для Axin и GSK3β для связывания и фосфорилирования LRP5 / 6 (трансмембранного белка, связанного с рецептором липопротеинов низкой плотности), предотвращая конститутивную деградацию β-катенина.[6][7] Предотвращение этой деградации DVL позволяет накапливать β-катенин в ядре, где он действует как коактиватор для TCF (T-клеточного фактора), чтобы активировать Wnt-чувствительные гены.[3][7] Напротив, без передачи сигналов Wnt комплекс разрушения, состоящий из APC, CKI, GSK3β и Axin, разрушает накопление β-катенина, сохраняя концентрацию β-катенина в клетке на низком уровне.[7]
Wnt неканонические пути
Путь планарной полярности клеток
Путь планарной полярности клеток (PCP) является наиболее заметным путем, независимым от β-катенина - сигнал Wnt принимается рецептором Frizzled, который передает сигналы на DVL, который затем действует как точка ветвления для двух независимых путей, что приводит к активации малых ГТФаз Rho и Rac.[3][7] Для ветви Rho сигналы Wnt индуцируют DVL к формированию комплекса с Daam1 (связанный с Disheveled активатор морфогенеза 1).[3] Затем этот комплекс взаимодействует с фактором обмена нуклеотидов гуанина WGEF (GEF слабого сходства), который активирует следующие эффекторы, такие как Rho-GTPase и Rho-ассоциированная киназа (ROCK), которая активирует архитектуру актина и цитоскелета в клетке. Для ветви Rac DVL активирует Rac GTPase.[3] Активация Rac GTPase стимулирует нижестоящую эффекторную N-концевую киназу c-Jun (JNK), которая контролирует перестройки в цитоскелете и экспрессию генов.[7] Более конкретно, он регулирует полярность и движение клетки в процессах у позвоночных (таких как Xenopus), включая гаструляцию, закрытие нервной трубки и ориентацию стереоцилий во внутреннем ухе.[7]
Wnt-кальциевый путь
Другой путь, независимый от β-катенина, - это Wnt-Ca2+ путь, который участвует в раке, воспалении и нейродегенерации. Wnt запускает опосредованную Frizzled активацию, вызывая каскад, ведущий к Ca2+ релиз, который активирует эффекторы (например, CaMKII ), которые контролируют транскрипцию генов, имеющих отношение к клеточной судьбе и миграции клеток.[7] Этот путь может выключить каскад Wnt / β-катенин, а также может быть ингибирован активацией DVL.[8]
Структура
Существует пять основных высококонсервативных регионов, которые существуют во всех вариантах DVL. К ним относятся аминоконцевой домен DIX (N-конец), PDZ (центральный) домен, карбоксиконцевой домен DEP (C-конец) и две области с положительно заряженными аминокислотными остатками.[3] Между доменами DIX и PDZ существует область с тяжелым пролином, а между доменами DIX и PDZ имеется в основном основная область, которая имеет консервативные остатки серина и треонина. Эти области опосредуют белок-белковые взаимодействия и помогают сигналам DVL-канала либо в β-катенин, либо в независимых от β-катенина путях.[3] Кроме того, существует консервативная последовательность ядерного экспорта (NES) и последовательность ядерной локализации (NLS), способность которых перемещать DVL между цитоплазмой и ядром может быть важной частью его функции.[3]

Домен DIX (ДиShevelled-AИксв)
Расположенный рядом с N-концевой областью DVL и состоящий примерно из 82-85 аминокислот для человеческого белка DVL, DIX обнаруживается в таких белках, как Axin и белок спиральной спирали, содержащий домен DIX I (DIXdc1 или Ccd1). Домен DIX DVL имеет пять β-цепей и одну α-спираль с высококонсервативными аминокислотными остатками.[3][6]
PDZ Домен
PDZ, название которого состоит из инициалов первых трех идентифицированных белков, которые разделяют этот общий структурный домен (пбелок синаптической плотности ost (PSD95), Dсупрессор больших опухолей диска розофилы (Dlg1) и Zonula occludens-1 (zo-1)), лежит в центральной области DVL. PDZ обычно содержит около 73 аминокислот в каждом белке DVL человека и состоит из 5-6 β-цепей и 2-3 α-спиралей. [3][6] Этот мотив играет решающую роль в связывании лиганда и конформационных свойствах белка DVL. Эта область опосредует многие белок-белковые взаимодействия и регулирует множество биологических процессов.[3]
Домен DEP (DровныйEGL-10-плеэкстрин)
DEP, который находится в C-концевом домене DVL, содержит 75 аминокислот в белках DVL человека и имеет три α-спирали, β-шпильку и две короткие β-цепи.[3][6] Этот домен обеспечивает взаимодействие между DVL и DAAM1, тем самым активируя неканонический путь. Этот домен также имеет результаты, которые подтверждают утверждения о том, что домен DEP отвечает за нацеливание белков DVL на мембрану при стимуляции сигнала Wnt. Домен DEP также может быть важен для сборки функциональных сигнаносом и для передачи сигнала Wnt в ядро.[3]
NES и NLS регионы
В дополнение к этим консервативным областям, DVL имеет как NES, так и NLS, которые регулируют клеточную локализацию DVL посредством перемещения между ядром и цитоплазмой. NLS находится между доменами PDZ и DEP, а NES - между DEP и C-концом DVL.[3]
Растрепанные посттрансляционные модификации
Есть три типа сетевых ДВЛ посттрансляционная модификация - фосфорилирование, убиквитинирование и метилирование. Фосфорилирование является наиболее хорошо изученным и, по-видимому, действует таким образом, что сайт-специфическое фосфорилирование может вызывать широкий спектр биологических реакций.[3] Убиквитинирование - это посттрансляционная модификация, которая играет роль в регуляции деградации DVL.
Выравнивание растрепанного специфичного домена

Рекомендации
- ^ Пентон А., Водарц А., Нусе Р. (июнь 2002 г.). «Мутационный анализ растрепанного у дрозофилы определяет новые домены растрепанного белка, а также новые супрессирующие аллели аксина». Генетика. 161 (2): 747–62. ЧВК 1462152. PMID 12072470.
- ^ а б c d Валлингфорд Дж. Б., Хабас Р. (октябрь 2005 г.). «Биология развития Disheveled: загадочный белок, управляющий клеточной судьбой и клеточной полярностью». Разработка. 132 (20): 4421–36. Дои:10.1242 / dev.02068. PMID 16192308.
- ^ а б c d е ж грамм час я j k л м п о п Шарма М., Кастро-Пьедрас I, Симмонс Г.Э., Прюитт К. (июль 2018 г.). «Растрепанный: мастерский проводник сложных сигналов Wnt». Сотовая связь. 47: 52–64. Дои:10.1016 / j.cellsig.2018.03.004. ЧВК 6317740. PMID 29559363.
- ^ Zhang H, Zhang H, Zhang Y, Ng SS, Ren F, Wang Y, Duan Y, Chen L, Zhai Y, Guo Q, Chang Z (ноябрь 2010 г.). «Белок, взаимодействующий с доменом Disheveled-DEP (DDIP), ингибирует передачу сигналов Wnt, способствуя деградации TCF4 и разрушая комплекс TCF4 / бета-катенин». Сотовая связь. 22 (11): 1753–60. Дои:10.1016 / j.cellsig.2010.06.016. PMID 20603214.
- ^ Ли Ю.Н., Гао И, Ван Х.Й. (февраль 2008 г.). «Дифференциальное посредничество канонического пути Wnt с помощью Dishevelleds-1, -2 и -3 млекопитающих». Сотовая связь. 20 (2): 443–52. Дои:10.1016 / j.cellsig.2007.11.005. ЧВК 2233603. PMID 18093802.
- ^ а б c d е Млодзик М (2016). Семья растрепанных белков: все еще загадка после более чем 20 лет молекулярных исследований. Актуальные темы биологии развития. 117. С. 75–91. Дои:10.1016 / bs.ctdb.2015.11.027. ISBN 9780128013823. ЧВК 4939608. PMID 26969973.
- ^ а б c d е ж грамм час Гомес-Орте Э, Саенс-Нарцисо Б., Морено С., Кабельо Дж. (Сентябрь 2013 г.). «Множественные функции неканонического пути Wnt». Тенденции в генетике. 29 (9): 545–53. Дои:10.1016 / j.tig.2013.06.003. PMID 23846023.
- ^ Гао Ц., Чен Ю.Г. (май 2010 г.). «Растрепанный: узел сигнализации Wnt». Сотовая связь. 22 (5): 717–27. Дои:10.1016 / j.cellsig.2009.11.021. PMID 20006983.
внешняя ссылка
- растрепанные белки в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
| Этот белок -связанная статья является заглушка. Вы можете помочь Википедии расширяя это. |
