Нодуларин - Nodularin
 | |
| Имена | |
|---|---|
| Другие имена Цикло [(2S,3S,4E,6E,8S,9S) -3-амино-9-метокси-2,6,8-триметил-10-фенил-4,6-декадиеноил-D-γ-глутамил- (2Z) -2- (метиламино) -2-бутеноил- (3S) -3-метил-D-β-аспартил-L-аргинил] | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.150.290 |
| Номер ЕС |
|
| КЕГГ | |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C41ЧАС60N8О10 | |
| Молярная масса | 824.977 г · моль−1 |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Нодулярины - сильнодействующие токсины, вырабатываемые цианобактериями. Nodularia spumigena .[1] Этот водный, фотосинтетический цианобактерии образует видимые колонии, которые представляют собой цветение водорослей в солоноватых водоемах по всему миру.[2] Конец лета расцветает Nodularia spumigena являются одними из самых массовых цианобактерий в мире. Цианобактерии состоят из многих токсичных веществ, в первую очередь из микроцистины и нодулярины: эти два вида трудно дифференцировать. Между ними существует значительная гомология структуры и функции, и микроцистины были изучены более подробно. Из-за этого факты из микроцистинов часто распространяются на нодулярины.[3]
Нодуларин-R является преобладающим вариантом токсина, хотя на сегодняшний день обнаружено 10 вариантов нодулярина. Нодулярины представляют собой циклические нерибосомные пентапептиды и содержат несколько необычных не протеиногенный аминокислоты такие как N-метилдидегидроаминомасляная кислота и β-аминокислота ДОБАВИТЬ. Эти соединения являются относительно стабильными соединениями: свет, температура и микроволны мало способствуют разложению соединений.[4]
Нодулярины часто связывают с гастроэнтеритом, реакциями аллергического раздражения и заболеваниями печени.[5] Нодуларин-R известен как мощный гепатотоксин, который может нанести серьезный вред печени человека и других животных. Предел концентрации нодуляринов в питьевой воде (заимствованный из microcystins-LR) ВОЗ составляет 1,5 мкг / л.[6]
Физические свойства
Нодуларин имеет молекулярную формулу C41ЧАС60N8О10 и средняя молекулярная масса 824,963 г / моль. Соединение имеет 8 определенных стереоцентров.[7] Это твердое вещество. В метаноле нодуларин растворим в 2 мг / мл.[8] Токсины медленно разрушаются при температурах выше 104 ° F, pH меньше 1 и pH больше 9.[9] Нодулярины обычно устойчивы к разрушению при гидролизе и окислении в водных условиях.[10] Опасными продуктами разложения нодуляринов являются оксид углерода и диоксид углерода.[11]
Механизм действия
Метаболизм
Нодулярин в первую очередь нацелен на печень, хотя нодулярины также накапливаются в крови, кишечнике и почках.[12] В печени это нацеливание приводит к повреждению цитоскелета, некроз, и быстрое образование пузырей гепатоциты. Гибель клеток и быстрое образование пузырей также разрушают более тонкие кровеносные сосуды печени. Повреждение приводит к скоплению крови в печени, что может привести к увеличению веса печени на 100%. От этого геморрагического шока наступает смерть от отравления нодулярином. Это быстродействующее действие, которое происходит в течение нескольких часов после приема высокой дозы. [13]
На молекулярном уровне и более подробно нодулярин обрабатывается сложным образом, чтобы вызвать токсические эффекты. Во время пищеварения нодулярины диффундируют из тонкой кишки в печень из-за активного поглощения неспецифическим переносчиком органических анионов в транспортной системе желчных кислот. Этот переносчик экспрессируется в желудочно-кишечном тракте, почках, головном мозге и печени.[14] Попадая в печень, нодуларин ингибирует три ключевых фермента, в частности каталитические единицы серин / треониновых протеинфосфатаз: Протеиновая фосфатаза 1 (ПП-1) и Протеиновая фосфатаза 2А. (PP-2A) и протеинфосфатаза 3 (PP-3).[15] Эти ферменты действуют, удаляя фосфат из белка, подавляя функцию белка.
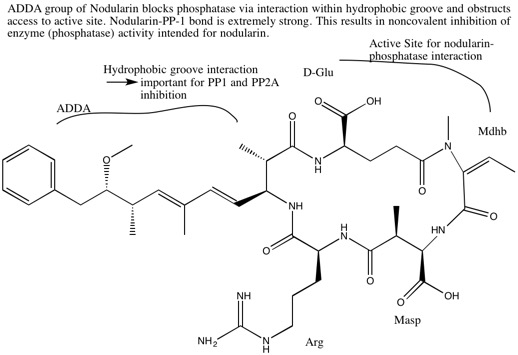
Источником токсичности является исходное нековалентное взаимодействие с участием боковой цепи ADDA (в частности, когда ADDA имеет двойную связь 6E) нодулярина и свободной D-глутамилкарбоксильной группы в циклической структуре фосфатазы. Группа ADDA блокирует активность фермента (фосфатазы), взаимодействуя с гидрофобной бороздкой и препятствуя доступу субстрата к щели активного сайта. Взаимодействия токсин-фосфатазной связи (нодуларин-PP-1, нодуларин-PP-2A) чрезвычайно сильны. Это приводит к угнетению активности фермента. Следует отметить, что нодулярины здесь отличаются от микроцистинов: нодулярины нековалентно связываются с протеинфосфатазами, тогда как микроцистины связываются ковалентно.[16]
Дальнейшее взаимодействие включает ковалентную связь по Михаэлю электрофильного α, β-ненасыщенного карбонила метилдегидроаланинового остатка на нодулярине с тиолом цистеина 273 на PP-1.[17] Хотя ковалентная связь на этапе 2 не важна для подавления активности фермента, она помогает опосредовать активность. Без этой ковалентной связи сродство нодулярина к фосфатазе снижается более чем в 10 раз.[18]Ингибирование протеинфосфатаз приводит к увеличению фосфорилирования белков цитоскелета и белков, связанных с цитоскелетом. Гиперфосфорилирование промежуточных филаментов клетки, в частности цитокератин 8 и цитокератин 18, является основной причиной белкового дисбаланса. Белковый дисбаланс стимулирует перераспределение и перестройку этих белков, что изменяет морфологию всей клетки и целостность мембраны. В частности, это перераспределение приводит к коллапсу микрофиламентов актина в цитоскелете гепатоцитов и смещению а-актинин и талин. Контакт с соседними клетками снижается, и синусоидальные капилляры теряют стабильность, что быстро приводит к внутрипеченочному кровоизлиянию и часто приводит к серьезным нарушениям функции печени или смерти.[19]
Реактивные окислительные формы
Нодулярины также участвуют в образовании реактивных окислительных форм (АФК), в частности, супероксидных и гидроксильных радикалов, которые, следовательно, вызывают окислительное повреждение ДНК через перекисное окисление липидов, белков и ДНК по неизвестному механизму.[20]
Активность по развитию опухолей
Нодулярины получили большое внимание как канцерогенный угроза, так как бактерии обладают активностью инициирования опухоли и развития опухоли. Уровень их опухолевой активности намного выше, чем у микроцистинов; Полагают, что это связано с меньшей кольцевой структурой нодуляринов, которая позволяет им легче проникать в гепатоциты. Эта активность, способствующая развитию опухоли, достигается за счет индуцированной экспрессии генов TNF-альфа и протоонкогены, хотя точный механизм неизвестен. Кроме того, продукты гена-супрессора опухоли ретинобластома и p53 инактивируются фосфорилированием (описано выше). Если опухолевый супрессор инактивирован, вероятно, произойдет рост опухоли.
С точки зрения общественного здравоохранения и эпидемиологии, существует корреляция первичного рака печени в районах Китая с нодуляринами и микроцистинами в воде прудов, канав, рек и неглубоких колодцев.[21]
Эксперименты на крысах, где животные подвергались воздействию нелетальных доз нодулярина, показали, что он является канцерогеном, вызывая опухоль и способствуя развитию опухоли. Это достигается ингибированием PP-1 и PP-2A. Нодулярины участвуют в экспрессии онкогенов и генов-супрессоров опухолей. фактор некроза опухоли альфа, с-июн, июн-B, июн-D, c-fos, фос-Б и фра-1 экспрессия гена. Чтобы лучше понять канцерогенность нодуляринов, необходимо больше данных.[22]
Медицинские аспекты
Симптомы
Симптомы воздействия включают образование волдырей вокруг рта, боль в горле, головную боль, боль в животе, тошноту и рвоту, диарею, сухой кашель и пневмонию.[23] Если с течением времени принимать нелетальные дозы, повреждение печени может проявляться в виде хронических симптомов заболевания печени. Эти симптомы включают желтуху, быстрое кровотечение, вздутие живота, психическую дезориентацию или спутанность сознания, сонливость или кому.
Нодулярины обычно поражают водные организмы, такие как рыбы и растения. Однако в некоторых случаях нодулярины упоминались в случаях смерти собак, овец и людей (dawson et al.). Отравление нодулярином не очень распространено у людей: очень мало случаев было зарегистрировано и подтверждено как отравление нодулярином.
Контакт
Нодулярины могут вызывать симптомы при приеме внутрь, вдыхании и чрескожном контакте. Методы воздействия включают аспирацию бактерий, попадание на кожу, проглатывание и / или вдыхание при занятиях любыми видами спорта, профессиональной рыбалке или бытовом использовании, например при принятии душа.[24] Обычные процессы очистки воды не позволяют полностью удалить нодулярины и микроцистины из сырой воды.[25] Нодулярины также могут попадать в организм через загрязненную питьевую воду или морепродукты. В частности, нодулярины были обнаружены в относительно высоких концентрациях в балтийских моллюсках, голубых мидиях, камбалах, треске и спине трехколюшки и относительно более низкие концентрации в сельди и лососе.[26] Кроме того, было зарегистрировано, что нодулярины попадают в организм человека во время диализа загрязненной воды.[27] Дующий ветер может распространять вещества от цветков цианобактерий на расстояние до 10 км, увеличивая зону потенциального воздействия.
Токсикология
В настоящее время концентрация токсина обычно определяется как масса нодуляринов внутри клеток и растворенных в определенном объеме воды. Предварительная рекомендация по безопасности нодуляринов составляет 1 микрограмм / л. Оральная токсичность LD оценивается по микроцистинам и составляет 5 мг / кг. Токсичность нодуляринов, основанная на LD и вдыхаемой токсичности, сопоставима с токсичностью химических фосфорорганических нервно-паралитических агентов.[28]
Уход
Поскольку отравление нодулярином встречается редко и по-прежнему трудно окончательно отличить отравление от отравления нодулярином, стандартного метода лечения не существует. Кроме того, поскольку нодулярины и микроцистины вызывают быстрое и необратимое повреждение печени, терапия практически не имеет ценности. Хроническое воздействие низких концентраций в равной степени вредно для печени.[29] Во избежание воздействия следует соблюдать строгие меры предосторожности.[30]
Исследования показали, что лечение мелатонином (доза: 15 мг / кг массы тела) во время и после него имеет защитные функции от окислительного стресса / повреждений, вызванных нодуляринами. (источник 121 из (# 1).
Безопасность
В группу риска по отравлению нодулярином входят люди, животные и растения, живущие в радиусе 10 км от побережья и озер. Кроме того, повышенному риску подвержены люди 50 лет и старше.
Рекомендации по безопасности могут быть реализованы для снижения риска, в частности, включая стандарты чистоты питьевой воды. Доказана эффективность микроорганизмов в биоразложении и удалении нодуляринов, что может быть полезно для борьбы с цветением цианобактерий в системах водоснабжения. Защитная одежда и физическое избегание участков видимого цветения цианобактерий помогают снизить вероятность случайного воздействия.
Синтез
Синтез нодуляринов в настоящее время изучен недостаточно. Биосинтез нодуляринов нерибосомный. Синтез осуществляется мультиферментными комплексами, такими как пептидные синтетазы, полипептидные синтазы и адаптирующие ферменты.[31]
История
Первым задокументированным случаем отравления нодулярином было животное (овца) в Австралии в 1878 году. Химическая структура нодулярина-R была идентифицирована в 1988 году. В Каруару, Бразилия, в 1996 году диализные растворы из местного резервуара были загрязнены сине-зелеными водорослями. . Пациенты, получавшие гемодиализ, подвергались воздействию этих растворов, у 100 из 131 развилась острая печеночная недостаточность и 52 из 131 пациента умерли после развития токсического гепатита.[32]
Смотрите также
Рекомендации
- ^ Сивонен К., Кононен К., Кармайкл В.В., Далем А.М., Райнхарт К.Л., Кивиранта Дж., Ниемела С.И. (1989). «Распространение гепатотоксической цианобактерии Nodularia spumigena в Балтийском море и структура токсина». Appl. Environ. Микробиол. 55 (8): 1990–5. ЧВК 202992. PMID 2506812.
- ^ Чен, Юнь; Шен, Даньфэн; Фанг, Даньцзюнь (21 октября 2013 г.). «Нодулярины в отравлении». Clinica Chimica Acta. 425: 18–29. Дои:10.1016 / j.cca.2013.07.005. PMID 23872223.
- ^ Чен, Юнь; Шен, Даньфэн; Фанг, Даньцзюнь (21 октября 2013 г.). «Нодулярины в отравлении». Clinica Chimica Acta. 425: 18–29. Дои:10.1016 / j.cca.2013.07.005. PMID 23872223.
- ^ Чен, Юнь; Шен, Даньфэн; Фанг, Даньцзюнь (21 октября 2013 г.). «Нодулярины в отравлении». Clinica Chimica Acta. 425: 18–29. Дои:10.1016 / j.cca.2013.07.005. PMID 23872223.
- ^ Доусон, Р. М. (1998). «Токсикология микроцистинов». Токсикон. 36 (7): 953–962. Дои:10.1016 / S0041-0101 (97) 00102-5. PMID 9690788.
- ^ «Нодуларин». Вещества, представляющие биологический интерес, бактериальный токсин, природный токсин. SelfDecode. Получено 30 апреля 2017.
- ^ «Нодуларин». ChemSpider. Королевское химическое общество.
- ^ «Нодуларин». Сигма-Олдрич. Сигма-Олдрич. Получено 2017-04-30.
- ^ «Нодуларин». Вещества, представляющие биологический интерес, бактериальный токсин, природный токсин. SelfDecode. Получено 30 апреля 2017.
- ^ «Нодуларин». Вещества, представляющие биологический интерес, бактериальный токсин, природный токсин. SelfDecode. Получено 30 апреля 2017.
- ^ «Нодуларин». База данных PubChem Open Chemistry. Национальный институт здоровья.
- ^ Чен, Юнь; Шен, Даньфэн; Фанг, Даньцзюнь (21 октября 2013 г.). «Нодулярины в отравлении». Clinica Chimica Acta. 425: 18–29. Дои:10.1016 / j.cca.2013.07.005. PMID 23872223.
- ^ Доусон, Р. М. (1998). «Токсикология микроцистинов». Токсикон. 36 (7): 953–962. Дои:10.1016 / S0041-0101 (97) 00102-5. PMID 9690788.
- ^ Зегура, Бояна; Стразер, Аля; Филипич, Метка (январь – апрель 2011 г.). «Генотоксичность и потенциальная канцерогенность токсинов цианобактерий - обзор». Обзоры в Mutation Research. 727 (1–2): 16–41. Дои:10.1016 / j.mrrev.2011.01.002. PMID 21277993.
- ^ Охта, Т; Sueoka, E; Иида, N; Комори, А; Suganuma, M; Нишиваки, Р. Татэмацу, М; Kim, S.J .; Кармайкл, У. В .; Фуджики, Х (1994). «Нодуларин, мощный ингибитор протеинфосфатаз 1 и 2A, представляет собой новый канцероген в окружающей среде в печени самцов крыс F344». Исследования рака. 54 (24): 6402–6. PMID 7527297.
- ^ Чен, Юнь; Шен, Даньфэн; Фанг, Даньцзюнь (21 октября 2013 г.). «Нодулярины в отравлении». Clinica Chimica Acta. 425: 18–29. Дои:10.1016 / j.cca.2013.07.005. PMID 23872223.
- ^ Чен, Юнь; Шен, Даньфэн; Фанг, Даньцзюнь (21 октября 2013 г.). «Нодулярины в отравлении». Clinica Chimica Acta. 425: 18–29. Дои:10.1016 / j.cca.2013.07.005. PMID 23872223.
- ^ Доусон, Р. М. (1998). «Токсикология микроцистинов». Токсикон. 36 (7): 953–962. Дои:10.1016 / S0041-0101 (97) 00102-5. PMID 9690788.
- ^ Чен, Юнь; Шен, Даньфэн; Фанг, Даньцзюнь (21 октября 2013 г.). «Нодулярины в отравлении». Clinica Chimica Acta. 425: 18–29. Дои:10.1016 / j.cca.2013.07.005. PMID 23872223.
- ^ Чен, Юнь; Шен, Даньфэн; Фанг, Даньцзюнь (21 октября 2013 г.). «Нодулярины в отравлении». Clinica Chimica Acta. 425: 18–29. Дои:10.1016 / j.cca.2013.07.005. PMID 23872223.
- ^ Доусон, Р. М. (1998). «Токсикология микроцистинов». Токсикон. 36 (7): 953–962. Дои:10.1016 / S0041-0101 (97) 00102-5. PMID 9690788.
- ^ Зегура, Бояна; Стразер, Аля; Филипич, Метка (январь – апрель 2011 г.). «Генотоксичность и потенциальная канцерогенность токсинов цианобактерий - обзор». Обзоры в Mutation Research. 727 (1–2): 16–41. Дои:10.1016 / j.mrrev.2011.01.002. PMID 21277993.
- ^ «Как люди подвергаются воздействию цианобактерий и цианотоксинов?». Данные о политике в отношении пищевых веществ - воздействие на здоровье и экологию. EPA.gov. 2014-06-19.
- ^ Чен, Юнь; Шен, Даньфэн; Фанг, Даньцзюнь (21 октября 2013 г.). «Нодулярины в отравлении». Clinica Chimica Acta. 425: 18–29. Дои:10.1016 / j.cca.2013.07.005. PMID 23872223.
- ^ Доусон, Р. М. (1998). «Токсикология микроцистинов». Токсикон. 36 (7): 953–962. Дои:10.1016 / S0041-0101 (97) 00102-5. PMID 9690788.
- ^ Чен, Юнь; Шен, Даньфэн; Фанг, Даньцзюнь (21 октября 2013 г.). «Нодулярины в отравлении». Clinica Chimica Acta. 425: 18–29. Дои:10.1016 / j.cca.2013.07.005. PMID 23872223.
- ^ Доусон, Р. М. (1998). «Токсикология микроцистинов». Токсикон. 36 (7): 953–962. Дои:10.1016 / S0041-0101 (97) 00102-5. PMID 9690788.
- ^ Доусон, Р. М. (1998). «Токсикология микроцистинов». Токсикон. 36 (7): 953–962. Дои:10.1016 / S0041-0101 (97) 00102-5. PMID 9690788.
- ^ Зегура, Бояна; Стразер, Аля; Филипич, Метка (январь – апрель 2011 г.). «Генотоксичность и потенциальная канцерогенность токсинов цианобактерий - обзор». Обзоры в Mutation Research. 727 (1–2): 16–41. Дои:10.1016 / j.mrrev.2011.01.002. PMID 21277993.
- ^ Доусон, Р. М. (1998). «Токсикология микроцистинов». Токсикон. 36 (7): 953–962. Дои:10.1016 / S0041-0101 (97) 00102-5. PMID 9690788.
- ^ Зегура, Бояна; Стразер, Аля; Филипич, Метка (январь – апрель 2011 г.). «Генотоксичность и потенциальная канцерогенность токсинов цианобактерий - обзор». Обзоры в Mutation Research. 727 (1–2): 16–41. Дои:10.1016 / j.mrrev.2011.01.002. PMID 21277993.
- ^ Доусон, Р. М. (1998). «Токсикология микроцистинов». Токсикон. 36 (7): 953–962. Дои:10.1016 / S0041-0101 (97) 00102-5. PMID 9690788.
