PMDTA - PMDTA
 | |
 | |
 | |
| Идентификаторы | |
|---|---|
3D модель (JSmol ) | |
| 1741396 | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.019.275 |
| Номер ЕС |
|
| 27747 | |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 2734 |
| |
| |
| Свойства | |
| C9ЧАС23N3 | |
| Молярная масса | 173.304 г · моль−1 |
| Внешность | Бесцветная жидкость |
| Запах | Рыбный, аммиачный |
| Плотность | 830 мг мл−1 |
| Температура плавления | -20 ° С (-4 ° F, 253 К) |
| Точка кипения | 198 ° С (388 ° F, 471 К) |
| Давление газа | 31 Па (при 20 ° C) |
| 1.442 | |
| Опасности | |
| Паспорт безопасности | sigmaaldrich.com |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Опасность |
| H302, H311, H314 | |
| P280, P305 + 351 + 338, P310 | |
| точка возгорания | 53 ° С (127 ° F, 326 К) |
| 155 ° С (311 ° F, 428 К) | |
| Пределы взрываемости | 1.1–5.6% |
| Смертельная доза или концентрация (LD, LC): | |
LD50 (средняя доза ) |
|
| Родственные соединения | |
Родственные амины | |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
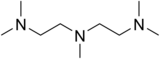
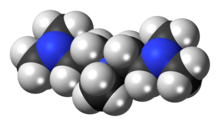
PMDTA (N,N,N ′,N ′ ′,N ′ ′-пентаметилдиэтилентриамин) представляет собой органическое соединение с формулой [(CH3)2NCH2CH2]2NCH3. PMDTA - это простой, громоздкий и гибкий, тридентатный лиганд это используется в литийорганическая химия. Это бесцветная жидкость, хотя нечистые образцы кажутся желтоватыми.
Синтез
PMDTA готовится из диэтилентриамин посредством Реакция Эшвайлера-Кларка, предполагающие использование формальдегида и Муравьиная кислота.[1]
- [ЧАС2N (CH2)2]2NH + 5 CH2O + 5 HCO2H → [Me2NCH2CH2]2NMe + 5 CO2 + 5 часов2О
Сравнение с диэтилентриамином
В отличие от диэтилентриамина, все три амина в PMDTA являются третичными. И PMDTA, и диэтилентриамин являются тридентатными лигандами, которые образуют два пятичленных хелатных кольца. Σ-донорные свойства аминогрупп диэтилентриамина выше, чем у PMDTA в комплексах меди (II).[2] Оба лиганда могут координировать комплексы металлов в расположении, в котором три азотных центра копланарны или взаимно расположены. СНГ.
Литийорганические соединения и PMDTA
PMDTA используется для изменения реактивности литийорганические соединения, которые дезагрегируют в присутствии оснований Льюиса для повышения их реакционной способности.[3] Обычно дитретичный амин TMEDA используется в этих приложениях; он связывается с литиевым центром как бидентатный лиганд. PMDTA ведет себя аналогично, но, поскольку он тридентатный, он сильнее связывается с литием. В отличие от TMEDA, PMDTA образует мономерные комплексы с литийорганическими соединениями. Оба амина влияют на региохимию металлирования.[3][4]
В PMDTA /п-BuLi, связи Li-C сильно поляризованы, что увеличивает основность бутильной группы.[5]
Влияние PMDTA на анилид лития иллюстрирует комплексообразующую способность PMDTA. Комплекс, [{PhN (H) Li}3· 2PMDTA], трехъядерный, содержащий приблизительно коллинеарный Li+ центры трех-, четырех- и пятикоординатные. Центральный трехкоординатный атом лития не связан с PMDTA. Один из концевых центров Li является псевдотетраэдром в N4 координационная сфера. Другой концевой атом лития является пятикоординатным и связывается с двумя анилино-N центрами и PMDTA.[6]
Переходные металлы и комплексы алюминия
PMDTA часто образует пятикоординатные комплексы из-за стерического объема метильных групп. PMDTA стабилизирует необычные катионы. Первое катионное производное алана, [H2Al (PMDTA)]+[AlH4]− был приготовлен путем обработки H3AlNMe3 с PMDTA.[5]
использованная литература
- ^ Марксер, А .; Мишер, К. (1951). "Über die stufenweise Quaternisierung von aliphatischen Polyaminen. Neue Verbindungen mit ganglienblockierender Wirkung". Helvetica Chimica Acta. 34 (3): 924–931. Дои:10.1002 / hlca.19510340327.
- ^ Angelici, R.J .; Эллисон, Дж. У. (1971). "Константы стабильности аминокислотной координации замещенными диэтилентриаминовыми комплексами меди (II) и кинетика гидролиза сложного эфира аминокислот". Неорганическая химия. 10 (10): 2238–2243. Дои:10.1021 / ic50104a030.
- ^ а б Strohmann, C .; Гесснер, В. Х. (2007). "Из алкиллитиевого агрегата (nBuLi)2· PMDTA2 к литированному ПМДТА ». Angewandte Chemie International Edition. 46 (24): 4566–4569. Дои:10.1002 / anie.200605105.
- ^ Френкель, Г. (2002). «ПМДТА». Энциклопедия реагентов для органического синтеза. Вайнхайм: Wiley-VCH. С. 806–813. Дои:10.1002 / 047084289X.rp028. ISBN 0-471-93623-5.
- ^ а б Эльшенбройх, К. (2006). Металлоорганические соединения. Вайнхайм: Wiley-VCH. С. 45–46. ISBN 978-3-527-29390-2.
- ^ Barr, D .; Clegg, W .; Cowton, L .; Horsburgh, L .; Mackenzie, F.M .; Малви, Р. (1995). «Комплекс анилида лития с pmdeta: ожидание простого мономера, но на самом деле странный трехъядерный состав, сочетающий трех-, четырех- и пятикоординированный литий». Журнал химического общества, химические коммуникации. 1995 (8): 891–892. Дои:10.1039 / C39950000891.
