Хирургическая сетка - Surgical mesh

Хирургическая сетка представляет собой неплотно сплетенный лист, который используется в качестве постоянной или временной опоры для органы и другие ткани в течение хирургия. Хирургическая сетка создается как из неорганический и биологические материалы и используется в различных хирургических вмешательствах. Хотя герниопластика хирургия - наиболее распространенное применение, ее также можно использовать для реконструктивный работа, например, в пролапс тазовых органов.[1]
Постоянные сетки остаются в теле, а временные со временем растворяются. Например, Тестовая сетка TIGR Matrix В 2012 году было показано, что он полностью растворяется после трех лет научных исследований на овцах.[2] Некоторые типы сеток сочетают в себе постоянные и временные сетки, такие как Vipro, который включает в себя как повторно рассасывающийся виприл, сделанный из полигликолевая кислота, и пролен, не реабсорбируемый полипропилен.[3]
Данные о механическом и биологическом поведении сетки in vivo не всегда может происходить одновременно в организме человека из-за тестирования на других организмах. Большинство опубликованных отчетов экспериментируют на мышах, таким образом создавая вероятность возможных различий при введении в человеческое тело. Кроме того, в большинстве опубликованных отчетов об исследованиях упоминаются сетки, которые в настоящее время удалены с рынка медицинских устройств из-за осложнений после операции. Кроме того, отсутствие утвержденных FDA нормативных протоколов и универсальных стандартных операционных процедур приводит к использованию множества различных методов тестирования от исследователя к исследователю. Эксперименты могут привести к разным результатам для некоторых сеток.
Медицинское использование
Основная функция хирургической сетки - временно или навсегда поддерживать выпавшие органы. Чаще всего он используется при хирургии грыжи в брюшной полости, когда какой-либо орган выступает через мышцы живота. Хирургическая сетка также может использоваться для реконструкции стенок таза или влагалища у женщин и применяется в качестве ориентира для роста поврежденных тканей. В идеале эти имплантаты должны быть достаточно прочными, чтобы выдерживать механические нагрузки и воздействия какой бы области тела они ни становились.
Хирургия грыжи
Хирургия грыжи - одно из наиболее распространенных применений хирургической сетки в настоящее время. Грыжи возникают, когда органы или жировая ткань выпячиваются через отверстия или ослабленные участки мышц, обычно в брюшной стенке. Хирургическая сетка имплантируется, чтобы усилить восстановление тканей и свести к минимуму вероятность рецидивов. Операция может быть выполнена лапароскопической (внутренне) или открытой с использованием различных материалов, доступных для протезирования.[4] Полипропилен (ПП) - это наиболее часто используемый тип сетки, хотя после имплантации он может быть неудобным для пациента. Другой тип, который меньше используется в хирургии грыж, - это полиэтилентерефталат (ПЭТ), который сталкивается с осложнениями в том, что он легко разрушается после нескольких лет имплантации, стирая последствия операции. Политетрафторэтилен (PTFE ) также используется, но изготавливается в виде фольги и с трудом интегрируется в окружающие ткани, поэтому теряет устойчивость.[5]
Тазовая хирургия
Подобно хирургии грыжи, синтетические сетки могут использоваться также при пролапсе органов в области таза. Выпадение тазовых органов происходит у 50% женщин старше 50 лет, у которых в анамнезе были один или несколько родов через естественные родовые пути на протяжении всей жизни.[6] Операция на сетке может выполняться в различных областях тазовой области, таких как цистоцеле, ректоцеле, свод влагалища или матка. Наиболее часто используемым материалом, как и в хирургии грыжи, является полипропилен, который, как считается, имеет приемлемую биосовместимость в данном регионе. Он вызывает легкую воспалительную реакцию, но имеет тенденцию прилипать к внутренним органам.[6]
Стенка влагалища состоит из трех слоев: слизистой оболочки, мышечной оболочки, адвентиции. Когда происходит выпадение, гладкие мышечные волокна нарушаются. Также было замечено, что пролапс у женщин увеличивает жесткость таза, особенно у женщин в постменопаузе.[6] Хирургическая сетка, используемая при реконструкции таза, должна противодействовать этой жесткости, но если модуль упругости слишком высок, она не будет в достаточной степени поддерживать органы. Напротив, если сетка слишком жесткая, ткань разрушится, а воспалительные реакции вызовут послеоперационные осложнения. После имплантации полипропиленовая сетка иногда имеет микротрещины, отслаивание волокон и фиброз.[7]
Кроме того, сетка обладает достаточной прочностью, чтобы противостоять основным воздействиям и поведению тканей в физиологических условиях, особенно во время регенерации тканей через саму сетку.[6] Эта область подвергается различным нагрузкам, исходящим от содержимого брюшной полости, давлению мышц брюшной полости / диафрагмы и половых органов, а также дыхательным воздействиям. У средней женщины репродуктивного возраста таз должен выдерживать нагрузки 20 Н в положении лежа на спине, 25-35 Н в положении стоя и 90-130 Н во время кашля.[6] Любая сетка, которая имплантируется в область таза, должна быть достаточно прочной, чтобы выдерживать эти нагрузки.
Регулирование
В 2018 году Соединенное Королевство временно приостановило использование вагинальных сетчатых имплантатов для лечения недержания мочи в ожидании дальнейшего расследования рисков и имеющихся мер безопасности.[8]
В США FDA реклассифицировало трансвагинальную хирургическую сетку как «класс III» (высокий риск) в 2016 г.[9] и в конце 2018 года поданы обязательные заявки на одобрение premark для сетки, предназначенной для трансвагинального лечения пролапса тазовых органов, дальнейшее расследование запланировано на 2019 год.[10] Затем 16 апреля 2019 года FDA приказало всем производителям трансвагинальных хирургических сеток немедленно прекратить их продажу и распространение.[9]
Биосовместимость

Имплантация сетки естественным образом вызывает воспалительную реакцию на вставленную сетку, но биосовместимость варьируется от того, насколько легко она интегрируется, до того, насколько серьезна реакция на инородное тело. Минимальная реакция включает образование фиброза вокруг протеза (как при образовании рубцовой ткани); этот ответ генерируется с наилучшей формой биосовместимости. Физическая реакция вызывает острую воспалительную реакцию, которая включает образование гигантских клеток, а затем и гранулем, что означает, что ткань достаточно хорошо «переносит» сетку. Наконец, химический ответ делает возможным серьезную воспалительную реакцию во время попытки интеграции ткани в сетку, включая пролиферацию фибробластных клеток.[6] В конечном итоге цель создания хирургической сетки - создать сетку с минимальным in vivo реакция для максимального комфорта пациента, предотвращения инфекции и обеспечения чистой интеграции в организм для восстановления тканей.
На биосовместимость сеток влияет ряд факторов. Пористость сетки - это отношение поры к общей площади, она играет роль в развитии бактериальной инфекции или регенерации гладкой ткани в зависимости от размера пор. Поры размером менее 10 микрометров восприимчивы к инфекции, потому что бактерии могут проникать и размножаться, а макрофаги и нейтрофилы слишком велики, чтобы пройти через них, и не могут способствовать их устранению. При размере пор, превышающем 75 микрометров, фибробласты, кровеносные сосуды и коллагеновые волокна разрешаются как часть регенерации тканей. Хотя нет единого мнения о наилучшем размере пор, можно сделать вывод, что более крупные поры лучше для развития ткани и интеграции. in vivo.[6]
Зная это, текущая проблема с множеством сеток, используемых во всех типах хирургических операций, заключается в том, что они недостаточно биосовместимы. ПП доказал свою эффективность в качестве сетки для коррекции выпавших органов, но может вызвать у пациента серьезный дискомфорт из-за своего высокого модуля упругости. Это делает протез жестким и приводит к более выраженной воспалительной реакции, что затрудняет интеграцию в организм с прорастанием тканей. Как упоминалось ранее, ПЭТ слишком легко разлагается. in vivo и ткани с трудом интегрируются с ПТФЭ. По этим причинам исследователи начинают искать различные типы хирургической сетки, которые могут подходить для биологической среды и обеспечивать больший комфорт при поддержке выпавших органов.[5]
ПВДФ (нановолоконная сетка)
Один конкретный тип сетки, который изучается, - это поливинилиденфторид (ПВДФ) или нановолоконная сетка, которая, как было обнаружено, более устойчива к гидролизу и разрушению, в отличие от ПЭТ, и не увеличивает ее жесткость с возрастом, в отличие от полипропилена. Он проходит испытания как при грыжах, так и при хирургии стенок таза / влагалища и производится путем размещения волокон слой за слоем, в то время как полипропилен изготавливается методом плетения. Это придает нановолоконной сетке тяжелую, но при этом малопористую структуру, а также увеличивает жесткость и порог напряжения по сравнению с полипропиленом. Это подтверждается основой HSP 70 - индикатора клеточного стресса и защитника формирования клеток от повреждений, который полезен для протеза и формирования тканей, - который отслеживался и наблюдался в большем присутствии PVDF.[5] Наблюдения за нановолоконной сеткой in vitro предоставили доказательства миграции и пролиферации клеток на сетке. Отмечен успешный рост клеток с длинными веретенообразными формами и четкими границами.[11]
Существенным преимуществом использования нановолоконной сетки является то, что она может нести гораздо больше стволовых клеток, чем традиционная полипропиленовая сетка, что может улучшить методы клеточной терапии пролапса и регенерации органов малого таза. Еще одним важным преимуществом PVDF является формирование капилляров через 12 недель, что важно для заживления ран. Чем быстрее происходит неоваскуляризация, тем быстрее ткань может быть восстановлена и регенерирована, что снижает вероятность страдания от обнажения или выдавливания сетки.[11]
Некоторые усовершенствования PVDF также необходимо внести, прежде чем его можно будет использовать в хирургии человека. Хотя модуль упругости выше, чем у полипропилена, результирующее растяжение при идентичном напряжении намного меньше, что может вызвать такие осложнения, как дегенерация тканей и потеря механической прочности. Нанофиброзная сетка в настоящее время также способствует большей реакции на инородное тело и воспалительной реакции, что является несовместимым с целями биосовместимости сетки.[11] По этим причинам PVDF все еще рассматривается и экспериментируется с телесными имплантатами.
Снижение воспалительного ответа с помощью МСК
Воспалительные реакции на введение сетки способствуют образованию ткани вокруг волокон сетки и пролиферации фибробластов, полиморфонуклеоцитов и макрофагов, которые способствуют интеграции сетки. Неспособность устранить воспалительные реакции может привести к реакциям на инородное тело и окончательной инкапсуляции имплантата, которая сводит на нет любую функциональную цель, которой имплант должен был служить. Известно, что мезенхимальные стволовые клетки (МСК) уменьшают воспалительные реакции, которые в сочетании с хирургической сеткой могут предотвратить их неконтролируемые и слишком трудные приручения. МСК в сочетании с хирургическими сетками могут использоваться как готовые продукты и увеличивать поляризацию макрофагов как в условиях in vivo, так и in vitro. Это может стимулировать противовоспалительную реакцию и регулировать воспалительную реакцию, связанную с имплантацией сетки.[12]
Антимикробные грыжевые сетки
Наряду с эрозией сетки, миграцией сетки и энтерокутенозной фистулой, инфекции области хирургического вмешательства (SSI), связанные с сеткой, остаются серьезной проблемой здравоохранения.[13] Ежегодно инфицировано около 60 000 паховых и вентральных грыж, примерно столько же в Европе.[13] CDC различает поверхностные SSI; которые затрагивают только кожу и подкожную клетчатку, и глубокие ИОХВ, когда инфекция может оседать на имплантате, что требует более сложных протоколов лечения.[14]
Патогенез загрязнения, связанного с сеткой, в основном связан с кожей или слизистой оболочкой пациента во время первичного разреза и клинической практики. Установлено, что введение медицинских устройств увеличивает восприимчивость к прилипшим бактериям от 10 000 до 100 000 раз.[15] В случае грыжевых операций от одной трети до двух третей имплантированной сетки будут загрязнены в месте введения, хотя только небольшое количество из них вызовет инфекцию. Многие факторы влияют на вероятность инфицирования сетчатого материала, среди которых наиболее важны тип хирургической процедуры и местоположение.[16] Например, вероятность инфицирования составляет 2–4% при открытой пластике паховой грыжи, но достигает 10% при пластике послеоперационной грыжи.[17] При лапароскопии самый низкий уровень инфицирования, который обычно колеблется от 1% до 0,1%.[17] Другими факторами, влияющими на вероятность заражения, являются кривая обучения хирурга, поскольку менее опытному хирургу может потребоваться больше времени для выполнения операции и, таким образом, увеличится время обнажения разреза. Кроме того, тип сетки с широким выбором доступных сегодня протезов можно было бы различить на основе материала и состава, конструкции нити, впитываемости и веса. Демографические данные пациента также влияют на вероятность возникновения инфекции; к ним относятся курение, диабет, ослабленный иммунитет и ожирение.
Прогностические факторы для раннего и позднего развития инфекций в области хирургического вмешательства включают воспаление, лихорадку, очаговую болезненность, эритему, отек с выделением гноя, покраснение, жар или боль.[18] Затем это будет оценено с помощью КТ или МРТ с последующей аспирацией жидкости и посевом. Виды стафилококков, а точнее S. aureus и S. epidermidis составляют примерно 90% инфекций с преобладающим присутствием метикулинорезистентности S. aureus (MRSA).[19] Грамотрицательные виды, такие как Pseudomonas sp., Энтеробактерии также часто встречаются. С многовидовыми биопленками также часто встречаются. Если инфекция оседает на сетке, введение антибиотиков обычно неэффективно из-за барьера гематоэнцефалической сетки, и удаление сетки требуется при более чем 40% глубоких ИОХВ.[20]
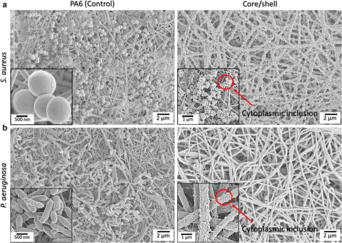
С точки зрения материаловедения сетка может играть пассивную роль в антибактериальной защите благодаря своей архитектуре или активную роль, сочетая терапевтические средства с составом сетки. Например, было обнаружено, что монофиламентные сетки в два раза реже прилипают к бактериям, чем мультифиламентные сетки.[22] В качестве системы доставки лекарств грыжевую сетку можно использовать для доставки антибиотиков,[23] антисептики,[24] противомикробные препараты,[21] антимикробные пептиды[25] или наночастицы.[26] Для реализации интеграции таких веществ могут использоваться различные методы, включая погружение / вымачивание, физическое покрытие, химическую функционализацию поверхности и электроспиннинг.
Противомикробные сетки для лечения грыж, одобренные FDA
- MycroMesh и DualMesh Plus от GORE [27]
- Хирургический трансплантат XenMatrix от BD [28]
- Пластырь вентриональной грыжи от BD [29]
Смотрите также
Рекомендации
- ^ «Информация о хирургической сетке при пролапсе тазовых органов и стрессовом недержании мочи». Связь с безопасностью медицинского оборудования. Управление по контролю за продуктами и лекарствами. 20 ноября 2012 г.. Получено 2 марта 2013.
- ^ Hjort, H .; Mathisen, T .; Alves, A .; Clermont, G .; Бутран, Дж. П. (2012). «Трехлетние результаты доклинического исследования имплантации долговременной рассасывающейся хирургической сетки с механическими характеристиками, зависящими от времени». Грыжа. 16 (2): 191–197. Дои:10.1007 / s10029-011-0885-у. ЧВК 3895198. PMID 21972049.
Через 36 месяцев тестовая сетка полностью рассосалась.
- ^ «Випро 2 сетка». Руководство по продукту Ethicon. Этикон. Получено 2 марта 2013.
- ^ Neumayer, Leigh; Джобби-Хердер, Анита; Йонассон, Ольга; Фитцгиббонс, Роберт-младший; Данлоп, Дороти; Гиббс, Джеймс; Реда, Доменик; Хендерсон, Уильям (2004-04-29). «Открытая сетка против лапароскопической пластики паховой грыжи сеткой». Медицинский журнал Новой Англии. 350 (18): 1819–1827. Дои:10.1056 / NEJMoa040093. ISSN 0028-4793. PMID 15107485.
- ^ а б c Браун, Брайан Н .; Лондоно, Рикардо; Тотти, Стивен; Чжан, Ли; Кукла, Кэтрин А .; Вольф, Мэтью Т .; Дейли, Керри А .; Рейнг, Джанет Э .; Бадилак, Стивен Ф. (2012-03-01). «Фенотип макрофагов как предиктор конструктивного ремоделирования после имплантации биологически полученных хирургических сетчатых материалов». Acta Biomaterialia. 8 (3): 978–987. Дои:10.1016 / j.actbio.2011.11.031. ЧВК 4325370. PMID 22166681.
- ^ а б c d е ж грамм Todros, S .; Паван, П. Г .; Натали, А. Н. (2016-03-01). «Биомеханические свойства синтетических хирургических сеток для лечения пролапса таза». Журнал механического поведения биомедицинских материалов. 55: 271–285. Дои:10.1016 / j.jmbbm.2015.10.024. PMID 26615384.
- ^ Азади, Али; Patnaik, Sourav S .; Jasinski, Jacek B .; Фрэнсис, Шон Л .; Лэй, Чжэньминь; Ляо, Цзюнь; Девено, Николетт Э .; Остергард, Дональд Р. (май 2015 г.). «Морфологическая оценка постимплантированной моноволоконной полипропиленовой сетки с использованием новой техники с количественной оценкой сканирующей электронной микроскопии». Surgical Technology International. 26: 169–173. ISSN 1090-3941. PMID 26055006.
- ^ «Правительство соглашается временно запретить имплантаты вагинальной сетки для женщин с недержанием мочи». Независимый. 2018-07-10. Получено 2018-12-09.
- ^ а б «FDA заказывает трансвагинальную хирургическую сетку, снятую с рынка». Рейтер. 16 апреля 2019 г.,. Получено 17 апреля, 2019.
- ^ Здравоохранение, Центр приборов и радиологии. «Урогинекологические хирургические сетчатые имплантаты». www.fda.gov. Получено 2018-12-09.
- ^ а б c Дин, Цзин; Дэн, Моу; Сун, Сяо-чен; Чен, Чун; Лай, Куй-лин; Ван, Го-шуай; Юань, Ю-ю; Сюй, Дао; Чжу, Лань (2016-08-01). «Нанофиброзная биомиметическая сетка может быть использована для реконструктивной хирургии таза: рандомизированное исследование». Журнал механического поведения биомедицинских материалов. 61: 26–35. Дои:10.1016 / j.jmbbm.2016.01.003. PMID 26820994.
- ^ Бласкес, Ребека; Санчес-Маргалло, Франсиско Мигель; Альварес, Вероника; Усон, Алехандра; Касадо, Хавьер Г. (01.02.2016). «Хирургические сетки, покрытые мезенхимальными стволовыми клетками, обеспечивают противовоспалительную среду за счет поляризации макрофагов M2». Acta Biomaterialia. 31: 221–230. Дои:10.1016 / j.actbio.2015.11.057. PMID 26654766.
- ^ а б Guillaume, O .; Pérez-Tanoira, R .; Фортельный, Р .; Redl, H .; Мориарти, Т. Ф .; Richards, R.G .; Eglin, D .; Петтер Пухнер, А. (01.06.2018). «Инфекции, связанные с сеткой при грыжах брюшной стенки: являются ли антимикробные биоматериалы долгожданным решением?». Биоматериалы. 167: 15–31. Дои:10.1016 / j.biomaterials.2018.03.017. ISSN 0142-9612.
- ^ Центры по контролю и профилактике заболеваний. Проект руководства по профилактике инфекций в области хирургического вмешательства, 1998 г. 63 Fed Reg 167-33, 192 (17 июня 1998 г.).
- ^ Циммерли, Вернер (01.12.2006). «Инфекции, связанные с протезированием суставов». Передовая практика и исследования в клинической ревматологии. Инфекция и опорно-двигательный аппарат. 20 (6): 1045–1063. Дои:10.1016 / j.berh.2006.08.003. ISSN 1521-6942.
- ^ Лангбах, Odd; Кристофферсен, Энн Карин; Абеша-Белай, Эмнет; Enersen, Morten; Рёкке, Ола; Ольсен, Ингар (01.01.2016). «Бактерии полости рта, кишечника и кожи в сетчатых имплантатах вентральной грыжи». Журнал оральной микробиологии. 8 (1): 31854. Дои:10.3402 / jom.v8.31854. ЧВК 4967714. PMID 27476443.
- ^ а б Olsen, Margaret A .; Никель, Кателин Б .; Уоллес, Анна Е .; Майнс, Дэниел; Фрейзер, Виктория Дж .; Уоррен, Дэвид К. (март 2015 г.). «Стратификация инфекции места операции по действующим факторам и сравнение показателей инфицирования после герниопластики». Инфекционный контроль и больничная эпидемиология. 36 (3): 329–335. Дои:10.1017 / ice.2014.44. ISSN 0899-823X. ЧВК 4683022. PMID 25695175.
- ^ «Протокол наблюдения за инфекцией в области хирургического вмешательства» (PDF).
- ^ Акьол, Джихангир; Коджаай, Фират; Орозакунов, Эркинбек; Генч, Волкан; Кепенекчи Байрам, Илькнур; Чакмак, Атил; Баскан, Семих; Кутердем, Эркумент (2013). «Исход пациентов с хронической сетчатой инфекцией после открытой пластики паховой грыжи». Журнал Корейского хирургического общества. 84 (5): 287. Дои:10.4174 / jkss.2013.84.5.287. ISSN 2233-7903. ЧВК 3641368. PMID 23646314.
- ^ Erdas, E .; Medas, F .; Pisano, G .; Nicolosi, A .; Кало, П. Г. (декабрь 2016 г.). «Антибиотикопрофилактика при пластике паховой грыжи открытой сеткой: систематический обзор и метаанализ». Грыжа. 20 (6): 765–776. Дои:10.1007 / s10029-016-1536-0. ISSN 1265-4906.
- ^ а б Кейруз, Антониос; Радачи, Норберт; Рен, Цюнь; Домманн, Алекс; Бельди, Гвидо; Маниура-Вебер, Катарина; Росси, Рене М .; Фортунато, Джузеппино (18.03.2020). «Антимикробные нановолокна из нейлона-6 / хитозана с сердцевиной и оболочкой для предотвращения инфицирования хирургической области, связанной с сеткой». Журнал нанобиотехнологий. 18 (1): 51. Дои:10.1186 / s12951-020-00602-9. ISSN 1477-3155. ЧВК 7081698. PMID 32188479.
- ^ Энгельсман, А. Ф .; Мей, Х. К. ван дер; Busscher, H.J .; Плоег, Р. Дж. (2008). «Морфологические аспекты хирургических сеток как фактор риска бактериальной колонизации». BJS (Британский журнал хирургии). 95 (8): 1051–1059. Дои:10.1002 / bjs.6154. ISSN 1365-2168.
- ^ Goëau-Brissonnière, O .; Leflon, V .; Леторт, М .; Николас, М. Х. (1 февраля 1999 г.). «Устойчивость полимерных сеток, связанных с антибиотиками, покрытых желатином, к Staphylococcus aureus в модели подкожного мешка кролика». Биоматериалы. 20 (3): 229–232. Дои:10.1016 / S0142-9612 (98) 00164-1. ISSN 0142-9612.
- ^ «Минимально инвазивная методика восстановления сетки при лечении инфекции грыжевой сетки: серия случаев». Международный журнал хирургических историй болезни. 70: 78–82. 2020-01-01. Дои:10.1016 / j.ijscr.2020.04.055. ISSN 2210-2612. ЧВК 7226635. PMID 32413773.
- ^ Лю, Пэнби; Чен, Нанлян; Цзян, Цзиньхуа; Вэнь Сюэцзюнь (23.05.2019). «Приготовление и оценка in vitro новой композитной сетки, функционализированной катионным антимикробным пептидом». Материалы. 12 (10): 1676. Дои:10.3390 / ma12101676. ISSN 1996-1944. ЧВК 6566986. PMID 31126063.
- ^ Грант, Д. Н .; Benson, J .; Cozad, M. J .; Whelove, О.Е .; Бахман, С. Л .; Ramshaw, B.J .; Грант, Д. А .; Грант, С.А. (01.12.2011). «Конъюгирование наночастиц золота с полипропиленовой сеткой для повышения биосовместимости». Журнал материаловедения: материалы в медицине. 22 (12): 2803–2812. Дои:10.1007 / s10856-011-4449-6. ISSN 1573-4838.
- ^ «MycroMesh и DualMesh Plus от GORE».
- ^ "Xenmatric от BARD Davol".
- ^ "Ventrio by BD".
