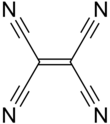
Тетрацианоэтилен - Tetracyanoethylene
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Ethenetetracarbonitrile | |||
| Другие имена TCNE | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ChemSpider | |||
| ECHA InfoCard | 100.010.527 | ||
PubChem CID | |||
| UNII | |||
| |||
| |||
| Характеристики | |||
| C6N4 | |||
| Молярная масса | 128.094 г · моль−1 | ||
| Плотность | 1,35 г / см3 | ||
| Температура плавления | 199 ° С (390 ° F, 472 К) | ||
| Точка кипения | От 130 до 140 ° C (от 266 до 284 ° F; от 403 до 413 K) 0,1 мм рт. Ст. (возвышенный )[1] | ||
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Тетрацианоэтилен (TCNE) является органическое соединение с формулой C2(CN)4. Это бесцветное твердое вещество. Это важный член цианоуглероды.
Синтез и реакции
TCNE подготовлен бромирование малононитрил в присутствии бромид калия дать KBr-комплекс и дегалогенировать с медь.[1]
Окисление TCNE с пероксид водорода дает соответствующий эпоксид, обладающий необычными свойствами.[2]
Редокс химия
TCNE часто используется в качестве акцептора электронов. Цианогруппы имеют π * -орбитали с низкой энергией, и присутствие четырех таких групп с их π-системами (сопряженными) с центральной двойной связью C = C приводит к образованию электрофильного алкена. TCNE уменьшается на йодид дать анион-радикалу:
- C2(CN)4 + Я− → [C2(CN)4]− + 1⁄2 я2
Из-за своей планарности и способности принимать электроны TCNE использовался для приготовления множества органические сверхпроводники, обычно служа одноэлектронным окислителем органического донора электронов. Такой соли с переносом заряда иногда называют Соли Бехгаарда.
Безопасность
TCNE гидролизуется во влажном воздухе с образованием цианистый водород и с ними следует обращаться соответственно.[1]
Рекомендации
- ^ а б c Карбони, Р. А. (1963). «Тетрацианоэтилен». Органический синтез.; Коллективный объем, 4, п. 877
- ^ Линн, У. Дж. (1973). «Оксид тетрацианоэтилена». Органический синтез.; Коллективный объем, 5, п. 1007