Поворот (биохимия) - Turn (biochemistry)
А повернуть является элементом вторичная структура в белках, у которых полипептидная цепь меняет свое общее направление.
Определение
Согласно одному определению,[1] поворот - структурный мотив, где Cα атомы двух остатков, разделенных несколькими (обычно от 1 до 5) пептидные связи близки (менее 7Å [0.70 нм ]). Близость терминала Cα атомов часто коррелирует с образованием межосновной цепи водородная связь между соответствующими остатками. Такая водородная связь является основой первоначального, возможно, более известного определения витка. Во многих случаях, но не во всех, водородные связи и Cαопределения -расстояния эквивалентны.
Виды поворотов
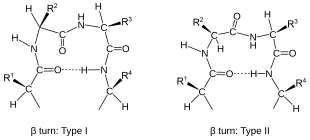
Повороты классифицируются[2] согласно разделению между двумя концевыми остатками:
- В α-поворот конечные остатки разделены четыре пептидные связи (я → я ± 4).
- В β-поворот (наиболее распространенная форма), по три облигации (я → я ± 3).
- В γ-поворот, к два облигации (я → я ± 2).
- В δ-поворот, к один связь (я → я ± 1), что стерически маловероятно.
- В π-поворот, к пять облигации (я → я ± 5).
| Тип | φя + 1 | ψя + 1 | φя + 2 | ψя + 2 |
|---|---|---|---|---|
| я | −60° | −30° | −90° | 0° |
| II | −60° | 120° | 80° | 0° |
| VIII | −60° | −30° | −120° | 120° |
| Я' | 60° | 30° | 90° | 0° |
| II ′ | 60° | −120° | −80° | 0° |
| VIa1 | −60° | 120° | −90° | 0°* |
| VIa2 | −120° | 120° | −60° | 0°* |
| VIb | −135° | 135° | −75° | 160°* |
| IV | очереди исключены из всех вышеперечисленных категорий | |||
Повороты классифицируются по их основам двугранные углы (видеть Рамачандран сюжет ). Ход можно превратить в свой обратный поворот (в котором атомы основной цепи имеют противоположные хиральность ), изменив знак на его двугранных углах. (Обратный поворот не верен энантиомер поскольку Cα атом хиральность сохраняется.) Таким образом, γ-поворот имеет две формы, классическую форму с (φ, ψ) двугранные углы примерно (75 °, -65 °) и обратная форма с двугранными углами (-75 °, 65 °). По крайней мере восемь форм бета-ход происходят, в зависимости от того, СНГ изомер пептидной связи участвует и в двугранных углах двух центральных остатков. Классический и обратный β-повороты выделяются штрихом: например, тип I и тип I ′ бета-ходы. Если я → я + 3 водородная связь берется за критерий для поворотов, четыре категории Венкатачалам[4] (I, II, II ′, I ′) достаточно[5] описать все возможные бета-ходы. Все четыре часто встречаются в белках, но чаще всего встречается I, за которым следуют II, I 'и II' в этом порядке.
Петли
An ω-петля является универсальным термином для более длинных, протяженных или нерегулярных петель без фиксированной внутренней водородной связи.
Несколько поворотов
Во многих случаях один или несколько остатков участвуют в двух частично перекрывающихся витках. Например, в последовательности из 5 остатков оба остатка с 1 по 4 и остатки со 2 по 5 образуют очередь; в таком случае говорят о (я, я + 1) двойной поворот. Множественные повороты (до семи раз) обычно встречаются в белках.[6] Ленты Beta bend представляют собой другой тип многооборотного.
Заколки для волос
А заколка для волос представляет собой частный случай поворота, при котором направление основной цепи белка меняется на противоположное и фланкирующие элементы вторичной структуры взаимодействуют. Например, бета шпилька соединяет два водородная связь, антипараллельные β-тяжи (название довольно запутанное, так как β-шпилька может содержать много типов витков - α, β, γ и т. д.).
Бета шпильки могут быть классифицированы по количеству остатков, составляющих черед, то есть нет часть фланкирующих β-тяжей.[7] Если это число - X или Y (согласно двум различным определениям β листов), шпилька β определяется как X: Y.
Бета повороты на концах петли бета шпильки имеют другое распределение типов по сравнению с другими; тип I 'является наиболее распространенным, за ним следуют типы II', I и II.
Гибкие линкеры
Иногда повороты встречаются внутри гибкие линкеры или петли, соединяющие белковые домены. Последовательности линкера различаются по длине и обычно богаты полярными незаряженными аминокислоты. Гибкие линкеры позволяют соединяющимся доменам свободно скручиваться и поворачиваться для привлечения своих связывающих партнеров через динамика домена белка. Они также позволяют своим связывающим партнерам вызывать более крупный масштаб конформационные изменения на дальние расстояния аллостерия[8][9][10]
Роль в сворачивании белка
Были предложены две гипотезы о роли поворотов в сворачивание белка. С одной точки зрения, повороты играют решающую роль в складывании, объединяя и обеспечивая или разрешая взаимодействия между регулярными элементами вторичной структуры. Эта точка зрения подтверждается исследованиями мутагенеза, указывающими на критическую роль определенных остатков в поворотах некоторых белков. Кроме того, неродные изомеры X−Pro пептидные связи в свою очередь может полностью блокировать конформационную укладку некоторых белков. С другой стороны, повороты играют пассивную роль при сбрасывании. Это мнение подтверждается плохой консервацией аминокислот, наблюдаемой в большинстве поворотов. Кроме того, неродные изомеры многих X-Pro пептидные связи в свою очередь, мало или совсем не влияют на складывание.
Методы прогнозирования бета-разворота
За прошедшие годы было разработано множество методов прогнозирования бета-разворота. Недавно, Группа доктора Рагхавы развитый BetaTPred3 метод, который предсказывает полный бета-поворот, а не отдельные остатки, падающие в бета-поворот. Этот метод также обеспечивает хорошую точность и является первым методом, который предсказывает все 9 типов бета-разворотов. Помимо прогнозирования, этот метод также можно использовать для определения минимального количества мутаций, необходимых для инициирования или разрыва бета-поворота в белке в желаемом месте.
Смотрите также
Примечания
- ^ см. Rose et al. 1985 в Справочниках
- ^ Тониоло 1980
- ^ Venkatachalam 1968; Ричардсон 1981; Хатчинсон и Торнтон 1994
- ^ Венкатачалам, CM (1968). «Стерохимические критерии полипептидов и белков. V. Конформации системы трех связанных пептидных единиц» (PDF). Биополимеры. 6 (10): 1425–1436. Дои:10.1002 / bip.1968.360061006. HDL:2027.42/37819. PMID 5685102.
- ^ Ричардсон, Дж. С. (1981). Анатомия и таксономия структуры белка. Adv Protein Chem. Успехи в химии белков. 34. С. 167–339. Дои:10.1016 / с0065-3233 (08) 60520-3. ISBN 9780120342341. PMID 7020376.
- ^ Хатчинсон 1994, стр 2213
- ^ Сибанда 1989
- ^ Дункер А. К., Лоусон Дж. Д., Браун Си Джей, Уильямс Р. М., Ромеро П., О Дж. С., Олдфилд Си Джей, Кэмпен А. М., Рэтлифф К. М., Хиппс К. В., Аусио Дж., Ниссен М. С., Ривз Р., Канг С., Киссинджер К. Р., Бейли Р. В., Гризволд, доктор медицины , Чиу В., Гарнер Э.С., Обрадович З. (2001). «Внутренне неупорядоченный белок». Журнал молекулярной графики и моделирования. 19 (1): 26–59. CiteSeerX 10.1.1.113.556. Дои:10.1016 / с1093-3263 (00) 00138-8. PMID 11381529.
- ^ Bu Z, Callaway DJ (2011). «Белки движутся! Белковая динамика и дальняя аллостерия в передаче сигналов клетки». Структура белка и заболевания. Достижения в химии белков и структурной биологии. 83. С. 163–221. Дои:10.1016 / B978-0-12-381262-9.00005-7. ISBN 9780123812629. PMID 21570668.
- ^ Compiani M, Capriotti E (декабрь 2013 г.). «Вычислительные и теоретические методы фолдинга белков» (PDF). Биохимия. 52 (48): 8601–24. Дои:10.1021 / bi4001529. PMID 24187909. Архивировано из оригинал (PDF) на 2015-09-04.
внешняя ссылка
- BetaTPred3 - платформа Insilico для прогнозирования и инициации бетатурнов в белке в желаемом месте Ссылка на статью
- NetTurnP - Прогнозирование участков бета-поворота в белковых последовательностях
- BetaTPred - Прогнозирование бета-поворотов белков с использованием статистических алгоритмов
Рекомендации
Эти ссылки отсортированы по дате.
- Venkatachalam CM. (1968). «Стереохимические критерии полипептидов и белков. V. Конформация системы трех связанных пептидных единиц». Биополимеры. 6 (10): 1425–36. Дои:10.1002 / bip.1968.360061006. HDL:2027.42/37819. PMID 5685102.
- Немети, Джордж; Принц, Мортон П. (1972). "The -Turn, возможная складчатая конформация полипептидной цепи. Сравнение с β-поворотом ». Макромолекулы. 5 (6): 755–758. Дои:10.1021 / ma60030a017.
- Льюис П.Н., Момани Ф.А., Шерага Н.А. (1973). «Повороты цепи в белках». Biochim Biophys Acta. 303 (2): 211–29. Дои:10.1016/0005-2795(73)90350-4. PMID 4351002.
- Toniolo C .; Бенедетти, Этторе (1980). «Внутримолекулярные конформации пептидов с водородной связью». CRC Crit Rev Biochem. 9 (1): 1–44. Дои:10.3109/10409238009105471. PMID 6254725.
- Ричардсон Дж. С.. (1981). Анатомия и таксономия структуры белка. Adv Protein Chem. Успехи в химии белков. 34. С. 167–339. Дои:10.1016 / S0065-3233 (08) 60520-3. ISBN 9780120342341. PMID 7020376.
- Роуз Г.Д., Гираш Л.М., Смит Дж. А. (1985). Превращает пептиды и белки. Adv Protein Chem. Успехи в химии белков. 37. С. 1–109. Дои:10.1016 / S0065-3233 (08) 60063-7. ISBN 9780120342372. PMID 2865874.
- Милнер-Уайт Э.Дж., Поэт Р. (1987). «Петли, выпуклости, повороты и шпильки в белках». Тенденции Biochem Sci. 12: 189–192. Дои:10.1016/0968-0004(87)90091-0.
- Уилмот CM, Торнтон JM (1988). «Анализ и прогнозирование различных типов бета-превращения белков». Дж Мол Биол. 203 (1): 221–32. Дои:10.1016/0022-2836(88)90103-9. PMID 3184187.
- Sibanda, B.L .; Blundell, T.L .; Торнтон, Дж. М. (1989). «Конформация β-шпилек в белковых структурах :: систематическая классификация с приложениями к моделированию по гомологии, подгонке электронной плотности и инженерии белков». Журнал молекулярной биологии. 206 (4): 759–777. Дои:10.1016/0022-2836(89)90583-4. PMID 2500530.
- Милнер-Уайт, Э (1990). «Ситуации гамма-поворотов в белках. Их связь с альфа-спиралями, бета-листами и сайтами связывания лигандов». J. Mol. Биол. 216 (2): 385–397. Дои:10.1016 / S0022-2836 (05) 80329-8. PMID 2254936.
- Hutchinson, E.G .; Торнтон, Дж. М. (1994). «Пересмотренный набор потенциалов для образования β-поворотов в белках». Белковая наука. 3 (12): 2207–2216. Дои:10.1002 / pro.5560031206. ЧВК 2142776. PMID 7756980.
- Павоне V, Гаэта Г, Ломбарди А, Настри Ф, Маглио О, Изерния С, Савиано М (1996). «Обнаружение вторичных структур белков: классификация и описание изолированных альфа-поворотов». Биополимеры. 38 (6): 705–21. Дои:10.1002 / (SICI) 1097-0282 (199606) 38: 6 <705 :: AID-BIP3> 3.0.CO; 2-V. PMID 8652792.
- Раджашанкар К.Р., Рамакумар С. (1996). «Пи-повороты в белках и пептидах: классификация, конформация, наличие, гидратация и последовательность». Белковая наука. 5 (5): 932–46. Дои:10.1002 / pro.5560050515. ЧВК 2143406. PMID 8732765. Архивировано из оригинал на 24.05.2009.

