Сворачивание белков - Protein folding
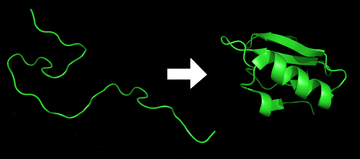

Сворачивание белков это физический процесс по которому белок сеть приобретает родной трехмерная структура, а конформация это обычно биологически функционально, быстро и воспроизводимо. Это физический процесс, посредством которого полипептид складывается в характерную и функциональную трехмерную структуру из случайный катушки.[1] Каждый белок существует как развернутый полипептид или случайный клубок, когда переведено из последовательности мРНК к линейной цепочке аминокислоты. У этого полипептида отсутствует какая-либо стабильная (долговечная) трехмерная структура (левая часть первого рисунка). Поскольку полипептидная цепь синтезируется рибосома, линейная цепочка начинает сворачиваться в свою трехмерную структуру. Сворачивание начинает происходить даже при трансляции полипептидной цепи. Аминокислоты взаимодействуют друг с другом, образуя четко определенную трехмерную структуру, свернутый белок (правая часть рисунка), известный как родное государство. Полученная трехмерная структура определяется аминокислотной последовательностью или первичной структурой (Догма Анфинсена ).[2]
Правильная трехмерная структура необходима для функционирования, хотя некоторые части функциональных белков может оставаться развернутым,[3] так что динамика белка это важно. Неспособность свернуться в нативную структуру обычно дает неактивные белки, но в некоторых случаях неправильно свернутые белки имеют модифицированную или токсичную функциональность. Несколько нейродегенеративный и другие болезни считается результатом накопления амилоид фибриллы образованы неправильно свернутыми белками.[4] Много аллергия вызваны неправильным сворачиванием некоторых белков, потому что иммунная система не производит антитела для определенных белковых структур.[5]
Денатурация белков - это процесс перехода от свернутого к развернутое состояние. Это происходит в Готовка, в ожоги, в протеинопатии, и в других контекстах.
Продолжительность процесса сворачивания сильно варьируется в зависимости от интересующего белка. Когда учился вне камеры, самым медленным сворачиванием белков требуется много минут или часов, чтобы сворачиваться в основном из-за изомеризация пролина, и должен пройти через ряд промежуточных состояний, например контрольных точек, прежде чем процесс будет завершен.[6] С другой стороны, очень маленькие одиночныедомен белки длиной до сотни аминокислот обычно складываются за один этап.[7] Временные шкалы в миллисекунды являются нормой, и самые быстрые из известных реакций сворачивания белка завершаются в течение нескольких микросекунд.[8]
Точный предсказание структуры свернутого белка была главной целью вычислительная биология с конца 1960-х гг. Понимание деталей того, как процесс складывания на самом деле происходит в природе, - еще одна проблема.
Процесс сворачивания белка
Первичная структура
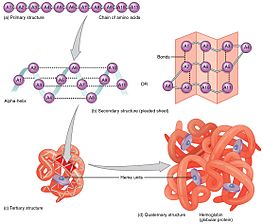
В первичная структура белка, его линейная аминокислотная последовательность, определяет его нативную конформацию.[9] Конкретные аминокислотные остатки и их положение в полипептидной цепи являются определяющими факторами, для которых части белка плотно складываются вместе и образуют его трехмерную конформацию. Аминокислотный состав не так важен, как последовательность.[10] Однако существенным фактом фолдинга остается то, что аминокислотная последовательность каждого белка содержит информацию, которая определяет как нативную структуру, так и путь достижения этого состояния. Это не означает, что почти идентичные аминокислотные последовательности всегда складываются одинаково.[11] Конформации различаются также в зависимости от факторов окружающей среды; похожие белки складываются по-разному в зависимости от того, где они находятся.
Вторичная структура
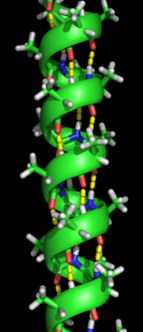

Формирование вторичная структура это первый шаг в процессе сворачивания, который принимает белок, чтобы принять свою нативную структуру. Для вторичной структуры характерны структуры, известные как альфа спирали и бета-листы которые быстро складываются, потому что они стабилизируются внутримолекулярный водородные связи, как это было впервые охарактеризовано Линус Полинг. Образование внутримолекулярных водородных связей вносит еще один важный вклад в стабильность белка.[12] α-спирали образованы водородными связями позвоночник в форме спирали (см. рисунок справа).[10] Β-гофрированный лист - это структура, которая формируется, когда основная цепь изгибается над собой, образуя водородные связи (как показано на рисунке слева). Водородные связи находятся между амидным водородом и карбонильным кислородом пептидная связь. Существуют антипараллельные β-гофрированные листы и параллельные β-гофрированные листы, где стабильность водородных связей выше в антипараллельном β-листе, поскольку он связывает водородные связи с идеальным углом 180 градусов по сравнению с наклонными водородными связями, образованными параллельными листами.[10]
Третичная структура
Альфа-спирали и бета-гофрированные листы могут быть амфипатический в природе или содержат гидрофильную часть и гидрофобную часть. Это свойство вторичных конструкций способствует третичная структура белка в котором складывание происходит так, что гидрофильные стороны обращены к водный среда, окружающая белок, и гидрофобные стороны обращены к гидрофобному ядру белка.[13] Вторичная структура иерархически уступает место образованию третичной структуры. После того, как третичная структура белка сформирована и стабилизируется за счет гидрофобных взаимодействий, также может возникнуть ковалентная связь в виде дисульфидные мостики сформированный между двумя цистеин остатки. Третичная структура белка включает одну полипептидную цепь; однако дополнительные взаимодействия свернутых полипептидных цепей приводят к образованию четвертичной структуры.[14]
Четвертичная структура
Третичная структура может уступить место образованию четвертичная структура в некоторых белках, что обычно включает «сборку» или «совместную сборку» субъединиц, которые уже свернуты; другими словами, несколько полипептидных цепей могут взаимодействовать с образованием полностью функционального четвертичного белка.[10]
Движущие силы сворачивания белка
Складывание - это самопроизвольный процесс что в основном определяется гидрофобными взаимодействиями, образованием внутримолекулярных водородные связи, силы Ван дер Ваальса, и ему противостоит конформационная энтропия.[15] Часто начинается процесс складывания совместный перевод, таким образом N-конец белка начинает сворачиваться, в то время как C-терминал часть белка все еще синтезированный посредством рибосома; однако молекула белка может спонтанно складываться во время или после биосинтез.[16] Пока эти макромолекулы можно рассматривать как "складываются ", процесс также зависит от растворитель (воды или липидный бислой ),[17] концентрация соли, то pH, то температура, возможное присутствие кофакторов и молекулярных шапероны.
Белки будут иметь ограничения на их способность к складыванию из-за ограниченных углов изгиба или возможных конформаций. Эти допустимые углы сворачивания белка описываются двумерным графиком, известным как Рамачандран сюжет с допустимыми углами поворота в фунтах на кв. дюйм и фи.[18]
Гидрофобный эффект

Сворачивание белка должно быть термодинамически благоприятным внутри клетки, чтобы реакция была спонтанной. Поскольку известно, что сворачивание белка является спонтанной реакцией, она должна иметь отрицательный характер. Свободная энергия Гиббса ценность. Свободная энергия Гиббса при сворачивании белка напрямую связана с энтальпия и энтропия.[10] Для возникновения отрицательной дельта G и для того, чтобы сворачивание белка стало термодинамически благоприятным, тогда либо энтальпия, либо энтропия, либо оба условия должны быть благоприятными.
Сведение к минимуму количества гидрофобных боковых цепей, подверженных воздействию воды, является важной движущей силой процесса складывания.[19] Гидрофобный эффект - это явление, при котором гидрофобные цепи белка схлопываются в ядро белка (вдали от гидрофильной среды).[10] В водной среде молекулы воды имеют тенденцию к агрегированию вокруг гидрофобных областей или боковых цепей белка, создавая водные оболочки из упорядоченных молекул воды.[20] Упорядочение молекул воды вокруг гидрофобной области увеличивает порядок в системе и, следовательно, способствует отрицательному изменению энтропии (уменьшению энтропии в системе). Молекулы воды закреплены в этих водяных клетках, что приводит в движение гидрофобный коллапс или складывание внутрь гидрофобных групп. Гидрофобный коллапс возвращает энтропию в систему за счет разрушения водяных клеток, что освобождает упорядоченные молекулы воды.[10] Множество гидрофобных групп, взаимодействующих внутри ядра глобулярно свернутого белка, вносит значительный вклад в стабильность белка после складывания из-за значительного накопления сил Ван-дер-Ваальса (в частности, Лондонские силы рассеяния ).[10] В гидрофобный эффект существует как движущая сила в термодинамике только при наличии водной среды с амфифильный молекула, содержащая большую гидрофобную область.[21] Прочность водородных связей зависит от их окружения; таким образом, водородные связи, заключенные в гидрофобное ядро, вносят больший вклад, чем водородные связи, находящиеся в водной среде, для стабильности нативного состояния.[22]
В белках с глобулярными складками гидрофобные аминокислоты имеют тенденцию быть вкрапленными вдоль первичной последовательности, а не случайным образом распределены или сгруппированы вместе.[23][24] Однако недавно появившиеся белки de novo, которые, как правило, внутренне неупорядоченный,[25][26] показывают противоположный паттерн кластеризации гидрофобных аминокислот вдоль первичной последовательности.[27]
Шапероны

Молекулярные шапероны представляют собой класс белков, которые помогают в правильном сворачивании других белков in vivo. Шапероны существуют во всех клеточных компартментах и взаимодействуют с полипептидной цепью, чтобы позволить сформироваться нативной трехмерной конформации белка; однако сами шапероны не входят в окончательную структуру белка, которому они помогают.[28] Шапероны могут способствовать сворачиванию, даже если возникающий полипептид синтезируется рибосомой.[29] Молекулярные шапероны действуют путем связывания для стабилизации нестабильной в других отношениях структуры белка в его пути складывания, но шапероны не содержат необходимой информации, чтобы знать правильную нативную структуру белка, которому они помогают; скорее, шапероны работают, предотвращая неправильные складчатые конформации.[29] Таким образом, шапероны фактически не увеличивают частоту отдельных шагов, участвующих в пути сворачивания к нативной структуре; вместо этого они работают, уменьшая возможные нежелательные агрегации полипептидной цепи, которые в противном случае могли бы замедлить поиск подходящего промежуточного соединения, и они обеспечивают более эффективный путь для полипептидной цепи, чтобы принять правильные конформации.[28] Шапероны не следует путать с катализаторами сворачивания, которые на самом деле катализируют медленные в противном случае этапы пути сворачивания. Примерами катализаторов фолдинга являются протеин-дисульфидные изомеразы и пептидил-пролилизомеразы, которые могут участвовать в образовании дисульфидных связей или взаимном превращении между цис- и транс-стереоизомерами соответственно.[29] Показано, что шапероны имеют решающее значение в процессе сворачивания белков. in vivo потому что они предоставляют белку помощь, необходимую для принятия его надлежащих выравниваний и конформаций, достаточно эффективно, чтобы стать «биологически значимыми».[30] Это означает, что полипептидная цепь теоретически может складываться в свою нативную структуру без помощи шаперонов, как показали проведенные эксперименты по укладке белков. in vitro;[30] однако этот процесс оказывается слишком неэффективным или слишком медленным, чтобы существовать в биологических системах; следовательно, шапероны необходимы для сворачивания белков. in vivo. Наряду с их ролью в содействии формированию нативной структуры, шапероны, как показано, участвуют в различных ролях, таких как транспорт белка, деградация и даже позволяют денатурированные белки подверженные воздействию определенных внешних денатурирующих факторов, они получают возможность перестроиться в свои правильные естественные структуры.[31]
Полностью денатурированный белок не имеет ни третичной, ни вторичной структуры и существует как так называемый случайный катушки. При определенных условиях некоторые белки могут складываться заново; однако во многих случаях денатурация необратима.[32] Клетки иногда защищают свои белки от денатурирующего воздействия тепла с помощью ферменты известный как белки теплового шока (тип шаперона), которые помогают другим белкам складываться и оставаться свернутыми. Белки теплового шока были обнаружены у всех исследованных видов, начиная с бактерии для людей, предполагая, что они развились очень рано и выполняют важную функцию. Некоторые белки вообще никогда не сворачиваются в клетках, кроме как с помощью шаперонов, которые либо изолируют отдельные белки, так что их сворачивание не прерывается взаимодействиями с другими белками, либо помогают разворачивать неправильно свернутые белки, позволяя им преобразоваться в правильную нативную структуру.[33] Эта функция имеет решающее значение для предотвращения риска атмосферные осадки в нерастворимый аморфные агрегаты. К внешним факторам, участвующим в денатурации белка или нарушении нативного состояния, относятся температура, внешние поля (электрические, магнитные),[34] молекулярное скопление,[35] и даже ограничение пространства (т. е. замкнутость), которое может иметь большое влияние на сворачивание белков.[36] Высокая концентрация растворенные вещества, крайности pH, механические силы и присутствие химических денатурирующих веществ также могут способствовать денатурации белка. Эти отдельные факторы вместе классифицируются как стрессы. Показано, что шапероны существуют в возрастающих концентрациях во время клеточного стресса и помогают правильному сворачиванию возникающих белков, а также денатурированных или неправильно свернутых.[28]
При некоторых условиях белки не будут сворачиваться в свои биохимически функциональные формы. Температура выше или ниже диапазона, в котором обычно живут клетки, вызовет термически нестабильный белки разворачиваются или денатурируются (вот почему кипячение вызывает Яичный белок становятся непрозрачными). Однако термостойкость белков далеко не постоянна; Например, гипертермофильные бактерии было обнаружено, что они растут при температуре до 122 ° C,[37] что, конечно, требует, чтобы их полный набор жизненно важных белков и белковых ансамблей был стабильным при этой температуре или выше.
Бактерия Кишечная палочка хозяин для бактериофаг Т4, и кодируемый фагом белок gp31, по-видимому, функционально гомологичен Кишечная палочка шаперонный белок GroES и может заменить его в сборке бактериофага Т4 вирус частицы при заражении.[38] Подобно GroES, gp31 образует стабильный комплекс с GroEL шаперонин, который абсолютно необходим для сворачивания и сборки in vivo основного капсидного белка бактериофага Т4 gp23.[38]
Неправильная упаковка белка и нейродегенеративное заболевание
Белок считается неправильно сложенный если он не может достичь своего нормального исходного состояния. Это может быть связано с мутациями в аминокислотной последовательности или нарушением нормального процесса сворачивания внешними факторами.[39] Неправильно свернутый белок обычно содержит β-листы которые организованы в супрамолекулярную структуру, известную как перекрестная β-структура. Эти богатые β-слоями ансамбли очень стабильны, очень нерастворимы и обычно устойчивы к протеолизу.[40] Структурная стабильность этих фибриллярных ансамблей обусловлена обширными взаимодействиями между белковыми мономерами, образованными водородными связями основной цепи между их β-цепями.[40] Неправильная укладка белков может вызвать дальнейшую неправильную укладку и накопление других белков в агрегаты или олигомеры. Повышенный уровень агрегированных белков в клетке приводит к образованию амилоид -подобные структуры, которые могут вызывать дегенеративные нарушения и гибель клеток.[39] Амилоиды представляют собой фибриллярные структуры, которые содержат межмолекулярные водородные связи, которые очень нерастворимы и образованы из преобразованных белковых агрегатов.[39] Следовательно, протеасомный путь может быть недостаточно эффективным для разрушения неправильно свернутых белков до агрегации. Неправильно свернутые белки могут взаимодействовать друг с другом и образовывать структурированные агрегаты и приобретать токсичность за счет межмолекулярных взаимодействий.[39]
Агрегированные белки связаны с прион -связанные заболевания, такие как Болезнь Крейтцфельдта-Якоба, губчатая энцефалопатия (коровье бешенство), амилоид -связанные заболевания, такие как Болезнь Альцгеймера и семейная амилоидная кардиомиопатия или полинейропатия,[41] а также заболевания внутриклеточной агрегации, такие как Хантингтона и болезнь Паркинсона.[4][42] Эти возрастные дегенеративные заболевания связаны с агрегацией неправильно свернутых белков в нерастворимые внеклеточные агрегаты и / или внутриклеточные включения, включая перекрестные β амилоид фибриллы. Не совсем ясно, являются ли агрегаты причиной или просто отражением потери гомеостаза белка, баланса между синтезом, сворачиванием, агрегацией и обменом белка. Недавно Европейское агентство по лекарствам одобрил использование Тафамидис или Виндакель (кинетический стабилизатор тетрамерного транстиретина) для лечения заболеваний, связанных с амилоидом транстиретина. Это свидетельствует о том, что процесс образования амилоидных фибрилл (а не самих фибрилл) вызывает дегенерацию постмитотической ткани при амилоидных заболеваниях человека.[43] Неправильная укладка и чрезмерная деградация вместо складывания и функционирования приводит к ряду протеопатия болезни, такие как антитрипсин -ассоциированный эмфизема, кистозный фиброз и лизосомные болезни накопления, где потеря функции является причиной беспорядка. В то время как заместительная белковая терапия исторически использовалась для коррекции последних расстройств, появляется новый подход: фармацевтические шапероны сворачивать мутировавшие белки, чтобы сделать их функциональными.
Экспериментальные методы изучения сворачивания белков
В то время как выводы о сворачивании белка можно сделать через мутации как правило, экспериментальные методы изучения сворачивания белков основываются на постепенное развертывание или сворачивание белков и наблюдение конформационных изменений с использованием стандартных некристаллографических методов.
Рентгеновская кристаллография
Рентгеновская кристаллография является одним из наиболее эффективных и важных методов попытки расшифровать трехмерную конфигурацию свернутого белка.[44] Для возможности проведения рентгеновской кристаллографии исследуемый белок должен находиться внутри кристаллической решетки. Чтобы поместить белок в кристаллическую решетку, необходимо иметь подходящий растворитель для кристаллизации, получить чистый белок на перенасыщенных уровнях в растворе и осаждать кристаллы в растворе.[45] После того, как белок кристаллизован, рентгеновские лучи могут быть сконцентрированы через кристаллическую решетку, которая будет дифракционировать лучи или направлять их наружу в различных направлениях. Эти выходящие лучи соотносятся с конкретной трехмерной конфигурацией белка, заключенного внутри. Рентгеновские лучи взаимодействуют с электронными облаками, окружающими отдельные атомы в кристаллической решетке белка, и создают различимую дифракционную картину.[13] Только связав облака электронной плотности с амплитудой рентгеновских лучей, можно прочитать эту картину и сделать предположения о фазах или фазовых углах, которые усложняют этот метод.[46] Без связи, установленной на математической основе, известной как преобразование Фурье, "фазовая проблема "очень затруднит предсказание дифракционных картин.[13] Новые методы, такие как множественная изоморфная замена использовать присутствие иона тяжелого металла для более предсказуемой дифракции рентгеновских лучей, уменьшения количества задействованных переменных и решения фазовой проблемы.[44]
Флуоресцентная спектроскопия
Флуоресцентная спектроскопия это высокочувствительный метод изучения состояния сворачивания белков. Три аминокислоты, фенилаланин (Phe), тирозин (Tyr) и триптофан (Trp), обладают собственными флуоресцентными свойствами, но только Tyr и Trp используются экспериментально, поскольку их квантовые выходы достаточно высоки, чтобы давать хорошие сигналы флуоресценции. И Trp, и Tyr возбуждаются на длине волны 280 нм, тогда как только Trp возбуждается на длине волны 295 нм. Из-за их ароматического характера остатки Trp и Tyr часто обнаруживаются полностью или частично погруженными в гидрофобное ядро белков, на границе раздела между двумя доменами белка или на границе раздела между субъединицами олигомерных белков. В этой неполярной среде они имеют высокий квантовый выход и, следовательно, высокую интенсивность флуоресценции. После разрушения третичной или четвертичной структуры белка эти боковые цепи становятся более подверженными воздействию гидрофильной среды растворителя, и их квантовые выходы уменьшаются, что приводит к низкой интенсивности флуоресценции. Для остатков Trp длина волны их максимальной флуоресцентной эмиссии также зависит от их окружения.
Флуоресцентную спектроскопию можно использовать для характеристики установление равновесия белков путем измерения изменения интенсивности флуоресцентного излучения или длины волны максимального излучения в зависимости от значения денатуранта.[47][48] Денатурирующий агент может представлять собой химическую молекулу (мочевину, гидрохлорид гуанидиния), температуру, pH, давление и т.д. Равновесие между различными, но дискретными состояниями белка, то есть нативным состоянием, промежуточными состояниями, развернутым состоянием, зависит от значения денатурирующего агента; следовательно, глобальный сигнал флуоресценции их равновесной смеси также зависит от этого значения. Таким образом, получают профиль, связывающий глобальный белковый сигнал со значением денатуранта. Профиль равновесного развертывания может позволить обнаруживать и идентифицировать промежуточные звенья развертывания.[49][50] Общие уравнения были разработаны Hugues Bedouelle для получения термодинамических параметров, которые характеризуют развертывающиеся равновесия для гомомерных или гетеромерных белков, вплоть до тримеров и потенциально тетрамеров, из таких профилей.[47] Флуоресцентную спектроскопию можно комбинировать с устройствами быстрого смешивания, такими как остановился поток, для измерения кинетики сворачивания белков,[51] генерировать шеврон сюжет и получить Анализ значения Phi.
Круговой дихроизм
Круговой дихроизм является одним из самых общих и основных инструментов для изучения сворачивания белков. Круговой дихроизм спектроскопия измеряет поглощение круговой поляризованный свет. В белках такие структуры, как альфа спирали и бета-листы являются хиральными и поэтому поглощают такой свет. Поглощение этого света действует как маркер степени свернутости белкового ансамбля. Этот метод использовался для измерения установление равновесия белка, измеряя изменение этой абсорбции в зависимости от концентрации денатуранта или температура. Расплав денатуранта измеряет свободная энергия разворачивания, а также значение m белка или денатурирующая зависимость. А температура расплав измеряет температура денатурации (Tm) белка.[47] Что касается флуоресцентной спектроскопии, спектроскопию кругового дихроизма можно комбинировать с устройствами быстрого смешивания, такими как остановился поток для измерения сворачивания белка кинетика и произвести шевронные графики.
Колебательный круговой дихроизм белков
Последние разработки колебательный круговой дихроизм (VCD) для белков, в настоящее время включающие преобразование Фурье (FT) инструменты предоставляют мощные средства для определения конформации белка в растворе даже для очень больших молекул белка. Такие исследования белков VCD часто сочетаются с дифракция рентгеновских лучей кристаллов протеина, FT-IR данные для белковых растворов в тяжелой воде (D2O), или ab initio квантовые вычисления для обеспечения однозначных структурных назначений, которые невозможно получить из компакт диск.[нужна цитата ]
Спектроскопия ядерного магнитного резонанса белков
Ядерно-магнитный резонанс белков (ЯМР) позволяет собирать структурные данные белка, создавая магнитное поле через образцы концентрированного белка. В ЯМР в зависимости от химической среды определенные ядра будут поглощать определенные радиочастоты.[52][53] Поскольку структурные изменения белков происходят во временном масштабе от нс до мс, ЯМР особенно приспособлен для изучения промежуточных структур во временных масштабах от пс до с.[54] Некоторые из основных методов изучения структуры белков и структурных изменений нефолдинговых белков включают: УЮТНЫЙ, TOCSY, HSQC, Время релаксации (T1 и T2) и NOE.[52] NOE особенно полезен, поскольку наблюдается перенос намагниченности между пространственно проксимальными атомами водорода.[52]

Потому что сворачивание белка происходит примерно за 50-3000 с.−1 CPMG Релаксационная дисперсия и Химический обмен Перенос насыщения стали одними из основных методов ЯМР-анализа сворачивания.[53] Кроме того, оба метода используются для обнаружения возбужденных промежуточных состояний в ландшафте сворачивания белков.[55] Для этого CPMG Relaxation дисперсия использует преимущества Спин-эхо явление. Этот метод подвергает ядра-мишени воздействию импульса 90, за которым следует один или несколько импульсов 180.[56] Когда ядра перефокусируются, широкое распределение указывает на то, что ядра-мишени находятся в промежуточном возбужденном состоянии. Посмотрев на графики дисперсии релаксации, данные собирают информацию о термодинамике и кинетике между возбужденным и заземленным.[56][55] Saturation Transfer измеряет изменения сигнала от основного состояния, когда возбужденные состояния становятся возмущенными. Он использует слабое радиочастотное излучение для насыщения возбужденного состояния определенного ядра, которое переводит его насыщение в основное состояние.[53] Этот сигнал усиливается за счет уменьшения намагниченности (и сигнала) основного состояния.[53][55]
Основное ограничение ЯМР заключается в том, что его разрешение снижается с белками, размер которых превышает 25 кДа, и не так подробно, как Рентгеновская кристаллография.[53] Кроме того, анализ ЯМР белков довольно сложен и может предложить несколько решений из одного и того же спектра ЯМР.[52]
В исследовании, посвященном складыванию Боковой амиотрофический склероз вовлеченный белок SOD1, возбужденные интермедиаты изучались с помощью релаксационной дисперсии и переноса насыщения.[57] SOD1 ранее был связан со многими болезнетворными мутантами, которые, как предполагалось, участвовали в агрегации белков, однако механизм до сих пор был неизвестен. С помощью экспериментов по релаксационной дисперсии и переносу насыщения многие возбужденные промежуточные состояния были обнаружены неправильной сверткой у мутантов SOD1.[57]
Двойная поляризационная интерферометрия
Двойная поляризационная интерферометрия представляет собой поверхностный метод измерения оптических свойств молекулярных слоев. При использовании для характеристики сворачивания белка он измеряет конформация путем определения общего размера монослоя белка и его плотности в реальном времени с разрешением ниже Ангстрема,[58] хотя измерение кинетики сворачивания белка в реальном времени ограничено процессами, которые происходят медленнее, чем ~ 10 Гц. Похожий на круговой дихроизм стимулом к сворачиванию может быть денатурант или температура.
Исследования складчатости с высоким временным разрешением
В последние годы изучение сворачивания белков значительно продвинулось благодаря развитию быстрых методов с временным разрешением. Экспериментаторы быстро запускают сворачивание образца развернутого белка и наблюдают за результатом. динамика. Используемые быстрые методы включают: рассеяние нейтронов,[59] сверхбыстрое перемешивание растворов, фотохимические методы и лазерная спектроскопия скачков температуры. Среди многих ученых, которые внесли свой вклад в разработку этих методов, - Джереми Кук, Генрих Родер, Гарри Грей, Мартин Грюбеле, Брайан Дайер, Уильям Итон, Шина Рэдфорд, Крис Добсон, Алан Фершт, Бенгт Нёльтинг и Ларс Конерманн.
Протеолиз
Протеолиз обычно используется для исследования фракции, развернутой в широком диапазоне условий раствора (например, Быстрый параллельный протеолиз (FASTpp).[60][61]
Силовая спектроскопия одиночных молекул
Методы одиночных молекул, такие как оптический пинцет и АСМ, были использованы для понимания механизмов сворачивания белков как изолированных белков, так и белков с шаперонами.[62] Оптический пинцет были использованы для вытягивания отдельных белковых молекул с их C- и N-концов и их разворачивания, чтобы изучить последующую рефолдинг.[63] Этот метод позволяет измерять скорость сворачивания на уровне одной молекулы; например, оптический пинцет недавно был применен для изучения сворачивания и разворачивания белков, участвующих в свертывании крови. фактор фон Виллебранда (vWF) - это белок, играющий важную роль в процессе образования тромбов. С помощью оптического пинцета для измерения одиночных молекул было обнаружено, что связанный с кальцием vWF действует как датчик силы сдвига в крови. Сдвигающая сила приводит к разворачиванию домена A2 vWF, скорость рефолдинга которого резко увеличивается в присутствии кальция.[64] Недавно было также показано, что простой домен src SH3 получает доступ к множественным путям развертывания под действием силы.[65]
Биотиновая окраска
Биотиновая окраска позволяет делать снимки (не) свернутых белков в зависимости от состояния клеток. Биотиновая "живопись" демонстрирует предвзятость предсказанного Внутренне неупорядоченные белки.[66]
Вычислительные исследования сворачивания белков
Вычислительные исследования сворачивания белка включают три основных аспекта, связанных с предсказанием стабильности, кинетики и структуры белка. В недавнем обзоре обобщены доступные вычислительные методы фолдинга белков. [67]
Парадокс Левинталя
В 1969 году Сайрус Левинталь заметил, что из-за очень большого количества степеней свободы в развернутой полипептидной цепи молекула имеет астрономическое количество возможных конформаций. Оценка 3300 или 10143 было сделано в одной из его бумаг.[68] Парадокс Левинталя - мысленный эксперимент, основанный на наблюдении, что если бы белок был свернут путем последовательной выборки всех возможных конформаций, для этого потребовалось бы астрономическое количество времени, даже если бы конформации отбирались с большой скоростью (на наносекунда или пикосекунда масштаб).[69] Основываясь на наблюдении, что белки сворачиваются намного быстрее, чем это, Левинталь затем предположил, что случайного конформационного поиска не происходит, и, следовательно, белок должен сворачиваться через серию метастабильных промежуточные состояния.
Энергетический ландшафт сворачивания белков
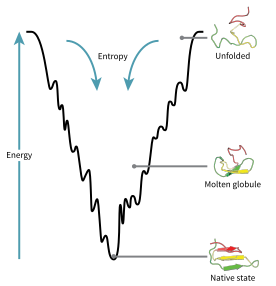
В конфигурационное пространство белка во время сворачивания можно представить как энергетический ландшафт. По мнению Джозефа Брюнгельсона и Питер Волайнс, белки следуют принцип минимального разочарования это означает, что естественно эволюционирующие белки оптимизировали свои энергетические ландшафты сворачивания[70] и что природа выбрала аминокислотные последовательности так, чтобы сложенное состояние белка было достаточно стабильным. Кроме того, приобретение сложенного состояния должно было стать достаточно быстрым процессом. Хотя природа снизила уровень разочарование в белках некоторая его степень сохраняется до сих пор, что можно наблюдать при наличии локальных минимумов в энергетическом ландшафте белков.
Следствием этих эволюционно выбранных последовательностей является то, что обычно считается, что белки имеют глобально «направляемые энергетические ландшафты» (придуманные Хосе Онучич )[71] которые в значительной степени направлены на родное государство. Эта "складная воронка «ландшафт позволяет белку сворачиваться до нативного состояния посредством любого из большого количества путей и промежуточных продуктов, а не ограничиваться одним механизмом. Теория поддерживается обоими компьютерное моделирование модельных белков и экспериментальные исследования,[70] и он был использован для улучшения методов предсказание структуры белка и дизайн.[70] Описание сворачивания белков с помощью выравнивающего ландшафта свободной энергии также согласуется со 2-м законом термодинамики.[72] С физической точки зрения представление о ландшафтах с точки зрения визуализируемого потенциала или поверхностей полной энергии просто с максимумами, седловыми точками, минимумами и воронками, как географические ландшафты, возможно, немного вводит в заблуждение. Соответствующее описание - это действительно многомерное фазовое пространство, в котором многообразия могут принимать множество более сложных топологических форм.[73]
Развернутая полипептидная цепь начинается на вершине воронки, где она может принимать наибольшее количество развернутых вариаций и находится в своем наивысшем энергетическом состоянии. Подобные энергетические ландшафты указывают на то, что существует большое количество начальных возможностей, но возможно только одно естественное состояние; однако он не показывает многочисленных возможных путей сворачивания. Другая молекула одного и того же конкретного белка может быть способна следовать незначительно разным путям сворачивания в поисках разных более низкоэнергетических промежуточных продуктов, если достигается та же самая нативная структура.[74] Различные пути могут иметь разную частоту использования в зависимости от термодинамической благоприятности каждого пути. Это означает, что если один путь окажется более термодинамически более благоприятным, чем другой, он, вероятно, будет чаще использоваться для поиска нативной структуры.[74] Когда белок начинает сворачиваться и принимать различные формы, он всегда ищет более термодинамически благоприятную структуру, чем раньше, и, таким образом, продолжает движение по энергетической воронке. Образование вторичных структур является убедительным признаком повышенной стабильности в белке, и только одна комбинация вторичных структур, предполагаемая основной цепью полипептида, будет иметь самую низкую энергию и, следовательно, будет присутствовать в нативном состоянии белка.[74] Среди первых структур, которые образуются после того, как полипептид начинает складываться, являются альфа-спирали и бета-витки, где альфа-спирали могут формироваться всего за 100 наносекунд, а бета-повороты - за 1 микросекунду.[28]
В ландшафте энергетической воронки существует седловая точка, в которой находится переходное состояние для конкретного белка.[28] Переходное состояние на диаграмме энергетической воронки - это конформация, которую должна принять каждая молекула этого белка, если белок желает, наконец, принять нативную структуру. Ни один белок не может принимать нативную структуру, не пройдя сначала через переходное состояние.[28] Переходное состояние можно назвать вариантом или преждевременной формой исходного состояния, а не просто еще одним промежуточным этапом.[75] Показано, что сворачивание переходного состояния определяет скорость, и даже несмотря на то, что оно существует в состоянии с более высокой энергией, чем естественная складка, оно очень похоже на естественную структуру. В переходном состоянии существует ядро, вокруг которого белок может сворачиваться, образованное процессом, называемым «конденсация зародышей», когда структура начинает схлопываться на ядро.[75]
Моделирование сворачивания белков

De novo или ab initio методы вычислительной предсказание структуры белка связаны с экспериментальными исследованиями фолдинга белков, но строго отличаются от них. Молекулярная динамика (MD) - важный инструмент для изучения сворачивания и динамики белков. in silico.[76] Первое моделирование равновесного складывания проводилось с использованием неявной модели растворителя и зонтичный отбор проб.[77] Из-за вычислительных затрат моделирование сворачивания ab initio MD с явной водой ограничено пептидами и очень маленькими белками.[78][79] МД моделирование более крупных белков остается ограниченным динамикой экспериментальной структуры или ее высокотемпературным развертыванием. К долгосрочным процессам сворачивания (более 1 миллисекунды), таким как сворачивание белков небольшого размера (около 50 остатков) или больше, можно получить доступ, используя крупнозернистые модели.[80][81][82]
100-петафлоп распределенных вычислений проект Складной @ дома созданный группой Виджая Панде в Стэндфордский Университет имитирует сворачивание белка, используя время простоя обработки Процессоры и GPU персональных компьютеров от волонтеров. Проект направлен на изучение неправильного сворачивания белков и ускорение разработки лекарств для исследования болезней.
Моделирование продолжительной непрерывной траектории было выполнено на Антон суперкомпьютер с массовым параллелизмом, спроектированный и построенный на ASIC и соединяет D. E. Shaw Research. Самый длинный опубликованный результат моделирования, выполненного с использованием Антона, - это моделирование NTL9 за 2,936 миллисекунды при 355 К.[83]
В последние годы произошли значительные улучшения в прогнозировании структуры за счет глубокое обучение искусственный интеллект (AI) подходит. В ноябре 2020 года ученые, связанные с компанией DeepMind сообщили, что их программное обеспечение ИИ AlphaFold решил ежегодный CASP проблема предсказания структуры с такой точностью, что другие ученые описали результаты как «трансформационные» и «возможно решающие» основную проблему предсказания структуры.[84]
Смотрите также
- Антон (компьютер)
- Шеврон сюжет
- Средняя точка денатурации
- Складывание под гору
- Складывание (химия)
- Складной @ Home
- Сложите его компьютерная игра
- Потенциальная энергия белка
- Pt-ствол
- Белковая динамика
- Циклическая амплификация с неправильным сворачиванием белков
- Программное обеспечение для предсказания структуры белка
- Протеопатия
- Rosetta @ home
- Программное обеспечение для моделирования молекулярной механики
- Статистический потенциал
- Масс-спектрометрия с временным разрешением
использованная литература
- ^ Альбертс Б, Джонсон А., Льюис Дж, Рафф М., Робертс К., Уолтерс П. (2002). «Форма и структура белков». Молекулярная биология клетки; Четвертый выпуск. Нью-Йорк и Лондон: Наука о гирляндах. ISBN 978-0-8153-3218-3.
- ^ Анфинсен CB (июль 1972 г.). «Формирование и стабилизация структуры белка». Биохимический журнал. 128 (4): 737–49. Дои:10.1042 / bj1280737. ЧВК 1173893. PMID 4565129.
- ^ Берг Ю.М., Тимочко Ю.Л., Страйер Л (2002). «3. Структура и функции белка». Биохимия. Сан-Франциско: В. Х. Фриман. ISBN 978-0-7167-4684-3.
- ^ а б Selkoe DJ (декабрь 2003 г.). «Фатальное сворачивание белков». Природа. 426 (6968): 900–4. Bibcode:2003Натура 426..900С. Дои:10.1038 / природа02264. PMID 14685251. S2CID 6451881.
- ^ Альбертс Б., Брэй Д., Хопкин К., Джонсон А., Льюис Дж., Рафф М., Робертс К., Уолтер П. (2010). «Структура и функции белка». Основная клеточная биология (Третье изд.). Нью-Йорк, Нью-Йорк: Наука о гирляндах. С. 120–70. ISBN 978-0-8153-4454-4.
- ^ Ким PS, Болдуин RL (1990). «Промежуточные звенья в реакциях сворачивания малых белков». Ежегодный обзор биохимии. 59: 631–60. Дои:10.1146 / annurev.bi.59.070190.003215. PMID 2197986.
- ^ Джексон С.Е. (1998). «Как складываются небольшие однодоменные белки?». Складывание и дизайн. 3 (4): Р81-91. Дои:10.1016 / S1359-0278 (98) 00033-9. PMID 9710577.
- ^ Кубелка Дж., Хофрихтер Дж., Итон В.А. (февраль 2004 г.). Ограничение скорости "сворачивания белка"'". Текущее мнение в структурной биологии. 14 (1): 76–88. Дои:10.1016 / j.sbi.2004.01.013. PMID 15102453.
- ^ Анфинсен CB (июль 1973 г.). «Принципы складывания белковых цепей». Наука. 181 (4096): 223–30. Bibcode:1973Sci ... 181..223A. Дои:10.1126 / science.181.4096.223. PMID 4124164.
- ^ а б c d е ж г час Воет Д., Воет Дж. Г., Пратт С. В. (2016). Принципы биохимии (Пятое изд.). Вайли. ISBN 978-1-118-91840-1.
- ^ Александр PA, He Y, Chen Y, Orban J, Bryan PN (июль 2007 г.). «Дизайн и характеристика двух белков с 88% идентичностью последовательностей, но различной структурой и функцией». Труды Национальной академии наук Соединенных Штатов Америки. 104 (29): 11963–8. Bibcode:2007ПНАС..10411963А. Дои:10.1073 / pnas.0700922104. ЧВК 1906725. PMID 17609385.
- ^ Роуз Дж. Д., Флеминг П. Дж., Банавар Дж. Р., Маритан А. (ноябрь 2006 г.). «Основанная на позвоночнике теория сворачивания белка». Труды Национальной академии наук Соединенных Штатов Америки. 103 (45): 16623–33. Bibcode:2006PNAS..10316623R. CiteSeerX 10.1.1.630.5487. Дои:10.1073 / pnas.0606843103. ЧВК 1636505. PMID 17075053.
- ^ а б c Фершт А (1999). Структура и механизм в науке о белках: руководство по ферментативному катализу и сворачиванию белков. Макмиллан. ISBN 978-0-7167-3268-6.
- ^ «Структура белка». Scitable. Природное образование. Получено 2016-11-26.
- ^ Пратт К., Корнели К. (2004). "Термодинамика". Основная биохимия. Вайли. ISBN 978-0-471-39387-0. Получено 2016-11-26.
- ^ Чжан Г, Игнатова З. (февраль 2011 г.). «Сворачивание при рождении зарождающейся цепи: координирующий перевод с ко-трансляционным сворачиванием». Текущее мнение в структурной биологии. 21 (1): 25–31. Дои:10.1016 / j.sbi.2010.10.008. PMID 21111607.
- ^ ван ден Берг Б., Уэйн Р., Добсон С. М., Эллис Р. Дж. (август 2000 г.). «Макромолекулярное скопление нарушает кинетику рефолдинга белка: последствия для сворачивания внутри клетки». Журнал EMBO. 19 (15): 3870–5. Дои:10.1093 / emboj / 19.15.3870. ЧВК 306593. PMID 10921869.
- ^ Аль-Карадаги С. «Торсионные углы и график Рамахнадрана в белковых структурах». www.proteinstructures.com. Получено 2016-11-26.
- ^ Пейс К.Н., Ширли Б.А., Макнатт М., Гадживала К. (январь 1996 г.). «Силы, способствующие конформационной стабильности белков». Журнал FASEB. 10 (1): 75–83. Дои:10.1096 / fasebj.10.1.8566551. PMID 8566551.
- ^ Цуй Д., Оу С., Патель С. (декабрь 2014 г.). «Водные сети, покрывающие белок, и значение для предсказания белок-белковых взаимодействий, опосредованных гидрофобными эффектами». Белки. 82 (12): 3312–26. Дои:10.1002 / prot.24683. PMID 25204743.
- ^ Танфорд С. (июнь 1978 г.). «Гидрофобный эффект и организация живого вещества». Наука. 200 (4345): 1012–8. Bibcode:1978Научный ... 200.1012Т. Дои:10.1126 / science.653353. PMID 653353.
- ^ Дичонгкит С., Нгуен Х., Пауэрс Е.Т., Доусон П.Е., Грюбеле М., Келли Дж. В. (июль 2004 г.). «Контекстно-зависимые вклады водородной связи основной цепи в энергетику складывания бета-листов». Природа. 430 (6995): 101–5. Bibcode:2004Натура430..101Д. Дои:10.1038 / природа02611. PMID 15229605. S2CID 4315026.
- ^ Ирбек А., Санделин Е. (ноябрь 2000 г.). «О соотношении гидрофобности в белковых цепях». Биофизический журнал. 79 (5): 2252–8. arXiv:cond-mat / 0010390. Bibcode:2000 баррелей в день .... 79.2252I. Дои:10.1016 / S0006-3495 (00) 76472-1. ЧВК 1301114. PMID 11053106.
- ^ Ирбек А., Петерсон С., Поттхаст Ф. (сентябрь 1996 г.). «Доказательства неслучайной гидрофобности структур в белковых цепях». Труды Национальной академии наук Соединенных Штатов Америки. 93 (18): 9533–8. arXiv:хим-ph / 9512004. Bibcode:1996PNAS ... 93.9533I. Дои:10.1073 / пнас.93.18.9533. ЧВК 38463. PMID 8790365.
- ^ Уилсон Б.А., Фой С.Г., Неме Р., Масел Дж. (Июнь 2017 г.). "Рождение Де Ново Джин". Природа, экология и эволюция. 1 (6): 0146–146. Дои:10.1038 / s41559-017-0146. ЧВК 5476217. PMID 28642936.
- ^ Уиллис С., Масел Дж. (Сентябрь 2018 г.). «Рождение гена способствует структурному нарушению, кодируемому перекрывающимися генами». Генетика. 210 (1): 303–313. Дои:10.1534 / генетика.118.301249. ЧВК 6116962. PMID 30026186.
- ^ Фой С.Г., Уилсон Б.А., Бертрам Дж., Кордес М.Х., Масел Дж. (Апрель 2019 г.). «Сдвиг в стратегии предотвращения агрегации указывает на долгосрочное направление эволюции белков». Генетика. 211 (4): 1345–1355. Дои:10.1534 / генетика.118.301719. ЧВК 6456324. PMID 30692195.
- ^ а б c d е ж Добсон CM (декабрь 2003 г.). «Сворачивание и неправильная сворачивание белков». Природа. 426 (6968): 884–90. Bibcode:2003Натура.426..884D. Дои:10.1038 / природа02261. PMID 14685248. S2CID 1036192.
- ^ а б c Hartl FU (июнь 1996 г.). «Молекулярные шапероны в сворачивании клеточного белка». Природа. 381 (6583): 571–9. Bibcode:1996Натура.381..571H. Дои:10.1038 / 381571a0. PMID 8637592. S2CID 4347271.
- ^ а б Hartl FU, Bracher A, Hayer-Hartl M (июль 2011 г.). «Молекулярные шапероны в сворачивании белков и протеостазе». Природа. 475 (7356): 324–32. Дои:10.1038 / природа10317. PMID 21776078. S2CID 4337671.
- ^ Ким Й.Е., Хипп М.С., Брахер А., Хейер-Хартл М., Хартл Ф.У. (2013). «Молекулярные функции шаперона в сворачивании белков и протеостазе». Ежегодный обзор биохимии. 82: 323–55. Дои:10.1146 / annurev-biochem-060208-092442. PMID 23746257.
- ^ Shortle D (январь 1996 г.). «Денатурированное состояние (другая половина уравнения сворачивания) и его роль в стабильности белка». Журнал FASEB. 10 (1): 27–34. Дои:10.1096 / fasebj.10.1.8566543. PMID 8566543.
- ^ Ли С., Цай FT (2005). «Молекулярные шапероны в контроле качества белков». Журнал биохимии и молекулярной биологии. 38 (3): 259–65. Дои:10.5483 / BMBRep.2005.38.3.259. PMID 15943899.
- ^ Охеда-Май П., Гарсия М.Э. (июль 2010 г.). «Нарушение конформации нативного белка бета-листа под действием электрического поля и создание спиральной структуры». Биофизический журнал. 99 (2): 595–9. Bibcode:2010BpJ .... 99..595O. Дои:10.1016 / j.bpj.2010.04.040. ЧВК 2905109. PMID 20643079.
- ^ ван ден Берг Б., Эллис Р. Дж., Добсон К. М. (декабрь 1999 г.). «Влияние макромолекулярного краудинга на сворачивание и агрегацию белков». Журнал EMBO. 18 (24): 6927–33. Дои:10.1093 / emboj / 18.24.6927. ЧВК 1171756. PMID 10601015.
- ^ Эллис Р.Дж. (июль 2006 г.). «Молекулярные шапероны: помощь сборке в дополнение к складыванию». Тенденции в биохимических науках. 31 (7): 395–401. Дои:10.1016 / j.tibs.2006.05.001. PMID 16716593.
- ^ Такай К., Накамура К., Токи Т., Цуногай У, Миядзаки М., Миядзаки Дж., Хираяма Х., Накагава С., Нуноура Т., Хорикоши К. (август 2008 г.). «Клеточная пролиферация при 122 градусах Цельсия и производство изотопно тяжелого CH4 гипертермофильным метаногеном при культивировании под высоким давлением». Труды Национальной академии наук Соединенных Штатов Америки. 105 (31): 10949–54. Bibcode:2008ПНАС..10510949Т. Дои:10.1073 / pnas.0712334105. ЧВК 2490668. PMID 18664583.
- ^ а б Марусич Е.И., Курочкина Л.П., Месянжинов В.В. Шапероны в сборке бактериофага Т4. Биохимия (Москва). 1998; 63 (4): 399-406.
- ^ а б c d Чаудхури Т.К., Пол С. (апрель 2006 г.). «Заболевания, связанные с неправильной упаковкой белков, и терапевтические подходы на основе шаперонов». Журнал FEBS. 273 (7): 1331–49. Дои:10.1111 / j.1742-4658.2006.05181.x. PMID 16689923.
- ^ а б Soto C, Estrada L, Castilla J (март 2006 г.). «Амилоиды, прионы и присущая им инфекционная природа неправильно свернутых белковых агрегатов». Тенденции в биохимических науках. 31 (3): 150–5. Дои:10.1016 / j.tibs.2006.01.002. PMID 16473510.
- ^ Хаммарстрём П., Вайзман Р.Л., Пауэрс Э.Т., Келли Д.В. (январь 2003 г.). «Профилактика транстиретин-амилоидной болезни путем изменения энергетики неправильного свертывания белков». Наука. 299 (5607): 713–6. Bibcode:2003Наука ... 299..713H. Дои:10.1126 / science.1079589. PMID 12560553. S2CID 30829998.
- ^ Чити Ф, Добсон CM (2006). «Неправильная упаковка белка, функциональный амилоид и болезнь человека». Ежегодный обзор биохимии. 75: 333–66. Дои:10.1146 / annurev.biochem.75.101304.123901. PMID 16756495.
- ^ Джонсон С.М., Вайзман Р.Л., Секидзима Ю., Грин Н.С., Адамски-Вернер С.Л., Келли Дж. В. (декабрь 2005 г.). «Кинетическая стабилизация в естественном состоянии как стратегия для облегчения заболеваний, связанных с неправильной упаковкой белков: основное внимание уделяется транстиретин-амилоидозам». Отчеты о химических исследованиях. 38 (12): 911–21. Дои:10.1021 / ar020073i. PMID 16359163.
- ^ а б Каутан К. (2001). «Фазовая проблема в рентгеновской кристаллографии и ее решение». (PDF). Энциклопедия наук о жизни. Macmillan Publishers Ltd, Nature Publishing Group. Получено 3 ноября, 2016.
- ^ Дрент Дж (2007-04-05). Принципы рентгеновской кристаллографии белков. Springer Science & Business Media. ISBN 978-0-387-33746-3.
- ^ Тейлор Дж. (2003). «Фазовая проблема». Acta Crystallographica Раздел D. 59 (11): 1881–90. Дои:10.1107 / S0907444903017815. PMID 14573942.
- ^ а б c Bedouelle H (февраль 2016 г.). «Принципы и уравнения для измерения и интерпретации стабильности белка: от мономера до тетрамера». Биохимия. 121: 29–37. Дои:10.1016 / j.biochi.2015.11.013. PMID 26607240.
- ^ Monsellier E, Bedouelle H (сентябрь 2005 г.). «Количественное измерение стабильности белка по развертывающемуся равновесию, контролируемому с максимальной длиной волны флуоресценции». Белковая инженерия, дизайн и выбор. 18 (9): 445–56. Дои:10.1093 / белок / gzi046. PMID 16087653.
- ^ Park YC, Bedouelle H (июль 1998 г.). «Димерная тирозил-тРНК синтетаза из Bacillus stearothermophilus разворачивается через мономерное промежуточное соединение. Количественный анализ в условиях равновесия». Журнал биологической химии. 273 (29): 18052–9. Дои:10.1074 / jbc.273.29.18052. PMID 9660761.
- ^ Ульд-Абей М.Б., Пети-Топен I, Зидан Н., барон Б., Бедуель Н. (июнь 2012 г.). «Множественные состояния сворачивания и нарушение рибосомного белка SA, мембранного рецептора ламинина, антиканцерогенов и патогенов». Биохимия. 51 (24): 4807–21. Дои:10.1021 / bi300335r. PMID 22640394.
- ^ Royer CA (май 2006 г.). «Исследование сворачивания белков и конформационных переходов с помощью флуоресценции». Химические обзоры. 106 (5): 1769–84. Дои:10.1021 / cr0404390. PMID 16683754.
- ^ а б c d Вютрих К. (декабрь 1990 г.). «Определение структуры белка в растворе методом ЯМР-спектроскопии».. Журнал биологической химии. 265 (36): 22059–62. PMID 2266107.
- ^ а б c d е Журавлева А, Коржнев Д.М. (май 2017 г.). «Фолдинг белка с помощью ЯМР». Прогресс в спектроскопии ядерного магнитного резонанса. 100: 52–77. Дои:10.1016 / j.pnmrs.2016.10.002. PMID 28552172.
- ^ Ортега Г., Понс М., Миллет О. (01.01.2013). Карабенчева-Христова Т (ред.). «Функциональная динамика белков в различных временных масштабах, как изучено с помощью ЯМР-спектроскопии». Достижения в химии белков и структурной биологии. Динамика белков и нуклеиновых кислот. Академическая пресса. 92: 219–51. Дои:10.1016 / b978-0-12-411636-8.00006-7. PMID 23954103.
- ^ а б c Валлурупалли П., Бувиньи Г., Кей Л. Е. (май 2012 г.). «Изучение« невидимых »возбужденных состояний белка при медленном обмене с конформацией основного состояния». Журнал Американского химического общества. 134 (19): 8148–61. Дои:10.1021 / ja3001419. PMID 22554188.
- ^ а б Neudecker P, Lundström P, Kay LE (март 2009 г.). «Релаксационная дисперсионная ЯМР-спектроскопия как инструмент детального изучения сворачивания белков». Биофизический журнал. 96 (6): 2045–54. Дои:10.1016 / j.bpj.2008.12.3907. ЧВК 2717354. PMID 19289032.
- ^ а б Сехар А., Рамфельдт Дж. А., Broom HR, Дойл С. М., Соберинг Р. Е., Мейеринг Е. М., Кей Л. Е. (ноябрь 2016 г.). «Исследование свободных энергетических ландшафтов мутантов болезни ALS SOD1 с помощью ЯМР-спектроскопии». Труды Национальной академии наук Соединенных Штатов Америки. 113 (45): E6939 – E6945. Дои:10.1073 / pnas.1611418113. ЧВК 5111666. PMID 27791136.
- ^ Кросс Г. Х., Фриман, штат Нью-Джерси, Суонн, М. Дж. (2008). "Двойная поляризационная интерферометрия: оптический метод в реальном времени для измерения (био) молекулярной ориентации, структуры и функций на границе твердое тело / жидкость". Справочник по биосенсорам и биочипам. Дои:10.1002 / 9780470061565.hbb055. ISBN 978-0-470-01905-4.
- ^ Bu Z, Cook J, Callaway DJ (сентябрь 2001 г.). «Динамические режимы и коррелированная структурная динамика в нативном и денатурированном альфа-лактальбумине». Журнал молекулярной биологии. 312 (4): 865–73. Дои:10.1006 / jmbi.2001.5006. PMID 11575938.
- ^ Минде Д.П., Морис М.М., Рюдигер С.Г. (2012). «Определение биофизической стабильности белков в лизатах с помощью анализа быстрого протеолиза, FASTpp». PLOS ONE. 7 (10): e46147. Bibcode:2012PLoSO ... 746147M. Дои:10.1371 / journal.pone.0046147. ЧВК 3463568. PMID 23056252.
- ^ Парк C, Marqusee S (март 2005 г.). «Импульсный протеолиз: простой метод количественного определения стабильности белка и связывания лиганда». Методы природы. 2 (3): 207–12. Дои:10.1038 / nmeth740. PMID 15782190. S2CID 21364478.
- ^ Машаги А., Крамер Дж., Лэмб, округ Колумбия, депутат Майер, Танс С.Дж. (январь 2014 г.). «Действие шаперона на уровне одной молекулы». Химические обзоры. 114 (1): 660–76. Дои:10.1021 / cr400326k. PMID 24001118.
- ^ Джаганнатан Б., Маркиз С. (ноябрь 2013 г.). «Сворачивание и разворачивание белка под действием силы». Биополимеры. 99 (11): 860–9. Дои:10.1002 / bip.22321. ЧВК 4065244. PMID 23784721.
- ^ Якоби А.Дж., Машаги А., Танс С.Дж., Хейзинга Э.Г. (июль 2011 г.). «Кальций модулирует чувствительность к силе доменом фактора фон Виллебранда А2». Nature Communications. 2: 385. Bibcode:2011НатКо ... 2..385J. Дои:10.1038 / ncomms1385. ЧВК 3144584. PMID 21750539.
- ^ Джаганнатан Б., Элмс П.Дж., Бустаманте С., Марки С. (октябрь 2012 г.). «Прямое наблюдение индуцированного силой переключения в анизотропном механическом пути разворачивания белка». Труды Национальной академии наук Соединенных Штатов Америки. 109 (44): 17820–5. Bibcode:2012PNAS..10917820J. Дои:10.1073 / pnas.1201800109. ЧВК 3497811. PMID 22949695.
- ^ Минде Д.П., Рамакришна М, Лилли К.С. (2018). «Биотинилирование с помощью бесконтактной метки благоприятствует развернутым белкам». bioRxiv. Дои:10.1101/274761.
- ^ Compiani M, Capriotti E (декабрь 2013 г.). «Вычислительные и теоретические методы фолдинга белков». Биохимия. 52 (48): 8601–24. Дои:10.1021 / bi4001529. PMID 24187909.
- ^ «Структурная биохимия / Белки / Сворачивание белков - Викиучебники, открытые книги для открытого мира». en.wikibooks.org. Получено 2016-11-05.
- ^ Левинталь C (1968). "Есть ли пути для сворачивания белков?" (PDF). Journal de Chimie Physique et de Physico-Chimie Biologique. 65: 44–45. Bibcode:1968JCP .... 65 ... 44L. Дои:10.1051 / jcp / 1968650044. Архивировано из оригинал (PDF) на 2009-09-02.
- ^ а б c Брингельсон Дж. Д., Онучич Дж. Н., Соци Н. Д., Волинс П. Г. (март 1995 г.). «Воронки, пути и энергетический ландшафт сворачивания белка: синтез». Белки. 21 (3): 167–95. arXiv:хим-ph / 9411008. Дои:10.1002 / prot.340210302. PMID 7784423. S2CID 13838095.
- ^ Леопольд PE, Монталь М, Онучич Ю.Н. (Сентябрь 1992 г.). "Белковые воронки сворачивания: кинетический подход к взаимосвязи" последовательность-структура ". Труды Национальной академии наук Соединенных Штатов Америки. 89 (18): 8721–5. Bibcode:1992PNAS ... 89.8721L. Дои:10.1073 / пнас.89.18.8721. ЧВК 49992. PMID 1528885.
- ^ Шарма В., Кайла В.Р., Аннила А. (2009). «Сворачивание белков как эволюционный процесс». Physica A: Статистическая механика и ее приложения. 388 (6): 851–62. Bibcode:2009PhyA..388..851S. Дои:10.1016 / j.physa.2008.12.004.
- ^ Робсон Б., Вайтилингам А. (2008). «Возвращение к сворачиванию белков». Молекулярная биология сворачивания белков, часть B. Прогресс в молекулярной биологии и трансляционной науке. 84. С. 161–202. Дои:10.1016 / S0079-6603 (08) 00405-4. ISBN 978-0-12-374595-8. PMID 19121702.
- ^ а б c Дилл К.А., МакКаллум Дж.Л. (ноябрь 2012 г.). «Проблема сворачивания белка, 50 лет спустя». Наука. 338 (6110): 1042–6. Bibcode:2012Sci ... 338.1042D. Дои:10.1126 / science.1219021. PMID 23180855. S2CID 5756068.
- ^ а б Фершт А.Р. (февраль 2000 г.). «Структура переходного состояния как объединяющая основа в механизмах сворачивания белков: порядок контактов, топология цепи, стабильность и механизм расширенного ядра». Труды Национальной академии наук Соединенных Штатов Америки. 97 (4): 1525–9. Bibcode:2000PNAS ... 97.1525F. Дои:10.1073 / пнас.97.4.1525. ЧВК 26468. PMID 10677494.
- ^ Риццути Б., Даггетт В. (март 2013 г.). «Использование моделирования для создания основы для экспериментальных исследований сворачивания белков». Архивы биохимии и биофизики. 531 (1–2): 128–35. Дои:10.1016 / j.abb.2012.12.015. ЧВК 4084838. PMID 23266569.
- ^ Шефер М., Бартельс С., Карплюс М. (декабрь 1998 г.). «Конформации раствора и термодинамика структурированных пептидов: моделирование молекулярной динамики с неявной моделью сольватации». Журнал молекулярной биологии. 284 (3): 835–48. Дои:10.1006 / jmbi.1998.2172. PMID 9826519.
- ^ Джонс Д. «Моделирование сворачивания белков на основе фрагментов». Университетский колледж Лондона.
- ^ «Сворачивание белков» (по молекулярной динамике).
- ^ Kmiecik S, Gront D, Kolinski M, Wieteska L, Dawid AE, Kolinski A (июль 2016 г.). «Крупнозернистые модели белков и их применение». Химические обзоры. 116 (14): 7898–936. Дои:10.1021 / acs.chemrev.6b00163. PMID 27333362.
- ^ Kmiecik S, Kolinski A (июль 2007 г.). «Характеристика путей сворачивания белков с помощью моделирования в ограниченном пространстве». Труды Национальной академии наук Соединенных Штатов Америки. 104 (30): 12330–5. Bibcode:2007ПНАС..10412330К. Дои:10.1073 / pnas.0702265104. ЧВК 1941469. PMID 17636132.
- ^ Адхикари А.Н., Фрид К.Ф., Сосник Т.Р. (октябрь 2012 г.). «De novo предсказание путей и структуры сворачивания белков с использованием принципа последовательной стабилизации». Труды Национальной академии наук Соединенных Штатов Америки. 109 (43): 17442–7. Bibcode:2012PNAS..10917442A. Дои:10.1073 / pnas.1209000109. ЧВК 3491489. PMID 23045636.
- ^ Линдорф-Ларсен К., Пиана С., Дрор Р.О., Шоу Д.Е. (октябрь 2011 г.). «Как складываются быстро сворачивающиеся белки». Наука. 334 (6055): 517–20. Bibcode:2011Наука ... 334..517Л. Дои:10.1126 / science.1208351. PMID 22034434. S2CID 27988268.
- ^ Callaway E (ноябрь 2020 г.). "'Это изменит все »: ИИ DeepMind совершает гигантский скачок в решении белковых структур». Природа. Дои:10.1038 / d41586-020-03348-4. PMID 33257889 Проверьте
| pmid =ценность (Помогите).


