HSPA8 - HSPA8
Тепловой шок, 70 кДа, белок 8 также известный как родственный белок теплового шока 71 кДа или же Hsc70 или же Hsp73 это белок теплового шока что у людей кодируется HSPA8 ген на хромосоме 11.[5] Являясь членом семейства белков теплового шока 70 и белком-шапероном, он способствует правильному сворачиванию вновь транслированных и неправильно свернутых белков, а также стабилизирует или разрушает мутантные белки.[5][6] Его функции вносят вклад в биологические процессы, в том числе преобразование сигнала, апоптоз, аутофагия, белковый гомеостаз и рост клеток и дифференциация.[6][7][8] Это было связано с большим количеством раки, нейродегенеративные заболевания, клетка старение, и старение.[6][7]
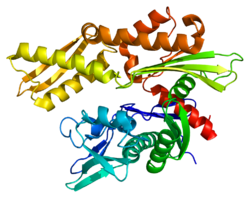
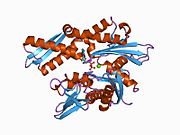
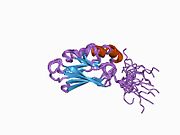
Структура
Этот ген кодирует белок теплового шока 70 кДа, который является членом семейства белков теплового шока 70 (Hsp70).[5] Как белок Hsp70, он имеет C-терминал белковый субстрат-связывающий домен и N-концевой АТФ -связывающий домен.[9][10][11] Субдомен-связывающий домен состоит из двух субдоменов, двухслойного субдомена β-сэндвича (SBDβ) и α-спирального субдомена (SBDα), которые соединены петлей Lα, β. SBDβ содержит карман для связывания пептида, тогда как SBDα служит крышкой, закрывающей щель для связывания субстрата. Связывающий домен АТФ состоит из четырех субдоменов, разделенных на две доли центральным карманом связывания АТФ / АДФ. Два концевых домена связаны между собой консервативной областью, называемой петлей LL, 1, которая имеет решающее значение для аллостерическая регуляция. Неструктурированная область в самом конце C-терминала считается местом стыковки для ко-шапероны.[11]
Функция
Белок теплового шока 70 (Hsp70 ) семейство содержит как индуцируемые теплом, так и конститутивно экспрессируемые члены. Последние называются родственными белками теплового шока (Hsc). Белок 8 теплового шока 70 кДа, также известный как Hsc70, принадлежит к подгруппе родственных тепловому шоку. Этот белок связывается с растущими полипептидами для облегчения правильного сворачивание белка.[5] Чтобы правильно сворачивать ненативные белки, шапероны Hsp70 взаимодействуют с гидрофобными пептидными сегментами белков АТФ-контролируемым образом. Хотя точный механизм до сих пор остается неясным, существует по крайней мере два альтернативных способа действия: кинетическое разделение и локальное развертывание. При кинетическом разделении Hsp70 повторно связываются и высвобождают субстраты в циклах, которые поддерживают низкие концентрации свободного субстрата. Это эффективно предотвращает агрегацию, позволяя свободным молекулам сворачиваться до нативного состояния. При локальном разворачивании циклы связывания и высвобождения вызывают локальное разворачивание в субстрате, что помогает преодолеть кинетические барьеры для сворачивания в нативное состояние. В конечном счете, его роль в сворачивании белка способствует его функции в передаче сигнала, апоптозу, гомеостазу белка, а также росту и дифференцировке клеток.[6][7] Известно, что Hsc70 локализуется в цитоплазма и лизосома, где он участвует в опосредованном шапероном аутофагия способствуя разворачиванию и перемещению субстратных белков через мембрану в лизосомные просвет.[12][13] Посредством этого пути Hsc70 также способствует деградации проапоптотических BBC3 / PUMA в нормальных условиях, обеспечивая таким образом цитопротекцию.[13]
Hsc70 дополнительно служит положительным регулятором перехода клеточного цикла и канцерогенеза. Например, Hsc70 регулирует накопление в ядре циклина D1, который играет ключевую роль в переходе клеточного цикла из G1 в S-фазу.[14][15]
Другая функция Hsc70 - это АТФаза в разборке клатрин покрытые оболочкой везикулы во время транспорта компонентов мембраны через клетку.[5][16] Работает с ауксилин удалять клатрин из покрытых оболочкой пузырьков. В нейронах синаптоянин также является важным белком, участвующим в снятии оболочки везикул.[5] Hsc70 является ключевым компонентом шаперон-опосредованная аутофагия где он придает селективность белкам, разлагаемым этим лизосомным путем.[5][16]
Сравнение Hsc70 и Hsp70
Человеческий Hsc70 на 85% идентичен человеческому Hsp70 (рабочая среда SDSC, анализ blosom26 по умолчанию). Научное сообщество давно предполагало, что Hsp70 и Hsc70 выполняют сходные клеточные роли, но это предположение оказалось неполным. Хотя Hsc70 также выполняет функции шаперона при нормальных условиях, в отличие от канонических белков теплового шока, Hsc70 конститутивно экспрессируется и выполняет функции, связанные с нормальными клеточными процессами, такими как белок убиквитилирование и деградация.[16][17]
Клиническое значение
Белки-члены Hsp70 являются важными составляющими апоптоза. Во время нормального эмбриологический процессов или во время повреждения клеток (например, ишемия-реперфузия во время сердечные приступы и удары ) или во время разработки и процессов в рак, апоптотическая клетка претерпевает структурные изменения, включая сжатие клеток, образование пузырей плазматической мембраны, ядерную конденсацию и фрагментацию ДНК и ядро. Далее следует фрагментация на апоптотические тельца, которые быстро удаляются фагоциты, тем самым предотвращая воспалительный отклик.[18] Это способ гибели клеток, определяемый характерными морфологическими, биохимическими и молекулярными изменениями. Сначала он был описан как «усадочный некроз», а затем этот термин был заменен на апоптоз, чтобы подчеркнуть его противоположную роль. митоз в кинетике тканей. На более поздних стадиях апоптоза вся клетка становится фрагментированной, образуя ряд апоптотических тел, связанных с плазматической мембраной, которые содержат ядерные и / или цитоплазматические элементы. Ультраструктурный вид некроз Совершенно иначе, основными признаками которого являются набухание митохондрий, разрушение плазматической мембраны и распад клеток. Апоптоз встречается во многих физиологический и патологический процессы. Он играет важную роль во время эмбриональный развитие как запрограммированная гибель клеток и сопровождает множество нормальных инволюционных процессов, в которых оно служит механизмом для удаления «нежелательных» клеток.
Белки-члены Hsp70, включая Hsp72, ингибируют апоптоз, воздействуя на каспаззависимый путь и против агентов, вызывающих апоптоз, таких как фактор некроза опухоли-α (TNFα), стауроспорин, и доксорубицин. Эта роль приводит к его вовлечению во многие патологические процессы, такие как онкогенез, нейродегенерация и старение. В частности, сверхэкспрессия HSP72 была связана с развитием некоторых видов рака, таких как гепатоцеллюлярная карцинома, рак желудка, рак толстой кишки, рак груди, и рак легких, что привело к его использованию в качестве прогностический маркер для этих видов рака.[7] Повышенный уровень Hsp70 в опухолевых клетках может увеличиваться злокачественная опухоль и сопротивление терапии путем комплексообразования и, следовательно, стабилизации онкофетальных белков и продуктов и их транспортировки во внутриклеточные участки, тем самым способствуя пролиферации опухолевых клеток.[19][7] В результате опухоль вакцина стратегии для Hsp70s были очень успешными в моделях на животных и прошли клинические испытания.[7] Одно лечение, рекомбинированная вакцина Hsp72 / AFP, вызывало устойчивый защитный иммунитет против опухолей, экспрессирующих AFP, в экспериментах на мышах. Таким образом, вакцина перспективна для лечения гепатоцеллюлярной карциномы.[7] С другой стороны, сверхэкспрессия Hsp70 может уменьшить повреждение от ишемия -реперфузия в сердечной мышце, а также повреждения от нейродегенеративных заболеваний, таких как Болезнь Альцгеймера, Болезнь Паркинсона, Болезнь Хантингтона, и спиноцеребеллярная атаксия, а также старение и старение клеток, наблюдаемые у долгожителей, подвергшихся воздействию теплового шока.[19][20] В частности, Hsc70 играет защитную роль при вышеупомянутых заболеваниях, а также при других нервно-психических расстройствах, таких как шизофрения.[21] Его защитная роль была дополнительно подчеркнута в исследовании, которое идентифицировало HSPA8 вместе с другими белками HSP70 в основной подсети более широкого интерактома шаперома, который функционирует как защита протеостаза и подавляется в стареющем мозге и в мозге при болезни Альцгеймера, Паркинсона и Хантингтона. больные заболеваниями.[22]
Взаимодействия
Hsc70 образует шаперонный комплекс, взаимодействуя с белком теплового шока 40 кДа (Hsp40 ), белок теплового шока 90 кДа (Hsp90 ), белок, взаимодействующий с hsc70 (БЕДРО ), белок-организатор hsc70-hsp90 (ПРЫГАТЬ ) и ассоциированный с Bcl2 белок атаноген 1 (BAG1 ).[12]
Также было показано, что HSPA8 взаимодействовать с:
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000109971 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000015656 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ а б c d е ж грамм «Ген Entrez: белок теплового шока HSPA8 70 кДа 8».
- ^ а б c d Майер М.П., Букау Б. (март 2005 г.). «Шапероны Hsp70: клеточные функции и молекулярный механизм». Клеточные и молекулярные науки о жизни. 62 (6): 670–684. Дои:10.1007 / s00018-004-4464-6. ЧВК 2773841. PMID 15770419.
- ^ а б c d е ж грамм Ван X, Ван Цюй, Линь Х, Ли С., Сунь Л., Ян Й (февраль 2013 г.). «HSP72 и gp96 при гастроэнтерологическом раке». Clinica Chimica Acta; Международный журнал клинической химии. 417: 73–9. Дои:10.1016 / j.cca.2012.12.017. PMID 23266770.
- ^ Xilouri M, Stefanis L (декабрь 2016 г.). "Шаперон опосредованная аутофагия: голодание, чтобы процветать". Обзоры исследований старения. 32: 13–21. Дои:10.1016 / j.arr.2016.07.001. PMID 27484893. S2CID 884595.
- ^ Ravagnan L, Gurbuxani S, Susin SA, Maisse C, Daugas E, Zamzami N, Mak T, Jäättelä M, Penninger JM, Garrido C, Kroemer G (сентябрь 2001 г.). «Белок теплового шока 70 противодействует фактору, вызывающему апоптоз». Nat. Cell Biol. 3 (9): 839–43. Дои:10.1038 / ncb0901-839. PMID 11533664. S2CID 21164493.
- ^ Чжан Б., Жун Р., Ли Х, Пэн Х, Сюн Л., Ван И, Ю Х, Мао Х (2015). «Белок теплового шока 72 подавляет апоптоз за счет повышения стабильности X-связанного ингибитора белка апоптоза при ишемии / реперфузии почек». Мол Мед Реп. 11 (3): 1793–9. Дои:10.3892 / mmr.2014.2939. ЧВК 4270332. PMID 25394481.
- ^ а б Чжан П., Лей Джи, Мерфи М.Э., Джордж Д.Л., Марморштейн Р. (2014). "Кристаллическая структура индуцируемого стрессом домена связывания субстрата человеческого белка теплового шока 70 в комплексе с пептидным субстратом". PLOS ONE. 9 (7): e103518. Дои:10.1371 / journal.pone.0103518. ЧВК 4110032. PMID 25058147.
- ^ а б Majeski AE, Dice JF (2004). «Механизмы шаперон-опосредованной аутофагии». Int. J. Biochem. Cell Biol. 36 (12): 2435–44. Дои:10.1016 / j.biocel.2004.02.013. PMID 15325583.
- ^ а б c Xie W, Zhang L, Jiao H, Guan L, Zha J, Li X, Wu M, Wang Z, Han J, You H (июль 2015 г.). «Шаперон-опосредованная аутофагия предотвращает апоптоз за счет разрушения BBC3 / PUMA». Аутофагия. 11 (9): 1623–1635. Дои:10.1080/15548627.2015.1075688. ЧВК 4590652. PMID 26212789.
- ^ Diehl, JA; Ян, Вт; Римерман, Р.А.; Сяо, H; Эмили, А (март 2003 г.). «Hsc70 регулирует накопление циклина D1 и циклин D1-зависимой протеинкиназы». Молекулярная и клеточная биология. 23 (5): 1764–74. Дои:10.1128 / mcb.23.5.1764-1774.2003. ЧВК 151693. PMID 12588994.
- ^ Хатакеяма Т, Дай П, Харада Й, Хино Х, Цукахара Ф, Мару Й, Оцудзи Э, Такамацу Т (2013). «Коннексин 43 действует как новый взаимодействующий партнер родственного белка теплового шока 70». Научные отчеты. 3: 2719. Дои:10.1038 / srep02719. ЧВК 3779846. PMID 24056538.
- ^ а б c Гольдфарб С.Б., Кашлан О.Б., Уоткинс Дж.Н., Суауд Л., Ян В., Клейман Т.Р., Рубинштейн Р.К. (апрель 2006 г.). «Дифференциальные эффекты Hsc70 и Hsp70 на внутриклеточный транспорт и функциональную экспрессию эпителиальных натриевых каналов». Труды Национальной академии наук Соединенных Штатов Америки. 103 (15): 5817–22. Дои:10.1073 / pnas.0507903103. ЧВК 1458656. PMID 16585520.
- ^ Сосс С.Е., Роуз К.Л., Хилл С., Жуан С., Чазин В.Дж. (2015). «Биохимический и протеомный анализ убиквитинирования Hsc70 и Hsp70 с помощью E3-лигазы CHIP». PLOS ONE. 10 (5): e0128240. Дои:10.1371 / journal.pone.0128240. ЧВК 4444009. PMID 26010904.
- ^ Керр Дж. Ф., Уилли А. Х., Карри А. Р. (август 1972 г.). «Апоптоз: основное биологическое явление с широким спектром влияния на кинетику тканей». Британский журнал рака. 26 (4): 239–57. Дои:10.1038 / bjc.1972.33. ЧВК 2008650. PMID 4561027.
- ^ а б Майер М.П., Букау Б. (март 2005 г.). «Шапероны Hsp70: клеточные функции и молекулярный механизм». Клеточные и молекулярные науки о жизни. 62 (6): 670–84. Дои:10.1007 / s00018-004-4464-6. ЧВК 2773841. PMID 15770419.
- ^ Хенстридж, округ Колумбия, Уизем М., Феббрайо, Массачусетс (2014). «Сопровождение метаболической стороны: новая терапевтическая роль белков теплового шока при ожирении и диабете 2 типа». Мол Метаб. 3 (8): 781–93. Дои:10.1016 / j.molmet.2014.08.003. ЧВК 4216407. PMID 25379403.
- ^ Бозидис П., Хифантис Т., Мантас С., Сотиропулу М., Антипа Н., Андреулакис Е., Серретти А., Мавреас В., Антониу К. (апрель 2014 г.). «Полиморфизмы HSP70 у пациентов с шизофренией, не принимавших наркотики в первый психотический эпизод». Науки о жизни. 100 (2): 133–7. Дои:10.1016 / j.lfs.2014.02.006. PMID 24548631.
- ^ Бреме М., Войзин С., Роллан Т., Вачи С., Сопер Дж. Х., Чжу Й., Ортон К., Виллелла А., Гарза Д., Видаль М., Ге Г., Моримото Р. И. (2014). «Консервированная подсеть шаперома защищает гомеостаз белка при старении и нейродегенеративных заболеваниях». Сотовый представитель. 9 (3): 1135–1150. Дои:10.1016 / j.celrep.2014.09.042. ЧВК 4255334. PMID 25437566.
- ^ а б c Такаяма С., Се З., Рид Дж. К. (январь 1999 г.). «Эволюционно консервативное семейство регуляторов молекулярных шаперонов Hsp70 / Hsc70». Журнал биологической химии. 274 (2): 781–6. Дои:10.1074 / jbc.274.2.781. PMID 9873016.
- ^ Такаяма С., Бимстон Д. Н., Мацузава С., Фриман BC, Эйме-Семпе С., Се З., Моримото Р. И., Рид Дж. К. (август 1997 г.). «BAG-1 модулирует шаперонную активность Hsp70 / Hsc70». Журнал EMBO. 16 (16): 4887–96. Дои:10.1093 / emboj / 16.16.4887. ЧВК 1170124. PMID 9305631.
- ^ Мики К., Эдди Э.М. (апрель 2002 г.). «Рецептор 1 фактора некроза опухоли представляет собой АТФазу, регулируемую глушителем домена смерти». Молекулярная и клеточная биология. 22 (8): 2536–43. Дои:10.1128 / MCB.22.8.2536-2543.2002. ЧВК 133739. PMID 11909948.
- ^ Ajuh P, Kuster B, Panov K, Zomerdijk JC, Mann M, Lamond AI (декабрь 2000 г.). «Функциональный анализ человеческого комплекса CDC5L и идентификация его компонентов с помощью масс-спектрометрии». Журнал EMBO. 19 (23): 6569–81. Дои:10.1093 / emboj / 19.23.6569. ЧВК 305846. PMID 11101529.
- ^ Yahata T., de Caestecker MP, Lechleider RJ, Andriole S, Roberts AB, Isselbacher KJ, Shioda T. (март 2000 г.). «Не связывающийся с ДНК трансактиватор MSG1 связывается с коактиваторами p300 / CBP, усиливая их функциональную связь с факторами транскрипции Smad». Журнал биологической химии. 275 (12): 8825–34. Дои:10.1074 / jbc.275.12.8825. PMID 10722728.
- ^ а б Хатакеяма Т, Дай П, Харада Й, Хино Х, Цукахара Ф, Мару Й, Оцудзи Э, Такамацу Т (2013). «Коннексин 43 действует как новый взаимодействующий партнер родственного белка теплового шока 70». Научные отчеты. 3: 2719. Дои:10.1038 / srep02719. ЧВК 3779846. PMID 24056538.
- ^ Саркар С., Поллак Б. П., Лин К. Т., Котенко С. В., Кук Дж. Р., Льюис А., Пестка С. (декабрь 2001 г.). «hTid-1, белок DnaJ человека, модулирует путь передачи сигналов интерферона». Журнал биологической химии. 276 (52): 49034–42. Дои:10.1074 / jbc.M103683200. PMID 11679576.
- ^ Руал Дж. Ф., Венкатесан К., Хао Т., Хирозане-Кишикава Т., Дрикот А., Ли Н., Берриз Г. Ф., Гиббонс Ф. Д., Дрезе М., Айви-Гедехуссу Н., Клитгорд Н., Саймон К., Боксем М., Мильштейн С., Розенберг Дж., Голдберг DS, Zhang LV, Wong SL, Franklin G, Li S, Albala JS, Lim J, Fraughton C, Llamosas E, Cevik S, Bex C, Lamesch P, Sikorski RS, Vandenhaute J, Zoghbi HY, Smolyar A, Bosak S, Sequerra R, Doucette-Stamm L, Cusick ME, Hill DE, Roth FP, Vidal M (октябрь 2005 г.). «К карте протеомного масштаба сети взаимодействия белок-белок человека». Природа. 437 (7062): 1173–8. Дои:10.1038 / природа04209. PMID 16189514. S2CID 4427026.
- ^ Stelzl U, Worm U, Lalowski M, Haenig C, Brembeck FH, Goehler H, Stroedicke M, Zenkner M, Schoenherr A, Koeppen S, Timm J, Mintzlaff S, Abraham C, Bock N, Kietzmann S, Goedde A, Toksöz E , Droege A, Krobitsch S, Korn B, Birchmeier W, Lehrach H, Wanker EE (сентябрь 2005 г.). «Сеть взаимодействия белок-белок человека: ресурс для аннотирования протеома». Клетка. 122 (6): 957–68. Дои:10.1016 / j.cell.2005.08.029. HDL:11858 / 00-001M-0000-0010-8592-0. PMID 16169070. S2CID 8235923.
- ^ Имаи Ю., Сода М., Хатакеяма С., Акаги Т., Хашикава Т., Накаяма К.И., Такахаши Р. (июль 2002 г.). «CHIP связан с паркином, геном, ответственным за семейную болезнь Паркинсона, и усиливает его активность убиквитинлигазы». Молекулярная клетка. 10 (1): 55–67. Дои:10.1016 / S1097-2765 (02) 00583-X. PMID 12150907.
- ^ Баллинджер CA, Коннелл П., Ву И, Ху З., Томпсон Л.Дж., Инь Л.Й., Паттерсон С. (июнь 1999 г.). «Идентификация CHIP, нового белка, содержащего тетратрикопептидные повторы, который взаимодействует с белками теплового шока и отрицательно регулирует функции шаперонов». Молекулярная и клеточная биология. 19 (6): 4535–45. Дои:10.1128 / mcb.19.6.4535. ЧВК 104411. PMID 10330192.
дальнейшее чтение
- Кианг Дж. Г. (декабрь 2004 г.). «Индуцируемый белок теплового шока 70 кДа и индуцибельная синтаза оксида азота при повреждении, вызванном кровотечением / реанимацией». Клеточные исследования. 14 (6): 450–9. Дои:10.1038 / sj.cr.7290247. PMID 15625011. S2CID 21654486.
- Расмуссен Х. Х., ван Дамм Дж., Пуйпе М., Гессер Б., Селис Дж. Э., Вандекеркхов Дж. (Декабрь 1992 г.). «Микропоследовательности 145 белков, записанные в базе данных двумерных гелевых белков нормальных эпидермальных кератиноцитов человека». Электрофорез. 13 (12): 960–9. Дои:10.1002 / elps.11501301199. PMID 1286667. S2CID 41855774.
- Хаттори Х., Лю Ю.С., Тонай И., Уэда М., Канеда Т., Кобаяши Т., Танабе К., Оцука К. (февраль 1992 г.). «Внутриклеточная локализация и частичная аминокислотная последовательность стресс-индуцируемого белка 40 кДа в клетках HeLa». Структура и функции клеток. 17 (1): 77–86. Дои:10.1247 / csf.17.77. PMID 1586970.
- ДеЛука-Флаэрти C, McKay DB, Parham P, Hill BL (сентябрь 1990 г.). «Непокрытый белок (hsc70) связывает конформационно лабильный домен легкой цепи клатрина LCa, чтобы стимулировать гидролиз АТФ». Клетка. 62 (5): 875–87. Дои:10.1016 / 0092-8674 (90) 90263-Е. PMID 1975516. S2CID 9501568.
- Лим М.Ю., Дэвис Н., Чжан Дж.Й., Bose HR (март 1990 г.). «Онкогенный продукт v-rel образует комплекс с клеточными белками, включая его протоонкогенный продукт и белок теплового шока 70». Вирусология. 175 (1): 149–60. Дои:10.1016 / 0042-6822 (90) 90195-В. PMID 2155506.
- Уэлч WJ, Mizzen LA (апрель 1988 г.). «Характеристика термотолерантной клетки. II. Влияние на внутриклеточное распределение белка теплового шока 70, промежуточных филаментов и малых ядерных рибонуклеопротеидных комплексов». Журнал клеточной биологии. 106 (4): 1117–30. Дои:10.1083 / jcb.106.4.1117. ЧВК 2115010. PMID 2966179.
- Dworniczak B, Mirault ME (июль 1987 г.). «Структура и экспрессия человеческого гена, кодирующего« родственный »белок теплового шока 71 кД». Исследования нуклеиновых кислот. 15 (13): 5181–97. Дои:10.1093 / nar / 15.13.5181. ЧВК 305955. PMID 3037489.
- Rensing SA, Maier UG (июль 1994 г.). «Филогенетический анализ семейства белков стресс-70». Журнал молекулярной эволюции. 39 (1): 80–6. Дои:10.1007 / BF00178252. PMID 7545947. S2CID 37505045.
- Лейн Б., Ириарте А., Маттингли-младший, Морено Дж. И., Мартинес-Каррион М. (октябрь 1995 г.). «Структурные особенности предшественника митохондриальной аспартатаминотрансферазы, ответственного за связывание с hsp70». Журнал биологической химии. 270 (42): 24732–9. Дои:10.1074 / jbc.270.42.24732. PMID 7559589.
- Бенароудж Н., Бателье Дж., Триниоль Ф., Ладжими М.М. (ноябрь 1995 г.). «Самоассоциация молекулярного шаперона HSC70». Биохимия. 34 (46): 15282–90. Дои:10.1021 / bi00046a037. PMID 7578144.
- Nunes SL, Calderwood SK (август 1995 г.). «Фактор теплового шока-1 и родственный ему белок 70 связываются в высокомолекулярные комплексы в цитоплазме клеток NIH-3T3». Сообщения о биохимических и биофизических исследованиях. 213 (1): 1–6. Дои:10.1006 / bbrc.1995.2090. PMID 7639722.
- Иноуэ А., Торигоэ Т., Согахата К., Камигучи К., Такахаши С., Савада Ю., Сайджо М., Тайя Ю., Исии С., Сато Н., Кикучи К. (сентябрь 1995 г.). "Родственный белок теплового шока 70 кДа взаимодействует непосредственно с N-концевой областью продукта гена ретинобластомы pRb. Идентификация новой области взаимодействия белков, опосредующих pRb". Журнал биологической химии. 270 (38): 22571–6. Дои:10.1074 / jbc.270.38.22571. PMID 7673249.
- Абэ Т., Кониси Т., Хирано Т., Касаи Х., Симидзу К., Кашимура М., Хигаши К. (январь 1995 г.). «Возможная корреляция между повреждением ДНК, вызванным перекисью водорода, и перемещением белка теплового шока 70 в ядро». Сообщения о биохимических и биофизических исследованиях. 206 (2): 548–55. Дои:10.1006 / bbrc.1995.1078. PMID 7826371.
- Furlini G, Vignoli M, Re MC, Gibellini D, Ramazzotti E, Zauli G, La Placa M (январь 1994 г.). «Взаимодействие вируса иммунодефицита человека типа 1 с мембраной клеток CD4 + индуцирует синтез и ядерную транслокацию 70К белка теплового шока». Журнал общей вирусологии. 75 (1): 193–9. Дои:10.1099/0022-1317-75-1-193. PMID 7906708.
- Маруяма К., Сугано С. (январь 1994 г.). «Олиго-кэппинг: простой метод замены кэп-структуры эукариотических мРНК олигорибонуклеотидами». Ген. 138 (1–2): 171–4. Дои:10.1016/0378-1119(94)90802-8. PMID 8125298.
- Тавария М., Габриэль Т., Андерсон Р.Л., Миро М.Э., Бейкер Е., Сазерленд Дж., Кола I (сентябрь 1995 г.). «Локализация гена, кодирующего родственный белок теплового шока человека, HSP73, на хромосоме 11». Геномика. 29 (1): 266–8. Дои:10.1006 / geno.1995.1242. PMID 8530083.
- Гао Б., Айзенберг Е., Грин Л. (июль 1996 г.). «Влияние конститутивной полимеризации белка теплового шока 70 кДа на его взаимодействие с белковым субстратом». Журнал биологической химии. 271 (28): 16792–7. Дои:10.1074 / jbc.271.28.16792. PMID 8663341.
- Эгертон М., Мориц Р.Л., Друкер Б., Келсо А., Симпсон Р.Дж. (июль 1996 г.). «Идентификация родственного протеина теплового шока 70 кДа (Hsc70) и альфа-актинина-1 как новых фосфотирозин-содержащих белков в Т-лимфоцитах». Сообщения о биохимических и биофизических исследованиях. 224 (3): 666–74. Дои:10.1006 / bbrc.1996.1082. PMID 8713105.
- Lamian V, Small GM, Feldherr CM (октябрь 1996 г.). «Доказательства существования нового механизма ядерного импорта Hsc70». Экспериментальные исследования клеток. 228 (1): 84–91. Дои:10.1006 / excr.1996.0302. PMID 8892974.
- Хансен С., Миджли Калифорния, Лейн Д.П., Фриман Британская Колумбия, Моримото Р.И., Хапп Т.Р. (ноябрь 1996 г.). «Для активации мышиного p53 бактериальным Hsp70 требуется модификация двух различных COOH-концевых доменов». Журнал биологической химии. 271 (48): 30922–8. Дои:10.1074 / jbc.271.48.30922. PMID 8940078.
внешняя ссылка
- Hsc70 + белок в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- PDBe-KB предоставляет обзор всей структурной информации, доступной в PDB для человеческого родственного белка 71 кДа теплового шока