Алюминий (I) - Aluminium(I)
В химии, алюминий (I) относится к одновалентный алюминий (+1 степень окисления) в обоих ионный и ковалентный облигации. Наряду с алюминием (II) это чрезвычайно нестабильная форма алюминия.
Пока поздно Элементы группы 3 Такие как таллий и индий предпочитают степень окисления +1, алюминий (I) встречается редко. В отличие от элементов поздней группы XIII, алюминий не испытывает эффект инертной пары, явление, при котором валентные s-электроны плохо защищены от ядерного заряда из-за наличия заполненных d- и f-орбиталей.[1] Таким образом, алюминий (III) () является гораздо более распространенной степенью окисления алюминия.
Оба соединения алюминия (I) склонны к непропорциональность и сложно приготовить.[2] В стандартных условиях они легко окисляются до формы алюминия (III).
Характеристики

Al (I) кажется красным, так как растворы AlBr и AlCl в органических растворителях оба красные.[4] Наличие этого цвета означает относительно небольшой промежуток HOMO / LUMO, доступный для зеленого света.[5]
Геометрия соединений может быть определена путем анализа тонкой структуры электронных спектров.[2] Спектроскопия матричной изоляции предотвращает диспропорционирование моногалогенидов алюминия и, таким образом, позволяет измерять переходные колебания, а также реакционную способность с такими молекулами, как O2.[2][6]
Анализ 27Al ЯМР-спектроскопия AlCl, AlBr и AlI в толуоле / диэтиловом эфире при комнатной температуре обнаруживают два сигнала: один очень широкий сигнал при δ = 100-130 м.д. (независимо от галогена) и один при более высокой напряженности поля (AlCl: δ = + 30, AlBr: δ = + 50 , AlI: δ = + 80).[2] Первый сигнал соответствует стабилизированной донором четырехкоординатной разновидности алюминия, в то время как идентичность последнего не доказана.[2]
Моногалогениды
Катион алюминия (I) реагирует с галогенидами водорода с образованием следующих моногалогенидов алюминия:[1]
- монофторид алюминия (AlF)
- монохлорид алюминия (AlCl)
- монобромид алюминия (AlBr)
- монойодид алюминия (AlI)
Эти соединения термодинамически устойчивы только при высоких температурах и низких давлениях в основном синглетном состоянии.[7] Однако разложение можно предотвратить, сделав диспропорционирование кинетически невыгодным. При низких температурах (ниже 77 K ) диспропорционирование происходит достаточно медленно, чтобы твердое вещество AlCl могло сохраняться в течение длительных периодов времени.[1]
Синтез
AlCl синтезируется реакцией жидкого алюминия с газообразным HCl при 1200 К и 0,2 мбар с образованием газообразного AlCl и газообразного водорода.[1] При 77 К AlCl представляет собой темно-красное твердое вещество, которое становится черным при диспропорционировании при температурах выше 180 К. При температурах ниже 77 К и растворенном в матрице полярных и неполярных растворителей он существует в виде метастабильного раствора, реакционная способность которого может быть учился. AlBr, красное масло, получают аналогичным образом из жидкого металлического алюминия и газообразного HBr.[4]
Из-за характера HF, у которого связь намного сильнее, чем у его сородичей,[8] Вместо этого AlF синтезируется соразмерность Ала и AlF3 которые прессуются и смешиваются с гранулами.[9] Затем окатыши загружают в графитовую печь и нагревают до 1050 К.[9]
Стабильность увеличивается с увеличением массы: в то время как AlCl разлагается при 77 К или выше, AlBr остается стабильным до 253 К.[1][4] Примечательно, что было обнаружено, что при любой заданной температуре давление пара AlF на порядки ниже, чем у других моногалогенидов алюминия.[9]
Диспропорционирование
При комнатной температуре соединения AlX имеют тенденцию к непропорциональности Al и AlX.3. Когда темно-красный твердый AlCl нагревается, он становится черным, образуя металлический алюминий и более стабильную хлоридную соль алюминия (III).[1]
Dohmier et. все документально подтверждено, что исключением является AlBr. AlBr достаточно стабилен при температурах ниже -30 C, поэтому он пропорционален AlBr.2 в присутствии AlBr3.[2]
Олигомеризация
В основных растворах Льюиса соединения AlX имеют тенденцию к олигомеризации.[2]
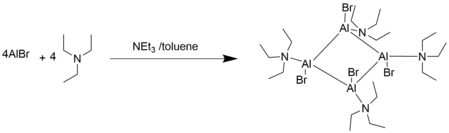
Комплексная химия
Алюминий - это не только самый распространенный металл в земной коре, но также элемент малотоксичный. Как таковые комплексы алюминия (I) вызывают значительный интерес. Эти комплексы могут поддерживаться различными лигандами и использоваться для активации небольших молекул.
β-Дикетиминато Системы
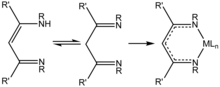
В 2018 году Liu et. al сделал обзор химии алюминия (I) с β-дикетиминатными лигандами,[10] широко используемые лиганды с огромным разнообразием электронных и стерических свойств. Эти комплексы алюминия (I) обладают огромным потенциалом для активации малых молекул.[10]
Синтез
β-дикетиминатоалюминийалкилы и галогениды алюминия синтезируются путем добавления соединения триалкилалюминия к исходным β-дикетиминатным лигандам, добавления йода и восстановления калием.[10]
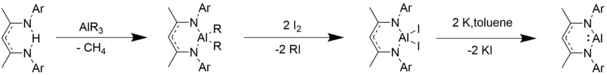
[1 + 2] Циклоприсоединения
Соединения Al (I) демонстрируют поведение, аналогичное поведению синглетных карбены.[10] Подобно карбенам, они претерпевают [1 + 2] циклоприсоединение с алкинами и азидами с образованием трехчленных кольцевых производных, таких как диалюмациклогексадиен.[1][10]
Подобно нуклеофильному углеродному центру в карбене неподеленная пара на алюминиевом центре связывается с первым азидным эквивалентом. Выделяется газообразный азот. Со вторым эквивалентом азида образуется пятичленное кольцо.
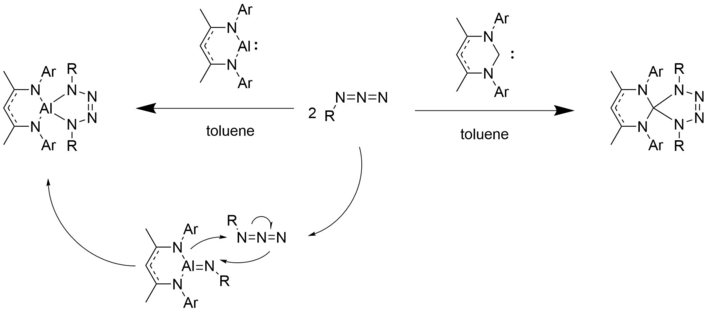
Реакции с другими небольшими молекулами
Такие комплексы алюминия (I) могут активировать воду, а также элементарный фосфор, кислород и серу с образованием мостиковых димеров. Это происходит за счет частичного восстановления элементарной небольшой молекулы.[10]


AlCp *
AlCp *, состоящий из алюминия (I), соединенного с пентаметилциклопентадиен-анион ((CCH3)5−), был впервые синтезирован в 1991 г. Dohmier et al.[12] (AlCp *)4, желтое кристаллическое твердое вещество, сначала получают из комбинации AlCl и MgCp *2.[6] При испарении длинные связи Al-Al (276,9 мкм)[12] расщепляются, и образуются мономерные молекулы [AlCp *].
Как показала работа Шнокеля, [AlCp *] реагирует, вставляя себя в другие связи. Реакция с Al2я6 дает субвалентные галогениды; реакция с As4tBu4 дает связи As-Al.[6] При взаимодействии с комплексами переходный металл-циклопентадиенил, такими как NiCp2, он предлагает прямой путь к соединениям, содержащим связи алюминий-переходный металл, которые имеют большой потенциал для важных каталитических реакций.[2]


Как и другие лиганды AlR, [AlCp *] можно рассматривать как CO аналог, поскольку он имеет 2 пустые π-орбитали и задействован в аналогичных режимах координации (терминальный и мостовой).[6] Это сходство подразумевает возможность Пи обратное соединение взаимодействия между AlCp * и металлами, с которыми он соединяется.
Металлоидные кластеры
Работа с алюминиевыми кластерами была проделана Linti и Schnockel. Эти металлоидные кластеры могут быть образованы из соединений Al (I), а именно моногалогенидов алюминия. Эти кластеры называют «металлоидными кластерами», потому что количество немостиковых связей металл-металл больше, чем количество локализованных связей металл-лиганд. На пути к образованию металла промежуточные соединения улавливаются в присутствии объемных лигандов, которые замещают атомы галогенидов.[6][1] В результате кластеры с высоким содержанием металлов, такие как Al77р20 возможны и дают представление об образовании твердых массивных металлов.[6]
Тетраэдрический алюминий доступен в результате реакции между частицами алюминия (I) и металлоорганическими соединениями.[6] Эти кластеры можно получить с помощью таких комбинаций, как AlCp * и LiR, AlBr и Li (THF).3(SiMe3)3, и AlI и NaSiBu3.[6]


Этот метод образования кластеров создал единственный известный случай падения октаэдрического алюминиевого кластера [Al6(tBu)6]−, который образовался в результате реакции AlCl с тBuLi.[6] Аналогично, AlCl и LiN (SiMe3)2 реагируют с образованием первого известного примера кластера, в котором два M4 тетраэдры связаны общим центром.[6]
Естественное происхождение
В природе алюминий редко встречается в степени окисления +1 из-за огромной стабильности степени окисления +3.
Вращательные переходы AlF и AlCl обнаружены в околозвездные снаряды возле IRC +10216.[9][13] Присутствие AlF говорит о том, что фтор образуется во вспышках гелиевой оболочки, а не в взрывной нуклеосинтез.[13]
Рекомендации
- ^ а б c d е ж грамм час Таке, Матиас; Schnoeckel, Hansgeorg (1 июля 1989 г.). «Метастабильный хлорид алюминия, AlCl, в твердом виде и в растворе». Неорганическая химия. 28 (14): 2895–2896. Дои:10.1021 / ic00313a039. ISSN 0020-1669.
- ^ а б c d е ж грамм час я Домайер, Карстен; Лоос, Дагмар; Шнёкель, Хансгеорг (1996-02-02). «Соединения алюминия (I) и галлия (I): синтезы, структуры и реакции». Angewandte Chemie International Edition на английском языке. 35 (2): 129–149. Дои:10.1002 / anie.199601291. ISSN 0570-0833.
- ^ ван дер Верд, Марк Дж .; Ламмерцма, Куп; Дюк, Брайан Дж .; Шефер, Генри Ф. (1991-07-15). «Простые смешанные гидриды бора, алюминия и галлия: AlBH6, AlGaH6 и BGaH6». Журнал химической физики. 95 (2): 1160–1167. Дои:10.1063/1.461146. ISSN 0021-9606.
- ^ а б c Мокер, Марио; Робл, Кристиан; Шнёкель, Хансгеорг (1994-05-02). «Донор-стабилизированный бромид алюминия (II)». Angewandte Chemie International Edition на английском языке. 33 (8): 862–863. Дои:10.1002 / anie.199408621. ISSN 0570-0833.
- ^ Борен, Крейг (2006). Основы атмосферной радиации: введение с 400 проблемами. Wiley-VCH. стр.214. ISBN 978-3-527-40503-9.
- ^ а б c d е ж грамм час я j k Шнокель (1 сентября 2000 г.). «Низковалентные соединения алюминия и галлия - структурное разнообразие и способы координации с фрагментами переходных металлов». Обзоры координационной химии. 206–207: 285–319. Дои:10.1016 / S0010-8545 (00) 00339-8. ISSN 0010-8545.
- ^ Нагендран, Сельвараджан; Роески, Герберт В. (05.02.2008). «Химия алюминия (I), кремния (II) и германия (II)». Металлоорганические соединения. 27 (4): 457–492. Дои:10.1021 / om7007869. ISSN 0276-7333.
- ^ Бенсон, Сидней В. (1965). «III - Связанные энергии». Журнал химического образования. 42 (9): 502. Дои:10.1021 / ed042p502. ISSN 0021-9584.
- ^ а б c d Дайк, J.M .; Кирби, C .; Моррис, А .; Gravenor, B.W.J .; Klein, R .; Росмус, П. (1984-08-01). «Исследование монофторида алюминия и трифторида алюминия методами высокотемпературной фотоэлектронной спектроскопии». Химическая физика. 88 (2): 289–298. Bibcode:1984CP ..... 88..289D. Дои:10.1016/0301-0104(84)85286-6. ISSN 0301-0104.
- ^ а б c d е ж грамм Лю, Яшуай; Ли, Цзя; Ма, Сяоли; Ян, Чжи; Роески, Герберт В. (2018-11-01). «Химия алюминия (I) с β-дикетиминатными лигандами и пентаметилциклопентадиенильными заместителями: синтез, реакционная способность и применения». Обзоры координационной химии. 374: 387–415. Дои:10.1016 / j.ccr.2018.07.004. ISSN 0010-8545.
- ^ Цуй, Чуньмин; Роески, Герберт В .; Шмидт, Ханс-Георг; Нольтемейер, Матиас; Хао, Хайцзюнь; Чимпоэсу, Фаника (01.12.2000). «Синтез и структура мономерного соединения алюминия (I) [{HC (CMeNAr) 2} Al] (Ar = 2,6 – iPr2C6H3): стабильный алюминиевый аналог карбена». Angewandte Chemie International Edition. 39 (23): 4274–4276. Дои:10.1002 / 1521-3773 (20001201) 39:23 <4274 :: AID-ANIE4274> 3.0.CO; 2-K. ISSN 1521-3773.
- ^ а б Домайер, Карстен; Робл, Кристиан; Таке, Матиас; Шнёкель, Hansgeorg (1991). «Тетрамерное соединение алюминия (I) [{Al (η5-C5Me5)} 4]». Angewandte Chemie International Edition на английском языке. 30 (5): 564–565. Дои:10.1002 / anie.199105641. ISSN 0570-0833.
- ^ а б Зюрис, Л. М .; Аппони, А. Дж .; Филлипс, Т. Г. (1994-04-07). «Экзотические молекулы фторида в IRC +10216: Подтверждение наличия AlF и поиски MgF и CaF». Астрофизический журнал. 433: 729–732. Bibcode:1994ApJ ... 433..729Z. Дои:10.1086/174682. ISSN 0004-637X.





