Углекислый газ (страница данных) - Carbon dioxide (data page)
На этой странице представлены дополнительные химические данные о углекислый газ.
Паспорт безопасности материала
Обращение с этим химическим веществом может потребовать серьезных мер предосторожности. Настоятельно рекомендуется обратиться к паспорту безопасности материалов (MSDS ) для этого химического вещества из надежного источника, такого как СИРИ, и следуйте его указаниям. MSDS для твердого диоксида углерода можно получить в Pacific Dry Ice, inc.
Структура и свойства
| Структура и свойства | |
|---|---|
| Показатель преломления, пD | 1.000449 при 589,3 нм и 0 ° C [1] |
| Диэлектрическая постоянная, εр | 1,60 ε0 при 0 ° C, 50 атм |
| Средний энергия на связь C = O | 804,4 кДж / моль при 298 К (25 ° C)[2] |
| Длина скрепления | C = O 116,21 пм (1,1621 Å) [3] |
| Угол крепления | O – C – O: 180 °[3] |
| Магнитная восприимчивость | ? |
| Поверхностное натяжение | 4,34 дин / см при 20 ° C и равновесное давление |
| Вязкость[4] жидкости при равновесном давлении | 0,0925 мПа · с при 5 ° C 0,0852 мПа · с при 10 ° C 0,0712 мПа · с при 20 ° C 0,0625 мПа · с при 25 ° C 0,0321 мПа · с при 31,1 ° C |
Термодинамические свойства
| Фазовое поведение | |
|---|---|
| Тройная точка | 216,58 К (-56,57 ° C), 518,5 кПа |
| Критическая точка | 304,18 К (31,03 ° C), 7,38 МПа |
| Стандартное изменение энтальпии сплава, ΔсуетитьсяЧАС | 8,647 кДж / моль в тройной точке[5] |
| Изменение энтропии сплава, ΔсуетитьсяS | 40 Дж / (моль · К) в тройной точке |
| Стандартное изменение энтальпии испарения,[6] ΔvapЧАС | 15,326 кДж / моль при 215,7 К (-57,5 ° C) |
| Стандартное изменение энтропии испарения, ΔvapS | 70,8 Дж / (моль · К) |
| Твердые свойства | |
| Стандартное изменение энтальпии формирования, ΔжЧАС | -427,4 кДж / моль |
| Стандартная молярная энтропия,[7] S | 51,07 Дж / (моль · К) |
| Теплоемкость,[7] cп | 2,534 Дж / (моль · К) при 15,52 К (-257,63 ° C) |
| Жидкие свойства | |
| Стандартное изменение энтальпии формирования, ΔжЧАС | ? кДж / моль |
| Стандартная молярная энтропия, S | ? Дж / (моль К) |
| Теплоемкость, cп | ? Дж / (моль · К) |
| Свойства газа | |
| Стандартное изменение энтальпии формирования, ΔжЧАС | -393,52 кДж / моль |
| Стандартная молярная энтропия, S | 213,79 Дж / (моль · К) |
| Теплоемкость,[8] cп | 33,89 Дж / (моль К) при –75 ° C |
| Коэффициент теплоемкости[8] γ = cп/cv | 1,37 при –75 ° C |
| константы Ван-дер-Ваальса[9] | а = 363,96 л2 кПа / моль2 b = 0,04267 литра на моль |
| Равновесие с монооксид углерода[10] CO + ½O2 → CO2 K = pK = журнал10 K | pK = 45,0438 при T = 298,16 К |
Растворимость в воде при различных температурах
| Растворимость CO в воде2 при 101,3 кПа (1 банкомат ) частичное давление[11] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
- ‡Во втором столбце таблицы указана растворимость CO при каждой заданной температуре в объеме.2 поскольку это будет измерено при 101,3 кПа и 0 ° C на объем воды.
- Растворимость дана для «чистой воды», т.е. воды, содержащей только CO.2. Эта вода будет кислой. Например, при 25 ° C pH ожидается 3,9 (см. угольная кислота ). При менее кислых значениях pH растворимость будет увеличиваться из-за pH -зависимое видообразование CO2.
Давление пара твердого и жидкого
| P в мм рт. Ст. | 1 | 10 | 40 | 100 | 400 | 760 | 1520 | 3800 | 7600 | 15200 | 30400 | 45600 | |
| P в атм (2sf, рассчитано из мм рт. Ст.) | 0.0013 | 0.013 | 0.053 | 0.13 | 0.53 | 1.0 | 2.0 | 5.0 | 10 | 20 | 40 | 60 | |
| P в кПа (мм рт. Ст. / Атм.) | 0.13 | 1.3 | 5.3 | 13 | 53 | 101.325 | 202.65 | 506.625 | 1013.25 | 2026.5 | 4053 | 6079.5 | |
| Т в ° C | −134.3(s) | −119.5(s) | −108.6(s) | −100.2(s) | −85.7(s) | −78.2(s) | −69.1(s) | −56.7 | −39.5 | −18.9 | 5.9 | 22.4 | |
Табличные данные получены из CRC Справочник по химии и физике 44-е изд. Обозначение «(s)» указывает равновесную температуру пара над твердым телом. В противном случае температура - это равновесие пара над жидкостью. Для значений кПа, где исходное значение - это целое число атмосфер, приведены точные значения кПа, в других местах 2 значащих числа, полученных из данных в мм рт.

Фазовая диаграмма
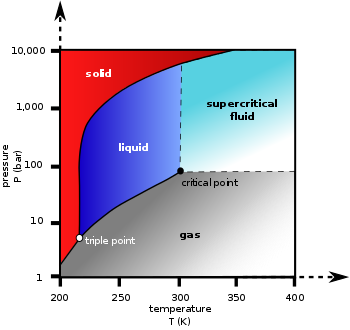
Термодинамические данные по равновесию жидкость / пар
В таблице ниже приведены термодинамические данные жидкого CO.2 в равновесии со своим паром при различных температурах. Данные теплосодержания, теплоты испарения и значения энтропии относятся к жидкому состоянию при температуре 0 ° C и давлении 3483 кПа. Чтобы преобразовать значение теплоты в джоуль на моль, умножьте его на 44,095 г / моль. Чтобы преобразовать плотность в моль на литр, умножьте его на 22,678 см.3 моль / (л · г). Данные получены из CRC Справочник по химии и физике, 44-е изд. стр. 2560–2561, за исключением критической температуры (31,1 ° C) и температуры −30 ° C и ниже, взятых из Справочник Ланге по химии, 10-е изд. стр. 1463.
| Термодинамические данные о равновесии диоксида углерода жидкость / пар | ||||||||
| Темп. ° C | пvap Пар давление кПа | ЧАСжидкость Высокая температура содержание жидкость J /грамм | ЧАСvap Высокая температура содержание пар J /грамм | ΔvapЧАС Жара пар ization J /грамм | ρvap Плотность пара г / см3 | ρжидкость Плотность жидкости г / см3 | Sжидкость Энтропия жидкость J /моль - ° С | Svap Энтропия пар J /моль - ° С |
|---|---|---|---|---|---|---|---|---|
| −56.6 | 518.3 | 1.179 | ||||||
| −56.0 | 531.8 | 1.177 | ||||||
| −54.0 | 579.1 | 1.169 | ||||||
| −52.0 | 629.6 | 1.162 | ||||||
| −50.0 | 683.4 | 1.155 | ||||||
| −48.0 | 740.6 | 1.147 | ||||||
| −46.0 | 801.3 | 1.139 | ||||||
| −44.0 | 865.6 | 1.131 | ||||||
| −42.0 | 933.8 | 1.124 | ||||||
| −40.0 | 1005.7 | 1.116 | ||||||
| −38.0 | 1081.9 | 1.108 | ||||||
| −36.0 | 1161.8 | 1.100 | ||||||
| −34.0 | 1246.2 | 1.092 | ||||||
| −32.0 | 1335.1 | 1.084 | ||||||
| −30.0 | 1428.6 | 1.075 | ||||||
| −28.89 | 1521 | −55.69 | 237.1 | 292.9 | 0.03846 | 1.0306 | −9.48 | 43.41 |
| −27.78 | 1575 | −53.76 | 237.3 | 291.0 | 0.03987 | 1.0276 | −9.13 | 43.21 |
| −26.67 | 1630 | −51.84 | 237.6 | 289.4 | 0.04133 | 1.0242 | −8.78 | 43.01 |
| −25.56 | 1686 | −49.87 | 237.6 | 287.5 | 0.04283 | 1.0209 | −8.45 | 42.78 |
| −24.44 | 1744 | −47.91 | 237.8 | 285.7 | 0.04440 | 1.0170 | −8.10 | 42.56 |
| −23.33 | 1804 | −45.94 | 237.8 | 283.6 | 0.04600 | 1.0132 | −7.75 | 42.36 |
| −22.22 | 1866 | −43.93 | 237.8 | 281.7 | 0.04767 | 1.0093 | −7.40 | 42.14 |
| −21.11 | 1928 | −41.92 | 237.8 | 279.6 | 0.04938 | 1.0053 | −7.05 | 41.94 |
| −20.00 | 1993 | −39.91 | 237.8 | 277.8 | 0.05116 | 1.0011 | −6.68 | 41.71 |
| −18.89 | 2059 | −37.86 | 237.8 | 275.7 | 0.05300 | 0.9968 | −6.31 | 41.49 |
| −17.78 | 2114 | −35.82 | 237.6 | 273.6 | 0.05489 | 0.9923 | −5.98 | 41.27 |
| −16.67 | 2197 | −33.73 | 237.6 | 271.2 | 0.05686 | 0.9875 | −5.61 | 41.05 |
| −15.56 | 2269 | −31.64 | 237.3 | 269.2 | 0.05888 | 0.9829 | −5.26 | 40.83 |
| −14.44 | 2343 | −29.54 | 237.3 | 266.9 | 0.06098 | 0.9782 | −4.91 | 40.61 |
| −13.33 | 2418 | −27.41 | 237.1 | 264.5 | 0.06314 | 0.9734 | −4.54 | 40.39 |
| −12.22 | 2495 | −25.27 | 236.9 | 262.2 | 0.06539 | 0.9665 | −4.17 | 40.15 |
| −11.11 | 2574 | −23.09 | 236.7 | 259.7 | 0.06771 | 0.9639 | −3.80 | 39.92 |
| −10.00 | 2654 | −20.90 | 236.4 | 257.3 | 0.07011 | 0.9592 | −3.43 | 39.68 |
| −8.89 | 2738 | −18.69 | 235.9 | 254.8 | 0.07259 | 0.9543 | −3.06 | 39.46 |
| −7.78 | 2823 | −16.45 | 235.7 | 252.2 | 0.07516 | 0.9494 | −2.69 | 39.22 |
| −6.67 | 2910 | −14.18 | 235.2 | 249.4 | 0.07783 | 0.9443 | −2.32 | 38.98 |
| −5.56 | 2999 | −11.90 | 234.8 | 246.6 | 0.08059 | 0.9393 | −1.94 | 38.74 |
| −4.44 | 3090 | −9.977 | 234.3 | 243.8 | 0.08347 | 0.9340 | −1.57 | 38.50 |
| −3.89 | 3136 | −8.410 | 234.1 | 242.4 | 0.08494 | 0.9313 | −1.37 | 38.37 |
| −2.78 | 3230 | −6.046 | 233.6 | 239.7 | 0.08797 | 0.9260 | −0.98 | 38.12 |
| −1.67 | 3327 | −3.648 | 232.9 | 236.6 | 0.09111 | 0.9206 | −0.59 | 37.88 |
| −0.56 | 3425 | −1.222 | 232.4 | 233.6 | 0.09438 | 0.9150 | −0.20 | 37.62 |
| 0.56 | 3526 | 1.234 | 231.7 | 230.5 | 0.09776 | 0.9094 | 0.20 | 37.36 |
| 1.67 | 3629 | 3.728 | 231.0 | 227.3 | 0.1013 | 0.9036 | 0.61 | 37.08 |
| 2.78 | 3735 | 6.268 | 230.4 | 224.0 | 0.1050 | 0.8975 | 1.01 | 36.83 |
| 3.89 | 3843 | 8.445 | 229.4 | 220.5 | 0.1088 | 0.8914 | 1.42 | 36.55 |
| 5.00 | 3953 | 11.46 | 228.5 | 217.0 | 0.1128 | 0.8850 | 1.83 | 36.25 |
| 6.11 | 4067 | 14.13 | 227.6 | 213.4 | 0.1169 | 0.8784 | 2.25 | 35.98 |
| 7.22 | 4182 | 16.85 | 226.5 | 209.7 | 0.1213 | 0.8716 | 2.69 | 35.68 |
| 8.33 | 4300 | 19.63 | 225.4 | 205.8 | 0.1258 | 0.8645 | 3.12 | 35.39 |
| 9.44 | 4420 | 22.46 | 224.3 | 201.8 | 0.1306 | 0.8571 | 3.56 | 35.07 |
| 10.56 | 4544 | 25.36 | 223.1 | 197.7 | 0.1355 | 0.8496 | 4.02 | 34.76 |
| 11.67 | 4670 | 28.33 | 221.8 | 193.4 | 0.1408 | 0.8418 | 4.48 | 34.45 |
| 12.78 | 4798 | 31.35 | 220.3 | 188.9 | 0.1463 | 0.8338 | 4.94 | 34.11 |
| 13.89 | 4929 | 34.49 | 218.8 | 184.3 | 0.1521 | 0.8254 | 5.42 | 33.76 |
| 15.00 | 5063 | 37.30 | 217.2 | 179.5 | 0.1583 | 0.8168 | 5.92 | 33.41 |
| 16.11 | 5200 | 41.03 | 215.1 | 174.4 | 0.1648 | 0.8076 | 6.42 | 33.02 |
| 17.22 | 5340 | 44.48 | 213.6 | 169.1 | 0.1717 | 0.7977 | 6.96 | 32.66 |
| 18.33 | 5482 | 48.03 | 211.5 | 163.5 | 0.1791 | 0.7871 | 7.49 | 32.25 |
| 19.44 | 5628 | 51.71 | 209.4 | 157.6 | 0.1869 | 0.7759 | 8.04 | 31.83 |
| 20.56 | 5776 | 55.61 | 207.0 | 151.4 | 0.1956 | 0.7639 | 8.63 | 31.38 |
| 21.67 | 5928 | 59.66 | 204.3 | 144.7 | 0.2054 | 0.7508 | 9.24 | 30.90 |
| 22.78 | 6083 | 63.97 | 201.5 | 137.5 | 0.2151 | 0.7367 | 9.89 | 30.39 |
| 23.89 | 6240 | 68.58 | 198.4 | 129.8 | 0.2263 | 0.7216 | 10.57 | 29.85 |
| 25.00 | 6401 | 73.51 | 194.8 | 121.3 | 0.2387 | 0.7058 | 11.31 | 29.24 |
| 26.11 | 6565 | 78.91 | 190.7 | 111.8 | 0.2532 | 0.6894 | 12.10 | 28.60 |
| 27.22 | 6733 | 84.94 | 186.0 | 101.1 | 0.2707 | 0.6720 | 12.99 | 27.84 |
| 28.33 | 6902 | 91.88 | 180.4 | 88.49 | 0.2923 | 0.6507 | 14.00 | 26.95 |
| 29.44 | 7081 | 100.4 | 173.1 | 72.72 | 0.3204 | 0.6209 | 15.24 | 25.85 |
| 30.00 | 7164 | 105.6 | 168.4 | 62.76 | 0.3378 | 0.5992 | 16.01 | 25.15 |
| 30.56 | 7253 | 112.3 | 162.3 | 50.04 | 0.3581 | 0.5661 | 16.99 | 24.24 |
| 31.1 | 7391 | 0.00 | 0.4641 | 0.4641 | ||||
| Темп. ° C | пvap Пар давление кПа | ЧАСжидкость Высокая температура содержание жидкость J /грамм | ЧАСvap Высокая температура содержание пар J /грамм | ΔvapЧАС Жара пар ization J /грамм | ρvap Плотность пара г / см3 | ρжидкость Плотность жидкости г / см3 | Sжидкость Энтропия жидкость J /моль - ° С | Svap Энтропия пар J /моль - ° С |
Спектральные данные
| УФ-видимый | |
|---|---|
| λМаксимум | ? нм |
| Коэффициент экстинкции, ε | ? |
| ИК[а] | |
| Основные полосы поглощения[нужна цитата ] | 2350 и 667 см−1 (4,25 и 14,99 мкм) |
| ЯМР | |
| Протонный ЯМР | непригодный |
| Углерод-13 ЯМР | 125.0[12] |
| РС | |
| Массы основных фрагментов | |
Примечания
- ^ Поскольку азот и кислород симметричны, а углекислый газ и водяной пар - нет, воздух в инфракрасном спектрофотометре может показывать поглощение CO.2 и вода. Это легко преодолеть, вычтя пустой спектр из экспериментального спектра, и инструменты часто также продувают сухим азотом.
Рекомендации
- ^ «Показатель преломления газов». НПЛ. Архивировано из оригинал 7 октября 2010 г.. Получено 7 апреля 2010.
- ^ Дарвент, Б. де Б. (1970). "Связанные энергии диссоциации в простых молекулах" Нац. Стоять. Ref. Data Ser., Nat. Бур. Стоять. (США) 31, 52 стр.
- ^ а б "Список экспериментальных данных CCCBDB, страница 2". cccbdb.nist.gov. Получено 1 декабря 2018.
- ^ Справочник Ланге по химии, 10-е изд. стр. 1669–1674
- ^ «Газовая энциклопедия». Air Liquide. Получено 1 июня 2007.
- ^ а б «Свойства чистого компонента» (Запрашиваемая база данных). Информационный центр исследований химической инженерии. Получено 8 мая 2007.
- ^ а б W. F. Giauque и C. J. Egan, "Двуокись углерода. Теплоемкость и давление пара твердого тела. Теплота сублимации. Термодинамические и спектроскопические значения энтропии", Journal of Chemical Physics, vol. 5. С. 45–54, 1937.
- ^ а б Справочник Ланге по химии, 10-е изд., С. 1525–1528.
- ^ Справочник Ланге по химии, 10-е изд., Стр. 1522–1524.
- ^ Справочник Ланге по химии, 10-е изд. С. 1573–1576.
- ^ Справочник Ланге по химии, 10 изд., 1100 с.
- ^ Райх, Х. Дж. «Химические сдвиги C-13». Информация об органической химии. Университет Висконсина. Архивировано из оригинал 2 марта 2015 г.. Получено 31 мая 2015.
- Линстром, Питер Дж .; Маллард, Уильям Г. (ред.); Веб-книга NIST Chemistry, стандартная справочная база данных NIST номер 69, Национальный институт стандартов и технологий, Гейтерсбург (Мэриленд), http://webbook.nist.gov
Если не указано иное, данные относятся к стандартная температура и давление окружающей среды.
Отказ от ответственности применяется.

![{ displaystyle { frac {[{ ce {CO2}}]} {[{ ce {CO}}] [{ ce {O2}}] ^ {1/2}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/68e0ac469da9090ce82b0809b5419cda523617c8)
