Частичное давление - Partial pressure
В смеси газы, каждый составляющий газ имеет частичное давление что является условным давление этого составляющего газа, если бы он один занимал всю объем исходной смеси при том же температура.[1] Общее давление идеальный газ смесь - это сумма парциальных давлений газов в смеси (Закон Дальтона ).
Парциальное давление газа является мерой термодинамической активности газа. молекулы. Газы растворяются, диффундируют и реагируют в соответствии с их парциальным давлением, а не в соответствии с их концентрации в газовых смесях или жидкостях. Это общее свойство газов справедливо и для химических реакций газов в биологии. Например, количество кислорода, необходимое для дыхания человека и количество токсичных веществ, определяется парциальным давлением только кислорода. Это верно для очень широкого диапазона различных концентраций кислорода, присутствующего в различных вдыхаемых газах для дыхания или растворенного в крови.[требуется разъяснение ][2] Парциальные давления кислорода и углекислого газа являются важными параметрами при испытаниях газы артериальной крови, но также может измеряться, например, в спинномозговая жидкость.
Символ
Символ давления обычно п или п которые могут использовать нижний индекс для обозначения давления, а газообразные вещества также обозначаются нижним индексом. При объединении эти индексы применяются рекурсивно.[3][4]
Примеры:
- или = давление в момент времени 1
- или = парциальное давление водорода
- или = венозное парциальное давление кислорода
Закон парциальных давлений Дальтона
Закон Дальтона выражает тот факт, что полное давление смеси газов равно сумме парциальных давлений отдельных газов в смеси.[5] Это равенство возникает из-за того, что в идеальном газе молекулы настолько удалены друг от друга, что не взаимодействуют друг с другом. Большинство реальных газов очень близко подходят к этому идеалу. Например, учитывая идеальную газовую смесь азот (N2), водород (ЧАС2) и аммиак (NH3):
| где: | |
| = полное давление газовой смеси | |
| = парциальное давление азота (Н2) | |
| = парциальное давление водорода (H2) | |
| = парциальное давление аммиака (NH3) |

Идеальные газовые смеси
В идеале отношение парциальных давлений равно отношению количества молекул. Это мольная доля отдельного газового компонента в идеальный газ смесь можно выразить через парциальное давление компонента или родинки компонента:
а парциальное давление отдельного газового компонента в идеальном газе можно получить с помощью этого выражения:
| где: | |
| = мольная доля любого отдельного газового компонента в газовой смеси | |
| = парциальное давление любого отдельного газового компонента в газовой смеси | |
| = моль любого отдельного газового компонента в газовой смеси | |
| = общее количество молей газовой смеси | |
| = полное давление газовой смеси |
Мольная доля газового компонента в газовой смеси равна объемной доле этого компонента в газовой смеси.[6]
Отношение парциальных давлений основывается на следующем соотношении изотерм:
- VИкс - это частичный объем любого отдельного газового компонента (X)
- Vмалыш общий объем газовой смеси
- пИкс это частичное давление газа X
- пмалыш полное давление газовой смеси
- пИкс это количество вещества газа (X)
- пмалыш это общее количество вещества в газовой смеси
Частичный объем (закон аддитивного объема Амагата)
Парциальный объем конкретного газа в смеси - это объем одного компонента газовой смеси. Это полезно в газовых смесях, например воздух, чтобы сосредоточиться на одном конкретном компоненте газа, например кислород.
Его можно аппроксимировать как парциальным давлением, так и молярной долей:[7]
- VИкс - парциальный объем отдельного газового компонента X в смеси
- Vмалыш общий объем газовой смеси
- пИкс - парциальное давление газа X
- пмалыш полное давление газовой смеси
- пИкс это количество вещества газа X
- пмалыш общее количество вещества в газовой смеси
Давление газа
Давление газа это давление пар в равновесии с его непаровой фазой (то есть жидкой или твердой). Чаще всего этот термин используется для описания жидкость склонность к испариться. Это мера тенденции молекулы и атомы вырваться из жидкости или твердый. Точка кипения жидкости при атмосферном давлении соответствует температуре, при которой давление ее пара равно окружающему атмосферному давлению, и ее часто называют температурой. нормальная точка кипения.
Чем выше давление пара жидкости при данной температуре, тем ниже нормальная точка кипения жидкости.
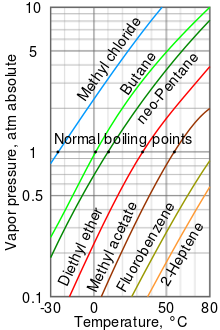
На отображаемой диаграмме давления пара есть графики зависимости давления пара от температуры для различных жидкостей.[8] Как видно из диаграммы, жидкости с самым высоким давлением пара имеют самую низкую нормальную температуру кипения.
Например, при любой заданной температуре метилхлорид имеет самое высокое давление пара среди всех жидкостей в таблице. Он также имеет самую низкую нормальную точку кипения (-24,2 ° C), где кривая давления паров хлористого метила (синяя линия) пересекает горизонтальную линию давления в одну атмосферу (банкомат ) абсолютного давления пара. Обратите внимание, что на больших высотах атмосферное давление ниже, чем на уровне моря, поэтому точки кипения жидкостей снижаются. На вершине гора Эверест, атмосферное давление составляет примерно 0,333 атм, поэтому, используя график, точка кипения диэтиловый эфир будет примерно 7,5 ° C по сравнению с 34,6 ° C на уровне моря (1 атм).
Константы равновесия реакций с участием газовых смесей
Возможно проработать константа равновесия для химической реакции с участием смеси газов с учетом парциального давления каждого газа и общей формулы реакции. Для обратимой реакции с участием газовых реагентов и газовых продуктов, таких как:
константа равновесия реакции будет:
| где: | |
| = константа равновесия реакции | |
| = коэффициент реагента | |
| = коэффициент реагента | |
| = коэффициент продукта | |
| = коэффициент продукта | |
| = парциальное давление возведен во власть | |
| = парциальное давление возведен во власть | |
| = парциальное давление возведен во власть | |
| = парциальное давление возведен во власть |
Для обратимых реакций изменения общего давления, температуры или концентрации реагентов будут сдвигать равновесие так, чтобы отдать предпочтение правой или левой стороне реакции в соответствии с Принцип Ле Шателье. Однако кинетика реакции может либо противодействовать, либо усиливать сдвиг равновесия. В некоторых случаях кинетика реакции может быть решающим фактором, который следует учитывать.
Закон Генри и растворимость газов
Газы будут растворяться в жидкости в степени, которая определяется равновесием между нерастворенным газом и газом, растворенным в жидкости (называемым растворитель ).[9] Константа равновесия для этого равновесия:
- (1)
где: = константа равновесия для сольватация обработать = парциальное давление газа в равновесии с решение содержащий немного газа = концентрация газа в жидком растворе
Вид константы равновесия показывает, что концентрация растворенное вещество газ в растворе прямо пропорционален парциальному давлению этого газа над раствором.. Это заявление известно как Закон Генри и константа равновесия довольно часто называют постоянной закона Генри.[9][10][11]
Закон Генри иногда записывают так:[12]
- (2)
где также называется постоянной закона Генри.[12] Как видно из сравнения уравнений (1) и (2) выше, является обратной величиной . Поскольку и то, и другое можно назвать константой закона Генри, читатели технической литературы должны быть очень осторожны, чтобы отметить, какая версия уравнения закона Генри используется.
Закон Генри - это приближение, которое применимо только к разбавленным идеальным растворам и к растворам, в которых жидкий растворитель не действует. химически реагировать с растворяющимся газом.
В дайвинге дышащие газы
В подводное плавание физиологические эффекты отдельных составляющих газов дышащие газы является функцией парциального давления.
Используя условия погружения, парциальное давление рассчитывается как:
- парциальное давление = (общее абсолютное давление) × (объемная доля газового компонента)
Для компонентного газа «i»:
- пя = P × Fя
Например, на глубине 50 метров (164 фута) под водой общее абсолютное давление составляет 6 бар (600 кПа) (т. Е. 1 бар абсолютного давления). атмосферное давление + 5 бар давления воды) и парциальные давления основных компонентов воздуха, кислород 21% к объему и азот примерно 79% по объему составляют:
- pN2 = 6 бар × 0,79 = 4,7 бар абс.
- pO2 = 6 бар × 0,21 = 1,3 бар абс.
| где: | |
| пя | = парциальное давление газовой составляющей i = в терминах, используемых в этой статье |
|---|---|
| п | = полное давление = в терминах, используемых в этой статье |
| Fя | = объемная доля газового компонента i = мольная доля, , в терминах, используемых в этой статье |
| pN2 | = парциальное давление азота = в терминах, используемых в этой статье |
| pO2 | = парциальное давление кислорода = в терминах, используемых в этой статье |
Минимальный безопасный нижний предел парциального давления кислорода в газовой смеси составляет 0,16 бар (16 кПа) абсолютного давления. Гипоксия и внезапная потеря сознания становится проблемой при парциальном давлении кислорода менее 0,16 бар абсолютного давления. Кислородная токсичность, включая судороги, становится проблемой при слишком высоком парциальном давлении кислорода. В NOAA Руководство по дайвингу рекомендует максимальную однократную экспозицию в течение 45 минут при абсолютном давлении 1,6 бара, 120 минут при абсолютном давлении 1,5 бара, 150 минут при абсолютном давлении 1,4 бара, 180 минут при абсолютном давлении 1,3 бара и 210 минут при абсолютном давлении 1,2 бара. Кислородная токсичность становится опасной, когда эти парциальные давления кислорода превышаются. Парциальное давление кислорода определяет максимальная рабочая глубина газовой смеси.
Наркоз это проблема при вдыхании газов под высоким давлением. Обычно максимальное общее парциальное давление наркотических газов, используемое при планировании технический дайвинг может составлять около 4,5 бар абсолютного давления, исходя из эквивалентная наркотическая глубина 35 метров (115 футов).
Воздействие токсичного загрязнителя, такого как монооксид углерода при вдыхании газа также связано с парциальным давлением при вдыхании. Смесь, которая может быть относительно безопасной на поверхности, может быть опасно токсичной на максимальной глубине погружения или допустимом уровне углекислый газ в дыхательной петле ныряния ребризер может стать невыносимым в течение нескольких секунд во время спуска, когда парциальное давление быстро увеличивается, и может привести к панике или выведению из строя дайвера.
В медицине
Парциальные давления особенно кислорода () и диоксид углерода () являются важными параметрами при тестировании газы артериальной крови, но также может измеряться, например, в спинномозговая жидкость.[Зачем? ]
| Единица измерения | Газ артериальной крови | Венозный газ крови | Спинномозговая жидкость | Альвеолярный легочный давление газа | |
|---|---|---|---|---|---|
| кПа | 11–13[13] | 4.0–5.3[13] | 5.3–5.9[13] | 14.2 | |
| мм рт. ст. | 75–100[14] | 30–40[15] | 40–44[16] | 107 | |
| кПа | 4.7–6.0[13] | 5.5–6.8[13] | 5.9–6.7[13] | 4.8 | |
| мм рт. ст. | 35–45[14] | 41–51[15] | 44–50[16] | 36 |
Смотрите также
- Газ для дыхания - Газ, используемый для дыхания человека
- Закон Генри - Связь равновесной растворимости газа в жидкости с его парциальным давлением в контактирующей газовой фазе.
- Идеальный газ - Математическая модель, которая приближает поведение реальных газов
- Закон идеального газа - Уравнение состояния гипотетического идеального газа
- Мольная доля - Отношение одного компонента к общему количеству всех компонентов в смеси, выраженное в моль / моль.
- Моль (единица) - единица измерения количества вещества в системе СИ
- Пар - Вещества в газовой фазе при температуре ниже своей критической точки
использованная литература
- ^ Чарльз Хенриксон (2005). Химия. Записки скал. ISBN 978-0-7645-7419-1.
- ^ «Давление газа и дыхание». Люмен Обучение.
- ^ Штат сотрудников. «Символы и единицы» (PDF). Респираторная физиология и нейробиология: Руководство для авторов. Эльзевир. п. 1. Получено 3 июн 2017.
Все символы, относящиеся к газам, находятся в нижнем индексе,
- ^ ИЮПАК, Сборник химической терминологии 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) "давление п ". Дои:10.1351 / goldbook.P04819
- ^ Закон частичных давлений Дальтона
- ^ «Общая химия онлайн» государственного университета Фростберга
- ^ Страница 200 в: Медицинская биофизика. Флемминг Корнелиус. 6-е издание, 2008 г.
- ^ Перри, Р.Х. и Грин, Д.В. (Редакторы) (1997). Справочник инженеров-химиков Перри (7-е изд.). Макгроу-Хилл. ISBN 978-0-07-049841-9.CS1 maint: несколько имен: список авторов (ссылка на сайт) CS1 maint: дополнительный текст: список авторов (ссылка на сайт)
- ^ а б Обширный список констант закона Генри и инструмент преобразования
- ^ Фрэнсис Л. Смит и Аллан Х. Харви (сентябрь 2007 г.). «Избегайте распространенных ошибок при использовании закона Генри». CEP (Прогресс химической инженерии). ISSN 0360-7275.
- ^ Введение в университетскую химию, закон Генри и растворимость газов В архиве 2012-05-04 в Wayback Machine
- ^ а б "Заметки о занятиях по химии в Университете Аризоны". Архивировано из оригинал на 2012-03-07. Получено 2006-05-26.
- ^ а б c d е ж Получено из значений в мм рт. Ст. С использованием 0,133322 кПа / мм рт.
- ^ а б Таблица нормального эталонного диапазона В архиве 2011-12-25 на Wayback Machine из Юго-западного медицинского центра Техасского университета в Далласе. Используется в интерактивном справочнике по изучению патологий болезни.
- ^ а б Отдел медицинского образования Brookside Associates -> ABG (газ артериальной крови) Проверено 6 декабря 2009 г.
- ^ а б ПАТОЛОГИЯ 425 ЦЕРЕБРОСПИНАЛЬНАЯ ЖИДКОСТЬ [CSF] В архиве 2012-02-22 в Wayback Machine на кафедре патологии и лабораторной медицины Университета Британской Колумбии. Автор: доктор Г. Бонди. Проверено ноябрь 2011 г.
















































