GRASP65 - GRASP65
Повторная сборка-укладка белка Гольджи 65 кДа (GRASP65) также известен как Повторная сборка-укладка белка Гольджи 1 (GORASP1) это белок что у людей кодируется GORASP1 ген.[4]
Функция

В аппарат Гольджи играет ключевую роль в сортировка и модификация белков, экспортируемых из эндоплазматический ретикулум. Белок GRASP65 представляет собой белок периферической мембраны привязанный к липидный бислой через миристоилирование из глицин остаток рядом с белком амино-конец.[6] Он участвует в создании многослойной структуры аппарата Гольджи и связывает стопки в более крупные ленты в клетках позвоночных.[6] Это каспаза-3 субстрат, и расщепление этого кодируемого белка способствует фрагментации Гольджи при апоптозе.[7][8] GRASP65 может образовывать комплекс с матричным белком Гольджи GM130, и этот комплекс связывается с белком стыковки везикул p115.[6][а] Было идентифицировано несколько альтернативно сплайсированных вариантов транскрипта этого гена, но их полноразмерная природа не определена.[4]
Структура
GRASP65 состоит из двух PDZ домены в амино-концевом домене GRASP (аминокислотные остатки 2–210), что составляет примерно половину белка. Область GRASP взаимодействует с матричным белком Гольджи GM130, а также с внутренне неупорядоченная область в C-конец.[6][9]
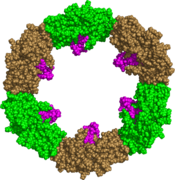
GRASP65 superhelix, вид сверху[6]
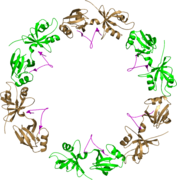


GRASP65 superhelix, вид сбоку[6]

Взаимодействия
GORASP1 был показан взаимодействовать с участием TGF альфа,[10] TMED2[10] и ГОЛГА2.[10][11][12]
Заметки
- ^ Это показано во внешней ссылке, озаглавленной «Молекулярные модели GRASP65 / GM130 / P115-опосредованного стэкинга цис-цистерн мембран и связывания везикул».
использованная литература
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000114745 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ а б "Ген Entrez: GORASP1 повторная сборка белка Гольджи 1, 65 кДа".
- ^ Ван И, Вэй Дж. Х., Бисел Б., Тан Д., Земанн Дж. (Февраль 2008 г.). «Цистернальное разложение по Гольджи стимулирует отрастание везикул COPI и транспорт белка». PLOS ONE. 3 (2): e1647. Дои:10.1371 / journal.pone.0001647. ЧВК 2249924. PMID 18297130.
- ^ а б c d е ж Ху Ф, Ши Х, Ли Б., Хуанг Х, Морелли Х, Ши Н (2015). «Структурная основа взаимодействия между белком повторной сборки-укладки Гольджи GRASP65 и матричным белком Гольджи GM130». Журнал биологической химии. 290 (44): 26373–82. Дои:10.1074 / jbc.M115.657940. ЧВК 4646294. PMID 26363069.
- ^ Лейн Дж. Д., Люкок Дж., Прайд Дж., Барр Ф. А., Вудман П. Г., Аллан В. Дж., Лоу М. (2002). «Опосредованное каспазой расщепление укладывающегося белка GRASP65 необходимо для фрагментации по Гольджи во время апоптоза». Журнал клеточной биологии. 156 (3): 495–509. Дои:10.1083 / jcb.200110007. ЧВК 2173349. PMID 11815631.
- ^ Ченг Дж. П., Бетин В. М., Вейр Х., Шелмани Г. М., Мосс Д. К., Лейн Дж. Д. (2010). «Расщепление каспазой стэкинг-фактора Гольджи GRASP65 необходимо для Fas / CD95-опосредованного апоптоза». Смерть и болезнь клеток. 1 (10): e82. Дои:10.1038 / cddis.2010.59. ЧВК 3035901. PMID 21368855.
- ^ Рабуй К., Линстедт А. Д. (2016). "GRASP: Связь многозадачности". Границы клеточной биологии и биологии развития. 4: 1. Дои:10.3389 / fcell.2016.00001. ЧВК 4726779. PMID 26858948.
- ^ а б c Барр Ф.А., Прайзингер С., Копайтих Р., Кёрнер Р. (декабрь 2001 г.). «Белки матрикса Гольджи взаимодействуют с рецепторами груза p24 и способствуют их эффективному удержанию в аппарате Гольджи». Журнал клеточной биологии. 155 (6): 885–91. Дои:10.1083 / jcb.200108102. ЧВК 2150891. PMID 11739402.
- ^ Short B, Preisinger C, Körner R, Kopajtich R, Byron O, Barr FA (декабрь 2001 г.). «Эффекторный комплекс GRASP55-rab2, связывающий структуру Гольджи с мембранным движением». Журнал клеточной биологии. 155 (6): 877–83. Дои:10.1083 / jcb.200108079. ЧВК 2150909. PMID 11739401.
- ^ Короче Дж., Уотсон Р., Джаннаку М.Э., Кларк М., Уоррен Г., Барр Ф.А. (сентябрь 1999 г.). «GRASP55, второй белок GRASP млекопитающих, участвующий в укладке цистерн Гольджи в бесклеточную систему». Журнал EMBO. 18 (18): 4949–60. Дои:10.1093 / emboj / 18.18.4949. ЧВК 1171566. PMID 10487747.
дальнейшее чтение
- Барр Ф.А., Пуйпе М., Вандекеркхов Дж., Уоррен Г. (октябрь 1997 г.). «GRASP65, белок, участвующий в укладке цистерн Гольджи». Ячейка. 91 (2): 253–62. Дои:10.1016 / S0092-8674 (00) 80407-9. PMID 9346242. S2CID 11655667.
- Барр Ф.А., Накамура Н., Уоррен Г. (июнь 1998 г.). «Картирование взаимодействия между GRASP65 и GM130, компонентами белкового комплекса, участвующего в укладке цистерн Гольджи». Журнал EMBO. 17 (12): 3258–68. Дои:10.1093 / emboj / 17.12.3258. ЧВК 1170664. PMID 9628863.
- Лин CY, Madsen ML, Yarm FR, Jang YJ, Liu X, Erikson RL (ноябрь 2000 г.). «Периферический белок Гольджи GRASP65 является мишенью митотической поло-подобной киназы (Plk) и Cdc2». Труды Национальной академии наук Соединенных Штатов Америки. 97 (23): 12589–94. Дои:10.1073 / pnas.220423497. ЧВК 18808. PMID 11050165.
- Мойер Б.Д., Аллан Б.Б., Балч В.Е. (апрель 2001 г.). «Взаимодействие Rab1 с эффекторным комплексом GM130 регулирует цис-связывание везикул COPII - связывание Гольджи». Движение. 2 (4): 268–76. Дои:10.1034 / j.1600-0854.2001.1o007.x. PMID 11285137. S2CID 43069518.
- Сюттерлин С., Линь С.Й., Фенг Й., Феррис Д.К., Эриксон Р.Л., Малхотра В. (июль 2001 г.). «Поло-подобная киназа необходима для фрагментации перицентриолярных стеков Гольджи во время митоза». Труды Национальной академии наук Соединенных Штатов Америки. 98 (16): 9128–32. Дои:10.1073 / pnas.161283998. ЧВК 55384. PMID 11447294.
- Ward TH, Полищук RS, Caplan S, Hirschberg K, Lippincott-Schwartz J (ноябрь 2001 г.). «Поддержание структуры и функции Гольджи зависит от целостности экспорта ER». Журнал клеточной биологии. 155 (4): 557–70. Дои:10.1083 / jcb.200107045. ЧВК 2198855. PMID 11706049.
- Лейн Дж. Д., Люкок Дж., Прайд Дж., Барр Ф. А., Вудман П. Г., Аллан В. Дж., Лоу М. (февраль 2002 г.). «Опосредованное каспазой расщепление стекового белка GRASP65 необходимо для фрагментации по Гольджи во время апоптоза». Журнал клеточной биологии. 156 (3): 495–509. Дои:10.1083 / jcb.200110007. ЧВК 2173349. PMID 11815631.
- Jesch SA (июль 2002 г.). «Наследование структурного каркаса для биосинтеза Гольджи». BioEssays. 24 (7): 584–7. Дои:10.1002 / bies.10122. PMID 12111718.
- Протопопов А., Кашуба В., Забаровская В.И., Муравенко О.В., Лерман М.И., Клейн Г., Забаровский Е.Р. (январь 2003 г.). «Интегрированная физическая и генная карта области 3,5 МП хромосомы 3p21.3 (AP20), вовлеченной в основные злокачественные новообразования эпителия человека». Исследования рака. 63 (2): 404–12. PMID 12543795.
- Ван Ю., Земанн Дж., Пипаерт М., Короче Дж., Уоррен Дж. (Июль 2003 г.). «Прямая роль GRASP65 как митотически регулируемого фактора стекинга Гольджи». Журнал EMBO. 22 (13): 3279–90. Дои:10.1093 / emboj / cdg317. ЧВК 165642. PMID 12839990.
- Колланд Ф., Жак Икс, Троплин В., Мужен С., Грозело С., Гамбург А., Мейл А., Войчик Дж., Легрен П., Готье Дж. М. (июль 2004 г.). «Функциональное протеомное картирование сигнального пути человека». Геномные исследования. 14 (7): 1324–32. Дои:10.1101 / гр. 2334104. ЧВК 442148. PMID 15231748.
- Ван И, Сато А., Уоррен Дж. (Февраль 2005 г.). «Картирование функциональных доменов фактора стекирования Гольджи GRASP65». Журнал биологической химии. 280 (6): 4921–8. Дои:10.1074 / jbc.M412407200. ЧВК 4443495. PMID 15576368.
- Йошимура С., Йошиока К., Барр Ф.А., Лоу М., Накаяма К., Окума С., Накамура Н. (июнь 2005 г.). «Конвергенция регуляции клеточного цикла и сигналов факторов роста на GRASP65». Журнал биологической химии. 280 (24): 23048–56. Дои:10.1074 / jbc.M502442200. PMID 15834132.
- Сюттерлин С., Полищук Р., Пекот М., Малхотра В. (июль 2005 г.). «Связанный с Гольджи белок GRASP65 регулирует динамику веретена и необходим для деления клеток». Молекулярная биология клетки. 16 (7): 3211–22. Дои:10.1091 / mbc.E04-12-1065. ЧВК 1165405. PMID 15888544.
внешние ссылки
| Эта статья о ген на хромосома человека 3 это заглушка. Вы можете помочь Википедии расширяя это. |









