Гальванический элемент - Galvanic cell

А гальванический элемент или же гальванический элемент, названный в честь Луиджи Гальвани или же Алессандро Вольта, соответственно, является электрохимическая ячейка который получает электрическую энергию от спонтанных редокс реакции, происходящие внутри клетки. Обычно он состоит из двух разных металлов, погруженных в электролиты, или из отдельных полуэлементов с разными металлами и их ионами в растворе, соединенных между собой. соляной мост или разделены пористой мембраной.
Вольта был изобретателем гальваническая свая, первый электрическая батарея. В общепринятом смысле слово «батарея» стало включать в себя один гальванический элемент, но батарея правильно состоит из нескольких элементов.[1]
История
В 1780 г. Луиджи Гальвани обнаружил, что когда два разных металла (например, медь и цинк) контактируют, а затем оба одновременно касаются двух разных частей мышцы лягушачьей ноги, замыкается цепь, лягушка сокращается.[2]Он назвал это "животное электричество ". Нога лягушки, будучи датчиком электрического тока, была также электролит (говоря языком современной химии).
Через год после того, как Гальвани опубликовал свою работу (1790 г.), Алессандро Вольта показали, что в лягушке не было необходимости, используя вместо этого силовой детектор и пропитанную рассолом бумагу (в качестве электролита). (Ранее Вольта установил закон емкости C = Q/V с силовыми детекторами). В 1799 году Вольта изобрел гальваническую батарею, которая представляет собой группу гальванических элементов, каждая из которых состоит из металлического диска, слоя электролита и диска из другого металла. Он построил его полностью из небиологического материала, чтобы бросить вызов Гальвани (и последующему экспериментатору). Леопольдо Нобили ) в пользу теории электричества животных в пользу его собственной теории контактного электричества металл-металл.[3] Карло Маттеуччи в свою очередь построил батарея полностью из биологического материала в ответ Вольте.[4] Взгляд Вольта на контактное электричество характеризовал каждый электрод числом, которое мы теперь назвали бы работой выхода электрода. Эта точка зрения игнорировала химические реакции на границах раздела электрод-электролит, которые включают ЧАС2 формирование на более благородном металле в куче Вольты.
Хотя Вольта не понимал принцип работы батареи или гальванического элемента, эти открытия проложили путь для электрических батарей; Ячейка Вольта получила название IEEE Milestone в 1999 году.[5]
Примерно сорок лет спустя Фарадей (см. Законы электролиза Фарадея ) показал, что гальванический элемент, который теперь часто называют гальваническим элементом, имел химическую природу. Фарадей ввел новую терминологию на язык химии: электрод (катод и анод ), электролит, и ион (катион и анион ). Таким образом, Гальвани ошибочно полагал, что источник электричества (или источник ЭДС, или место расположения ЭДС) находится в животном, Вольта ошибочно полагал, что это было в физических свойствах изолированных электродов, но Фарадей правильно определил источник ЭДС как химические реакции. на двух поверхностях раздела электрод-электролит. Авторитетная работа по интеллектуальной истории гальванической ячейки остается работой Оствальда.[6]
Это было предложено Вильгельм Кениг в 1940 году объект, известный как Багдадский аккумулятор может представлять технологию гальванических элементов из древних Парфия. Было показано, что реплики, наполненные лимонной кислотой или виноградным соком, производят напряжение. Однако нет уверенности, что это было его предназначением - другие ученые отмечали, что он очень похож на сосуды, которые, как известно, использовались для хранения пергаментных свитков.[7]
Основное описание
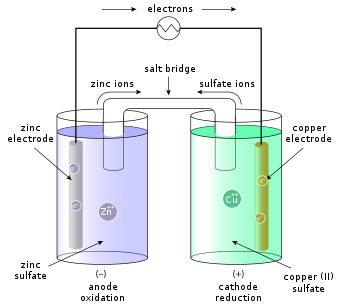
В простейшей форме полуклетка состоит из твердого металла (называемого электрод ), погруженный в раствор; решение содержит катионы (+) электродного металла и анионы (-) для балансировки заряда катионов. Полная ячейка состоит из двух полуячеек, обычно соединенных полупроницаемая мембрана или соляной мост это предотвращает осаждение ионов более благородного металла на другом электроде.
Конкретным примером является Клетка Даниэля (см. рисунок), с цинк (Zn) полуячейка, содержащая раствор ZnSO4 (сульфат цинка) и медь (Cu) полуячейка, содержащая раствор CuSO4 (сульфат меди). Здесь используется соляной мостик для замыкания электрической цепи.
Если внешний электрический провод соединяет медный и цинковый электроды, цинк из цинкового электрода растворяется в растворе в виде Zn.2+ ионы (окисление), высвобождая электроны, попадающие во внешний проводник. Чтобы компенсировать повышенную концентрацию ионов цинка, через солевой мостик ионы цинка уходят, а анионы попадают в цинковую полуячейку. В медной полуячейке ионы меди прикрепляются к медному электроду (восстановление), захватывая электроны, покидающие внешний проводник. Поскольку Cu2+ ионы (катионы) накладываются на медный электрод, последний называется катодом. Соответственно цинковый электрод является анодом. Электрохимическая реакция:
- Zn + Cu2+ → Zn2+ + Cu
Кроме того, электроны проходят через внешний проводник, который является основным назначением гальванического элемента.
Как обсуждалось в напряжение ячейки, то электродвижущая сила ячейки - это разность потенциалов полуячейки, мера относительной легкости растворения двух электродов в электролите. ЭДС зависит как от электродов, так и от электролита, что указывает на химическую природу ЭДС.
Электрохимическая термодинамика реакций гальванических элементов
Электрохимические процессы в гальваническом элементе происходят из-за того, что реагенты с высокой свободной энергией (например, металлический Zn и гидратированная Cu2+ в ячейке Даниэля) преобразуются в продукты с меньшей энергией (металлическая Cu и гидратированный Zn2+ в этом примере). Разница в энергиях когезии решетки [8] электродных металлов иногда является доминирующим энергетическим драйвером реакции, особенно в ячейке Даниэля.[9] Металлические Zn, Cd, Li и Na, не стабилизированные d-орбитальный связь, имеют более высокие энергии когезии (т.е.они более слабо связаны), чем все переходные металлы, включая Cu, и поэтому полезны в качестве анодных металлов с высокой энергией.[9]
Разница между энергиями ионизации металлов в воде [9] это другой энергетический вклад, который может запустить реакцию в гальваническом элементе; это не важно в ячейке Даниэля, потому что энергии гидратированной Cu2+ и Zn2+ ионы оказываются похожими.[9] Оба атомных переноса, например цинка с металлического электрода в раствор и перенос электронов от атомов металла или к ионам металлов играют важную роль в гальваническом элементе. Концентрационные ячейки, электроды и ионы которого сделаны из одного металла и которые двигаются за счет увеличения энтропии и уменьшения свободной энергии по мере выравнивания концентраций ионов, показывают, что электроотрицательность различие металлов не является движущей силой электрохимических процессов.
Гальванические элементы и батареи обычно используются в качестве источника электроэнергии. Энергию получают от растворения металла с высокой энергией когезии при осаждении металла с более низкой энергией и / или от осаждения ионов металла с высокой энергией, когда ионы с более низкой энергией переходят в раствор.
Количественно электрическая энергия, производимая гальваническим элементом, приблизительно равна стандартной разнице свободной энергии реагентов и продуктов, обозначенной как Δрграммо. В ячейке Даниэля большая часть электрической энергии Δрграммо = -213 кДж / моль можно отнести к разнице в -207 кДж / моль между энергиями когезии решеток Zn и Cu.[9]
Половина реакции и условности
В полуячейке металл пополам состояния окисления. Внутри изолированной полуячейки находится Снижение окисления (окислительно-восстановительная) реакция, которая находится в химическое равновесие, условие, символически записанное следующим образом (здесь "M" представляет катион металла, атом, который имеет дисбаланс заряда из-за потери "п«электроны):
- Mп+ (окисленные виды) + пе− ⇌ M (редуцированные виды)
Гальванический элемент состоит из двух полуэлементов, так что электрод одного полуэлемента состоит из металла A, а электрод другого полуэлемента состоит из металла B; Таким образом, окислительно-восстановительные реакции для двух отдельных полуэлементов:
- Ап+ + пе− ⇌ А
- Bм+ + ме− ⇌ B
Общая сбалансированная реакция
- м А + п Bм+ ⇌ п B + м Ап+
Другими словами, атомы металла одной полуячейки окисляются, а катионы металлов другой полуячейки восстанавливаются. Разделив металлы на две полуячейки, их реакцией можно управлять таким образом, чтобы обеспечить перенос электронов через внешнюю цепь, где они могут быть полезными. работай.
- Электроды соединяются металлической проволокой по порядку проводить электроны, участвующие в реакции.
- В одной полуячейке растворенные катионы металла-B объединяются со свободными электронами, которые доступны на границе раздела между раствором и электродом металла-B; эти катионы тем самым нейтрализуются, заставляя их осадок из раствора в виде отложений на электроде металла-B, процесс, известный как покрытие.
- Эта реакция восстановления заставляет свободные электроны по всему электроду металла-B, проволоке и электроду металла-A втягиваться в электрод металла-B. Следовательно, электроны отталкиваются от некоторых атомов электрода металла-A, как если бы катионы металла-B реагировали с ними напрямую; эти атомы металла-A становятся катионами, которые растворяются в окружающем растворе.
- По мере продолжения этой реакции в полуячейке с электродом металла-A образуется положительно заряженный раствор (потому что в нем растворяются катионы металла-A), в то время как в другой полуячейке образуется отрицательно заряженный раствор (поскольку катионы металла-B выпадать из него в осадок, оставляя после себя анионы); неослабевая, этот дисбаланс в ответственности остановит реакцию. Растворы полуэлементов соединены солевым мостиком или пористой пластиной, которая позволяет ионам переходить от одного раствора к другому, что уравновешивает заряды растворов и позволяет реакции продолжаться.
По определению:
- В анод - электрод, на котором происходит окисление (потеря электронов) (электрод металл-А); в гальваническом элементе это отрицательный электрод, потому что при окислении электроны остаются на электроде.[10] Эти электроны затем проходят через внешнюю цепь к катоду (положительный электрод) (в то время как при электролизе электрический ток движет поток электронов в противоположном направлении, а анод является положительным электродом).
- В катод - электрод, на котором происходит восстановление (усиление электронов) (электрод металл-В); в гальваническом элементе это положительный электрод, так как ионы восстанавливаются, забирая электроны с электрода и снимая пластину (в то время как при электролизе катод является отрицательной клеммой и притягивает положительные ионы из раствора). В обоих случаях утверждение КотХод привлекает Котions 'верно.
Гальванические элементы по своей природе производят постоянный ток. В Клетка Вестона имеет анод, состоящий из кадмий Меркурий амальгама, и катод из чистой ртути. Электролит представляет собой (насыщенный) раствор сульфат кадмия. В деполяризатор представляет собой пасту сульфата ртути. Когда раствор электролита насыщен, напряжение ячейки очень воспроизводимо; следовательно, в 1911 году он был принят как международный стандарт напряжения.
Батарея - это набор гальванических элементов, которые соединены вместе и образуют единый источник напряжения. Например, типичный 12В свинцово-кислотная батарея имеет шесть подключенных гальванических ячеек последовательно с анодами из свинца и катодами из диоксида свинца, оба погружены в серную кислоту. Большой аккумуляторные, например, в обмен телефонами Обеспечивая питание телефонов пользователей центрального офиса, ячейки могут быть подключены как последовательно, так и параллельно.
Напряжение ячейки
Напряжение (электродвижущая сила Eо), производимый гальваническим элементом, можно оценить по стандартной Свободная энергия Гиббса изменение электрохимической реакции согласно
куда νе - количество электронов, перенесенных в уравновешенных полуреакциях, и F является Постоянная Фарадея. Однако его можно определить более удобно, используя стандартная таблица потенциалов для двоих полуклетки участвует. Первый шаг - идентифицировать два металла и их ионы, взаимодействующие в клетке. Затем каждый смотрит вверх стандартный электродный потенциал,Eо, в вольт, для каждого из двух половина реакции. Стандартный потенциал ячейки равен более положительному Eо значение минус более отрицательное Eо ценить.
Например, на рисунке выше растворы CuSO4 и ZnSO4. В каждом растворе есть соответствующая металлическая полоска и солевой мостик или пористый диск, соединяющий два раствора и позволяющий ТАК2−
4 ионы свободно перемещаются между растворами меди и цинка. Чтобы вычислить стандартный потенциал, ищем полуреакции меди и цинка и находят:
- Cu2+ + 2
е−
⇌ Cu Eо = +0,34 В - Zn2+ + 2
е−
⇌ Zn Eо = −0,76 В
Таким образом, общая реакция такова:
- Cu2+ + Zn ⇌ Cu + Zn2+
Стандартный потенциал для реакции равен +0,34 В - (-0,76 В) = 1,10 В. Полярность ячейки определяется следующим образом. Металлический цинк восстанавливает сильнее, чем металлическая медь, потому что стандартный (восстановительный) потенциал цинка более отрицательный, чем у меди. Таким образом, металлический цинк теряет электроны на ионы меди и развивает положительный электрический заряд. В константа равновесия, K, для ячейки задается
куда F это Постоянная Фарадея, р это газовая постоянная и Т это температура в кельвины. Для ячейки Даниэля K примерно равно 1.5×1037. Таким образом, в состоянии равновесия переносится несколько электронов, достаточное для зарядки электродов.[11]
Фактические потенциалы полуэлементов должны быть рассчитаны с использованием Уравнение Нернста поскольку растворенные вещества вряд ли будут в своем стандартном состоянии,
куда Q это коэффициент реакции. Когда заряды ионов в реакции равны, это упрощается до
где {Mп+} это Мероприятия иона металла в растворе. На практике вместо активности используется концентрация в моль / л. Металлический электрод находится в стандартном состоянии, поэтому по определению имеет единичную активность. Потенциал всей клетки получается как разность потенциалов двух полуэлементов, поэтому он зависит от концентраций обоих растворенных ионов металла. Если концентрации одинаковы, и уравнение Нернста не требуется в предполагаемых здесь условиях.
Стоимость 2.303р/F является 1.9845×10−4 В / К, поэтому при 25 ° C (298,15 K) потенциал полуячейки изменится всего на 0,05918 В /νе если концентрация иона металла увеличивается или уменьшается в 10 раз.
Эти расчеты основаны на предположении, что все химические реакции находятся в равновесии. Когда в цепи протекает ток, условия равновесия не достигаются, и напряжение ячейки обычно снижается с помощью различных механизмов, таких как развитие перенапряжения.[12] Кроме того, поскольку химические реакции происходят, когда ячейка вырабатывает электроэнергию, концентрация электролита изменяется, а напряжение ячейки снижается. Следствием температурной зависимости стандартных потенциалов является то, что напряжение, создаваемое гальваническим элементом, также зависит от температуры.
Гальваническая коррозия
Гальваническая коррозия - это электрохимический эрозия металлов. Коррозия возникает, когда два разнородных металла контактируют друг с другом в присутствии электролит, например, соленая вода. При этом образуется гальванический элемент с образованием газообразного водорода на более благородном (менее активном) металле. Результирующий электрохимический потенциал затем создает электрический ток, который электролитически растворяет менее благородный материал. А ячейка концентрации может образоваться, если один и тот же металл подвергается воздействию двух разных концентраций электролита.
Типы клеток
- Концентрационная ячейка
- Электролитическая ячейка
- Электрохимическая ячейка
- Лимонная батарея
- Термогальваническая ячейка
Смотрите также
Рекомендации
- ^ "батарея" (по умолчанию 4b), Онлайн-словарь Merriam-Webster (2008). Проверено 6 августа 2008 года.
- ^ Кейтли, Джозеф Ф (1999). Дэниэл Селл. Джон Уайли и сыновья. С. 49–51. ISBN 978-0-7803-1193-0.
- ^ Кипнис, Наум (2003) «Изменение теории: случай контактного электричества Вольта», Нуова Вольтиана, Vol. 5. Università degli studi di Pavia, 2003 г. ISBN 88-203-3273-6. стр. 144–146
- ^ Кларк, Эдвин; Яцина, Л. С. (1992) Истоки нейронаучных концепций девятнадцатого века, Калифорнийский университет Press. ISBN 0-520-07879-9. п. 199
- ^ "Вехи: изобретение электрических батарей Вольта, 1799 г.". Сеть глобальной истории IEEE. IEEE. Получено 26 июля 2011.
- ^ Оствальд, Вильгельм (1980). Электрохимия: история и теория.
- ^ Хотон, Брайан (2007) Скрытая история: потерянные цивилизации, тайные знания и древние тайны. Карьера Пресса. ISBN 1564148971. стр. 129–132
- ^ Ashcroft, N.W .; Мермин, Н. Д. (1976). Физика твердого тела. Форт-Уэрт, Техас: Харкорт.
- ^ а б c d е Шмидт-Рор, К. (2018). «Как аккумуляторы накапливают и выделяют энергию: объяснение основ электрохимии» «J. Chem. Educ.» 95: 1801-1810 https://dx.doi.org/10.1021/acs.jchemed.8b00479
- ^ «Введение в окислительно-восстановительное равновесие». Chemguide. Получено 20 июля 2014.
- ^ Аткинс, П; де Паула (2006). Физическая химия. J. (8-е изд.). Издательство Оксфордского университета. ISBN 978-0-19-870072-2. Глава 7, разделы «Равновесная электрохимия»
- ^ Аткинс, П; де Паула (2006). Физическая химия. J. (8-е изд.). Издательство Оксфордского университета. ISBN 978-0-19-870072-2. Раздел 25.12 «Рабочие гальванические элементы»
внешняя ссылка
- Как построить гальваническую батарею с MiniScience.com
- Гальванический элемент, анимация
- Интерактивная анимация гальванического элемента. Исследовательская группа химического образования, Государственный университет Айовы.
- Реакции переноса электрона и окислительно-восстановительные потенциалы в ячейках GALVANIc - что происходит с ионами на границе раздела фаз (NERNST, FARADAY) (Видео SciFox на TIB AV-Portal)






![{ displaystyle E _ { text {half-cell}} = E ^ {o} - { frac {0.05918 { text {V}}} { nu _ {e}}} log _ {10} слева [{ text {M}} ^ {n +} right]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6a037534b006cae64ae53d028a0cc0212beab99d)
