Литий-серная батарея - Lithium–sulfur battery
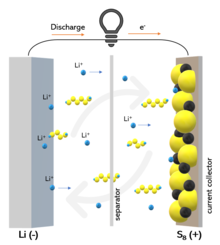 Принцип работы литий-серной батареи и эффект «челнока» | |
| Удельная энергия | 1,800,000 J /кг продемонстрировал |
|---|---|
| Плотность энергии | 1,260,000 J /L |
| Эффективность заряда / разряда | C / 5 номинальный |
| Долговечность цикла | оспаривается |
| Номинальное напряжение ячейки | клетка Напряжение изменяется нелинейно в диапазоне 2,5–1,7 V во время разряда; аккумуляторы часто упаковываются по 3 V |
В литий-серная батарея (Li – S аккумулятор) - это тип аккумуляторная батарея, отличающийся высоким удельная энергия.[1] Низкий атомный вес из литий и умеренный атомный вес сера означает, что Li – S батареи относительно легкие (примерно по плотности воды). Они использовались на самых длинных и высотных беспилотных питаемый солнечной энергией полет на самолете (в то время) Зефир 6 в августе 2008 г.[2]
Литий-серные батареи могут быть успешными литий-ионный ячеек из-за их более высокой плотности энергии и меньшей стоимости за счет использования сера.[3] Некоторые Li – S аккумуляторы имеют удельную энергию порядка 500 Wh /кг, значительно лучше, чем у большинства литий-ионных аккумуляторов, которые находятся в диапазоне 150–250 Втч / кг. Были продемонстрированы Li – S аккумуляторы, выдерживающие до 1500 циклов заряда и разряда,[4] но циклические испытания на долговечность в промышленных масштабах и с обедненным электролитом все еще необходимы. По состоянию на начало 2014 года в продаже не было.[5] Ключевой проблемой Li – S аккумуляторов является эффект полисульфидного «челнока», ответственный за постепенную утечку активного материала с катода, что приводит к сокращению срока службы аккумулятора.[6] Более того, чрезвычайно низкая электропроводность серного катода требует дополнительной массы для проводящего агента, чтобы использовать весь вклад активной массы в емкость.[7] Большое объемное расширение серного катода от S до Li2S и большое количество необходимого электролита также являются проблемами, которые необходимо решить.
История
Изобретение Li-S батарей восходит к 1960-м годам, когда Герберт и Улам запатентовали в 1962 году первичную батарею, в которой использовался литий или литиевые сплавы в качестве анодного материала, сера в качестве катодного материала и электролит, состоящий из алифатический насыщенный амины.[8][9] Спустя несколько лет технология была улучшена за счет введения органических растворителей в качестве ПК, ДМСО и DMF получение АКБ на 2.35-2.5 В.[10] К концу 1980-х была продемонстрирована перезаряжаемая Li – S батарея на основе эфиров, в частности ДОЛ, как растворитель электролита.[11][12] Благодаря научным достижениям в этой области был подчеркнут потенциал Li – S батарей. Аккумуляторы Li – S за последние двадцать лет снова стали популярными. В частности, стратегии ингибирования или смягчения эффекта полисульфидного «челнока» были глубоко изучены и были объектом изучения многих исследователей.
Manthiram определила критические параметры, необходимые для перехода литиево-серных батарей к коммерческому использованию.[13][14] В частности, литиево-серные батареи должны обеспечивать содержание серы> 5 мг / см3.−2, содержание углерода <5%, отношение электролита к сере <5 мкл мг−1, отношение электролита к емкости <5 мкл (мА · ч)−1и соотношение отрицательной и положительной емкости <5 в ячейках мешочного типа.[13]
По состоянию на 2017 год вышло 700 публикаций.[15]
Химия
Химические процессы в ячейке Li – S включают растворение лития из анод поверхность (и включение в щелочной металл полисульфид соли ) во время разряда, а обратный литиевый покрытие к аноду во время зарядки.[16]
Анод
На анодной поверхности происходит растворение металлического лития с образованием электронов и ионов лития во время разряда и электроосаждения во время заряда. В полуреакция выражается как:[17]
По аналогии с литиевыми батареями, реакция растворения / электроосаждения со временем вызывает проблемы нестабильного роста границы раздела твердый электролит (SEI), генерируя активные центры для зарождение и дендритный рост лития. Рост дендритов ответственен за внутреннее короткое замыкание в литиевых батареях и приводит к смерти самой батареи.[18]
Катод
В Li-S батареях энергия накапливается в серном электроде (S8). Во время разряда ионы лития в электролите мигрируют к катоду, где сера восстанавливается до сульфид лития (Li2S). Сера повторно окисляется до S8 во время фазы заправки. Таким образом, полуреакция выражается как:
(E ° ≈ 2,15 В относительно Li / Li+ )
На самом деле реакция восстановления серы до сульфида лития намного сложнее и включает образование полисульфидов лития (Li2SИкс, 2 ≤ Икс ≤ 8) при уменьшении длины цепочки по порядку:[19]
Конечный продукт на самом деле представляет собой смесь Li2S2 и Ли2S, а не чистый Li2S из-за медленной кинетики восстановления при Li2С.[20] Это контрастирует с обычными литий-ионными элементами, в которых ионы лития вставленный в аноде и катодах. Каждый атом серы может вместить два иона лития. Как правило, литий-ионные батареи содержат только 0,5–0,7 ионов лития на один атом хозяина.[21] Следовательно, Li – S обеспечивает гораздо более высокую плотность хранения лития. Полисульфиды - это уменьшенный на поверхности катода в последовательности при разрядке элемента:
- S
8 → Ли
2S
8 → Ли
2S
6 → Ли
2S
4 → Ли
2S
3
Через пористый диффузионный сепаратор сера полимеры форма в катод по мере заряда ячейки:
- Ли
2S → Ли
2S
2 → Ли
2S
3 → Ли
2S
4 → Ли
2S
6 → Ли
2S
8 → S
8
Эти реакции аналогичны реакциям в натриево-серная батарея.
Основные проблемы Li – S аккумуляторов - низкая проводимость серы и значительное изменение ее объема при разрядке, и поиск подходящего катода является первым шагом к коммерциализации Li – S аккумуляторов.[22] Поэтому большинство исследователей используют катод углерод / сера и литиевый анод.[23] Сера очень дешевая, но практически не имеет электропроводность, 5×10−30 S ⋅см−1 в 25 ° C.[24] Углеродное покрытие обеспечивает недостающую электропроводность. Углеродные нановолокна обеспечивают эффективный путь электронной проводимости и структурную целостность, но при этом их стоимость невысока.[25]
Одна из проблем конструкции литий-сера заключается в том, что, когда сера в катоде поглощает литий, объемное расширение LiИксS составов происходит, и прогнозируемое расширение объема Li2S составляет почти 80% от объема исходной серы.[26] Это вызывает большие механические напряжения на катоде, что является основной причиной быстрой деградации. Этот процесс уменьшает контакт между углеродом и серой и предотвращает поток ионов лития к поверхности углерода.[27]
Механические свойства литиированных соединений серы в значительной степени зависят от содержания лития, и с увеличением содержания лития прочность литиированных соединений серы улучшается, хотя это увеличение не является линейным с литиированием.[28]
Одним из основных недостатков большинства Li – S ячеек являются нежелательные реакции с электролитами. Пока S и Ли
2S относительно нерастворимы в большинстве электролитов, многие промежуточные полисульфиды - нет. Растворение Ли
2S
п в электролиты вызывает необратимую потерю активной серы.[29] Использование высокореактивного лития в качестве отрицательного электрода вызывает диссоциацию большинства обычно используемых электролитов другого типа. Было изучено использование защитного слоя на поверхности анода для повышения безопасности электролизера, т.е. Тефлон покрытие показало улучшение стабильности электролита,[30] ЛИПОН, Ли3N также показал многообещающие результаты.
Полисульфидный «шаттл»
Исторически сложилось так, что эффект «челнока» является основной причиной деградации Li – S батареи.[31] Полисульфид лития Li2SИкс (6≤x≤8) хорошо растворим[32] в обычных электролитах, используемых для Li – S аккумуляторов. Они образуются и утекают с катода, и они диффундируют к аноду, где они восстанавливаются до полисульфида с короткой цепью и диффундируют обратно к катоду, где снова образуются полисульфиды с длинной цепью. Этот процесс приводит к постоянной утечке активного материала с катода, коррозии лития, низкой кулоновской эффективности и малому сроку службы батареи.[33] Кроме того, эффект «челнока» ответственен за характерный саморазряд Li – S аккумуляторов из-за медленного растворения полисульфида, который также происходит в состоянии покоя.[31] Эффект «челнока» в Li – S батарее можно количественно оценить с помощью фактора f.c (0
куда ks, qвверх, [Sмалыш] и яc - соответственно кинетическая постоянная, удельная емкость, влияющая на анодное плато, общая концентрация серы и ток заряда.
Электролит
Обычно в Li – S батареях используется жидкий органический электролит, содержащийся в порах полипропиленового сепаратора.[31] Электролит играет ключевую роль в Li – S батареях, воздействуя как на эффект «челнока» за счет растворения полисульфида, так и на стабилизацию SEI на поверхности анода. Было продемонстрировано, что электролиты на основе органических карбонатов, обычно используемые в литий-ионных аккумуляторах (например, ПК, EC, DEC и их смеси) несовместимы с химическим составом Li – S батарей.[35] Полисульфиды с длинной цепью подвергаются нуклеофильной атаке на электрофильные участки карбонатов, что приводит к необратимому образованию побочных продуктов в виде этиловый спирт, метанол, этиленгликоль и тиокарбонаты. В Li – S батареях обычно используются циклические эфиры (как ДОЛ ) или короткоцепочечные эфиры (как DME ), а также семейство простых эфиров гликоля, включая DEGDME и TEGDME.[36] Один общий электролит - 1M LiTFSI в DOL: DME 1: 1 об. с 1% по весу LiNO3 в качестве добавки для пассивации поверхности литием.[36]
Безопасность
Из-за высокой плотности потенциальной энергии и нелинейной реакции разряда и заряда элемента микроконтроллер и другие схемы безопасности иногда используются вместе с регуляторы напряжения для управления работой ячейки и предотвратить быструю разрядку.[37]
Исследование
| Анод | Катод | Дата | Источник | Удельная мощность после цикла | Примечания |
|---|---|---|---|---|---|
| Литий металлический | Полиэтиленгликоль мезопористый углерод с ямками с покрытием | 17 мая 2009 г. | Университет Ватерлоо[38] | 1,110 мА⋅ч / г после 20 циклов при токе 168 мА⋅г−1[38] | Минимальная деградация во время цикла зарядки. Чтобы удерживать полисульфиды на катоде, поверхность была функционализирована так, чтобы отталкивать (гидрофобные) полисульфиды. В тесте с использованием глим растворителя, традиционный серный катод потерял 96% серы за 30 циклы, а экспериментальный катод потерял всего 25%. |
| Литий металлический | Покрытые серой неупорядоченные углеродные полые углеродные нановолокна | 2011 | Стэндфордский Университет[39][40] | 730 мА⋅ч / г после 150 циклов (при 0,5 C) | Добавка электролита повысила эффективность Фарадея от 85% до более 99%. |
| Кремниевая нанопроволока / углерод | Неупорядоченные углеродные нанотрубки с серным покрытием, изготовленные из углеводов | 2013 | CGS[41][42] | 1,300 мА⋅ч / г после 400 циклов (при 1 C) | Микроволновая обработка материалов и лазерная печать электродов. |
| Кремний-углерод | Сера | 2013 | Институт Фраунгофера по материалам и балочным технологиям IWS[43] | ? после 1400 циклов | |
| Сополимеризованный сера | 2013 | Университет Аризоны[44][45] | 823 мА⋅ч / г при 100 циклах | Использует обратный вулканизация "в основном на сере с небольшим количеством добавки 1,3-диизопропенилбензола (ДИБ) | |
| Пористый TiO 2-инкапсулированные наночастицы серы | 2013 | Стэндфордский Университет[46][47] | 721 мА⋅ч / г при 1000 циклах (0,5 C) | Оболочка защищает серно-литиевый промежуточный продукт от растворителя электролита. Каждая катодная частица имеет диаметр 800 нанометров. Эффективность Фарадея 98,4%. | |
| Сера | июнь 2013 | Национальная лаборатория Окриджа | 1200 мА · ч / г при 300 циклах при 60 ° С (0,1 C) 800 мА · ч / г при 300 циклах при 60 ° С (1 C)[48] | Электролит твердый полисульфидофосфат лития. Половина напряжения типичных LIB. К остающимся проблемам относятся низкая ионная проводимость электролита и хрупкость керамической структуры.[49][50] | |
| Литий | Сераоксид графена нанокомпозит с стирол-бутадиен -карбоксиметилцеллюлоза сополимерное связующее | 2013 | Национальная лаборатория Лоуренса Беркли[51] | 700 мА · ч / г при 1500 циклах (0,05 C разряд) 400 мА · ч / г при 1500 циклах (0,5 Заряд C / 1 C разряд) | Напряжение от 1,7 до 2,5 В в зависимости от уровня заряда. Бис (трифторметансульфонил) имид), растворенный в смеси нметил- (н-бутил) пирролидиния бис (трифторметансульфонил) -имида (PYR14TFSI), 1,3-диоксолана (DOL), диметоксиэтана (DME) с 1 M бис- (трифторметилсульфонил) имид лития (LiTFSI) и нитрат лития (LiNO 3). Сепаратор из полипропилена с высокой пористостью. Удельная энергия 500 Вт⋅ч / кг (начальное) и 250 Вт⋅ч / кг при 1500 циклах (C = 1,0) |
| Литированный графит | Сера | Февраль 2014 | Тихоокеанская Северо-Западная национальная лаборатория | 400 циклов | Покрытие предотвращает разрушение анода полисульфидами.[52] |
| Литированный графен | Пассивирующий слой серы / сульфида лития | 2014 | OXIS Energy[53][54] | 240 мА · ч / г (1000 циклов) 25 А · ч / ячейка | Пассивирующий слой предотвращает потерю серы |
| Литированный твердый углерод | Сополимер серы (поли (S-co-DVB)) | 2019 | Национальный университет Чунгнам | 400 мАч / г на 500 циклов при 3 ° C | SEI твердого углерода предотвращает осаждение полисульфидов на аноде и обеспечивает высокую производительность.[55] |
| Литий-серные батареи | Углеродные нанотрубки / сера | 2014 | Университет Цинхуа[56] | 15.1 мА · ч⋅см−2 при содержании серы 17,3 мгS⋅см−2 | Был изготовлен автономный бумажный электрод CNT – S с высокой поверхностной загрузкой серы, в котором короткие MWCNT служили электропроводящей сетью на малых расстояниях, а сверхдлинные УНТ действовали как проводящая сеть на большие расстояния, так и как скрещенные связующие. |
| Покрытая стеклом сера с умеренно восстановленным оксид графена для структурной поддержки | 2015 | Калифорнийский университет, Риверсайд[57] | 700 mA⋅h⋅g−1 (50 циклов)[58] | Стеклянное покрытие предотвращает постоянную миграцию полисульфидов лития на электрод | |
| Литий | Сера | 2016 | ЛИТАТ | 500 Вт⋅ч / кг | Проект ALISE H2020 по разработке Li – S аккумуляторной батареи для автомобилей с новыми компонентами, оптимизированными в отношении анода, катода, электролита и сепаратора. |
Коммерциализация
По состоянию на 2015 год немногие компании смогли коммерциализировать технологию в промышленных масштабах. Такие компании, как Sion Power, сотрудничают с Airbus Defense and Space протестировать технологию литий-серных батарей. Airbus Defense and Space успешно запустила свой прототип Псевдоспутник на большой высоте (HAPS) самолет, работающий от солнечной энергии днем и от литиево-серных батарей ночью в реальных условиях в течение 11-дневного полета. В батареях, использованных в испытательном полете, использовались Li – S элементы Sion Power, обеспечивающие 350 Вт kgч / кг.[59] Первоначально компания Sion утверждала, что находится в процессе массового производства, которое будет доступно к концу 2017 года, однако в последнее время можно увидеть, что они отказались от работы над своим литий-серным тестом в пользу литий-металлической батареи.[60][61].
Британская фирма OXIS Energy разработала прототип литий-серных батарей.[62][63] Вместе с Имперский колледж Лондон и Крэнфилдский университет они опубликовали схема замещения модели для своих ячеек.[64] В компании Lithium Balance из Дании они построили прототип аккумуляторной системы для скутеров в первую очередь для китайского рынка. Аккумулятор прототипа имеет емкость 1,2 кВтч с использованием 10 Элементы Ah Long Life весят на 60% меньше, чем свинцово-кислотные батареи со значительным увеличением дальности действия.[65] Они также построили 3U, 3000 С аккумулятором в стойку, который весит всего 25 кг и полностью масштабируется.[66] Они ожидают, что их литий-серные батареи будут стоить около 200 долларов за киловатт-час при массовом производстве.[67] Фирма также участвовала в проекте Европейского консорциума по производству литий-серной энергии для космической среды (ECLIPSE) H2020. В рамках этого проекта разрабатываются литий-ионные батареи большой емкости для спутников и ракет-носителей.[68]
Sony, которая также выпустила на рынок первую литий-ионную батарею, планирует вывести на рынок литий-серные батареи в 2020 году.[69]
Кафедра машиностроения и аэрокосмической техники Университета Монаша в Мельбурне, Австралия, разработала Li-S аккумулятор сверхвысокой емкости, который был изготовлен партнерами из Института материалов и лучевых технологий им. Фраунгофера в Германии. Утверждается, что аккумулятор может обеспечивать питание смартфона в течение пяти дней. [70]
Смотрите также
Рекомендации
- ^ Чжан, Шэн С (2013). «Литий-серная батарея с жидким электролитом: фундаментальная химия, проблемы и решения». Журнал источников энергии. 231: 153–162. Дои:10.1016 / j.jpowsour.2012.12.102.
- ^ Амос, Дж. (24 августа, 2008 г.) «Солнечный самолет совершил рекордный полет» Новости BBC
- ^ Мантирам, Арумугам; Фу, Юнчжу; Су, Юй-Шэн (2013). «Проблемы и перспективы литий-серных аккумуляторов» (PDF). Соотв. Chem. Res. 46: 1125–1134. Дои:10.1021 / ar300179v. Архивировано из оригинал (PDF) на 2020-01-03.
- ^ «Технология литий-серных батарей OXIS Energy». Получено 2017-05-20.
- ^ «Новый литий-серный аккумулятор вдвое увеличивает удельную энергию литий-ионного». NewAtlas.com. 2 декабря 2013 г.. Получено 2014-02-18.
- ^ Дяо, Ян; Се, Кай; Сюн, Шичжао; Хун, Сяобинь (август 2013 г.). «Феномен челнока - необратимый механизм окисления активного материала серы в Li – S батарее». Журнал источников энергии. 235: 181–186. Дои:10.1016 / j.jpowsour.2013.01.132.
- ^ Эфтехари, Али (2017). «Подъем литий-селеновых батарей». Устойчивая энергетика и топливо. 1: 14–29. Дои:10.1039 / C6SE00094K.
- ^ США 3043896A
- ^ США 3532543A
- ^ США 3413154A
- ^ Пелед, Э .; Горенштейн, А .; Сигал, М .; Штернберг, Ю. (май 1989 г.). «Литий-серная аккумуляторная батарея (расширенная аннотация)». Журнал источников энергии. 26 (3–4): 269–271. Bibcode:1989JPS .... 26..269P. Дои:10.1016/0378-7753(89)80133-8.
- ^ Пелед Э. (1989). «Литий-серная батарея: оценка электролитов на основе диоксолана». Журнал Электрохимического общества. 136 (6): 1621. Дои:10.1149/1.2096981.
- ^ а б Бхаргав, Амрут; Цзяжуй, Хе (2020). «Литий-серные аккумуляторы: достижение критических показателей». Джоуль. 4: 285–291. Дои:10.1016 / j.joule.2020.01.001.
- ^ Мантирам, Арумугам; Фу, Юнчжу; Чунг, Шэн-Хэн; Зу, Чэньси; Су, Юй-Шэн (2014). «Литий-серные аккумуляторные батареи». Химические обзоры. 114: 11751–11787. Дои:10.1021 / cr500062v.
- ^ Кумар, Рудра; Лю, Цзе; Хван, Чан Ён; Сунь, Ян-Кук (2018). «Последние тенденции исследований Li – S аккумуляторов». Журнал химии материалов A. 6 (25): 11582–11605. Дои:10.1039 / C8TA01483C. ISSN 2050-7488.
- ^ Тудрон, Ф. Б., Акридж, Дж. Р., Пуглиси, В. Дж. (2004) "Литий-серные аккумуляторные батареи: характеристики, состояние разработки и применимость для питания портативной электроники" (Тусон, Аризона: Сион Пауэр)
- ^ Кумар, Рудра; Лю, Цзе; Хван, Чан-Ён (2018). «Последние тенденции исследований Li – S аккумуляторов». Журнал химии материалов A. 6 (25): 11582–11605. Дои:10.1039 / C8TA01483C. Получено 2019-07-04.
- ^ Ульд Эли, Тейеб; Камзабек, Дана; Чакраборти, Дхритиман (29.05.2018). «Литий-серные аккумуляторы: современное состояние и направления на будущее». ACS Applied Energy Materials. 1 (5): 1783–1814. Дои:10.1021 / acsaem.7b00153.
- ^ Линь, Жан; Лян, Чэнду (2015). «Литий-серные батареи: от жидких к твердым элементам». Журнал химии материалов A. 3 (3): 18. Дои:10.1039 / C4TA04727C. OSTI 1185628. Получено 2019-07-04.
- ^ Сон, Мин-Гю; Кэрнс, Элтон Дж .; Чжан, Юэган (2013). «Литий-серные батареи с высокой удельной энергией: старые вызовы и новые возможности». Наномасштаб. 5 (6): 2186–204. Bibcode:2013Nanos ... 5.2186S. Дои:10.1039 / c2nr33044j. PMID 23397572. Получено 2019-07-04.
- ^ Буллис, Кевин (22 мая 2009 г.). «Возвращаясь к литий-серным батареям». Обзор технологий. Получено 12 августа, 2016.
- ^ Эфтехари, А. (2017). «Катодные материалы для литий-серных батарей: практическая перспектива». Журнал химии материалов A. 5 (34): 17734–17776. Дои:10.1039 / C7TA00799J.
- ^ Choi, Y.J .; Ким, К. (2008). «Улучшение цикличности серного электрода для литиево-серной батареи». Журнал сплавов и соединений. 449 (1–2): 313–316. Дои:10.1016 / j.jallcom.2006.02.098.
- ^ J.A. Дин, изд. (1985). Справочник Ланге по химии (третье изд.). Нью-Йорк: Макгроу-Хилл. стр.3–5.
- ^ Choi, Y.J .; Chung, Y.D .; Baek, C. Y .; Kim, K. W .; Ан, Дж. Х. (4 марта 2008 г.). «Влияние углеродного покрытия на электрохимические свойства серного катода для литиево-серного элемента». J. Источники энергии. 184 (2): 548–552. Bibcode:2008JPS ... 184..548C. Дои:10.1016 / j.jpowsour.2008.02.053.
- ^ Ислам, М. Махбубул; Остадхоссейн, Алиреза; Бородин, Олег; Йейтс, А. Тодд; Типтон, Уильям В .; Хенниг, Ричард Дж .; Кумар, Нитин; Дуин, Адри К. Т. ван (21 января 2015 г.). «Моделирование молекулярной динамики ReaxFF на катодных материалах с литированной серой». Phys. Chem. Chem. Phys. 17 (5): 3383–3393. Bibcode:2015PCCP ... 17.3383I. Дои:10.1039 / c4cp04532g. PMID 25529209.
- ^ Брайан Додсон, «Новый литий-серный аккумулятор вдвое увеличивает удельную энергию литий-ионного», Новый Атлас, 1 декабря 2013 г.
- ^ Ислам; и другие. (2015). «Моделирование молекулярной динамики ReaxFF на катодных материалах с литированной серой». Phys. Chem. Chem. Phys. 17 (5): 3383–3393. Bibcode:2015PCCP ... 17.3383I. Дои:10.1039 / C4CP04532G. PMID 25529209.
- ^ Jeong, S. S .; Lim, Y .; Choi, Y.T .; Kim, K. W .; Ahn, H.J .; Чо, К. К. (2006). «Электрохимические свойства литий-серных элементов с использованием полимерных электролитов PEO, полученных при трех различных условиях смешивания». J. Источники энергии. 174 (2): 745–750. Bibcode:2007JPS ... 174..745J. Дои:10.1016 / j.jpowsour.2007.06.108.
- ^ Ислам, М. Махбубул; Брянцев, Вячеслав С .; ван Дуин, Адри CT (2014). «Моделирование реактивного силового поля ReaxFF на влияние тефлона на разложение электролита при анодном разряде Li / SWCNT в литий-серных батареях» (PDF). Журнал Электрохимического общества. 161 (8): E3009 – E3014. Дои:10.1149 / 2.005408jes.
- ^ а б c Мантирам, Арумугам; Фу, Юнчжу; Чунг, Шэн-Хэн; Зу, Чэньси; Су Юй-Шэн (10.12.2014). «Литий-серные аккумуляторные батареи». Химические обзоры. 114 (23): 11751–11787. Дои:10.1021 / cr500062v. ISSN 0009-2665. PMID 25026475.
- ^ Чжан, Кинтао (2018). Химически полученный графен: функционализация, свойства и приложения (иллюстрированный ред.). Королевское химическое общество. п. 224. ISBN 978-1-78801-080-1. Выдержка страницы 224
- ^ Сон, Мин-Гю; Кэрнс, Элтон Дж .; Чжан, Юэган (2013). «Литий-серные батареи с высокой удельной энергией: старые вызовы и новые возможности». Наномасштаб. 5 (6): 2186–204. Bibcode:2013Nanos ... 5.2186S. Дои:10.1039 / c2nr33044j. ISSN 2040-3364. PMID 23397572.
- ^ Михайлик, Юрий В .; Акридж, Джеймс Р. (2004). «Исследование полисульфидного челнока в системе Li / S аккумуляторных батарей». Журнал Электрохимического общества. 151 (11): A1969. Дои:10.1149/1.1806394.
- ^ Йим, Тэын; Парк, Мин-Сик; Ю, Джи-Санг; Ким, Ки Джэ; Им, Кын Юнг; Ким, Джэ-Хун; Чон, Гуджин; Джо, Йонг Нам; Ву, Санг-Гиль (сентябрь 2013 г.). «Влияние химической активности полисульфида по отношению к электролиту на основе карбоната на электрохимические характеристики Li – S батарей». Electrochimica Acta. 107: 454–460. Дои:10.1016 / j.electacta.2013.06.039.
- ^ а б Шеерс, Йохан; Фантини, Себастьян; Йоханссон, Патрик (июнь 2014 г.). «Обзор электролитов для литий-серных батарей». Журнал источников энергии. 255: 204–218. Bibcode:2014JPS ... 255..204S. Дои:10.1016 / j.jpowsour.2014.01.023.
- ^ Акридж, Дж. Р. (октябрь 2001 г.) «Безопасность литиево-серных аккумуляторных батарей» Продукты и технологии для аккумуляторов
- ^ а б Сюлей Джи, Кю Тэ Ли и Линда Ф. Назар. (17 мая 2009 г.)«Высокоупорядоченный наноструктурированный катод углерод-сера для литий-серных батарей». Материалы Природы
- ^ Гуанюань, Чжэн; Юань Ян; Джуди Дж. Ча; Сеунг Сэ Хонг; И Цуй (14 сентября 2011 г.). «Серные катоды, инкапсулированные полым углеродом с нановолокном для литиевых аккумуляторных батарей высокой удельной емкости» (PDF). Нано буквы. 11 (10): 4462–4467. Bibcode:2011NanoL..11.4462Z. Дои:10.1021 / nl2027684. PMID 21916442.
- ^ Келлер, Сара Джейн (4 октября 2011 г.). «Сера в полых нановолокнах решает проблемы, связанные с конструкцией литий-ионных батарей». Stanford News. Стэндфордский Университет. Получено 18 февраля, 2012.
- ^ Розенберг, Сара; Хинтеннах (1 апреля 2014 г.). «Литий-серные микроэлектроды для Li / S аккумуляторов с лазерной печатью». Российский журнал электрохимии. 50 (4): 327–335. Дои:10.1134 / S1023193514040065.
- ^ Ванденберг, Аврелий; Хинтеннах (1 апреля 2014 г.). «Новый подход к дизайну литий-серных батарей». Российский журнал электрохимии. 50 (4): 317–326. Дои:10.1134 / S102319351306013X.
- ^ «Исследователи увеличивают срок службы литий-серных батарей». Gizmag.com. 4 апреля 2013 г.. Получено 2013-12-04.
- ^ Chung, W. J .; Griebel, J. J .; Kim, E.T .; Юн, H .; Simmonds, A. G .; Ji, H.J .; Dirlam, P.T .; Glass, R. S .; Wie, J. J .; Nguyen, N.A .; Guralnick, B.W .; Park, J .; Somogyi, Á. D .; Theato, P .; MacKay, M.E .; Sung, Y. E .; Char, K .; Пьюн, Дж. (2013). «Использование элементарной серы в качестве альтернативного сырья для полимерных материалов». Химия природы. 5 (6): 518–524. Bibcode:2013НатЧ ... 5..518С. Дои:10.1038 / nchem.1624. PMID 23695634.
- ^ Кэрил Ричардс (2013-04-16). «Радикальный подход к превращению серы в полимеры».
- ^ Национальная ускорительная лаборатория SLAC (6 сообщений) (2013-01-08). «Мировой рекорд производительности батареи достигнут с помощью яичных наноструктур». CleanTechnica. Получено 2013-06-11.
- ^ Wei Seh, Z .; Li, W .; Cha, J. J .; Zheng, G .; Ян, Й .; McDowell, M.T .; Hsu, P.C .; Цуй, Ю. (2013). «Наноархитектура сера – TiO2 желток – оболочка с внутренними пустотами для литий – серных аккумуляторов длительного цикла». Nature Communications. 4: 1331. Bibcode:2013 НатКо ... 4,1 331 Вт. Дои:10.1038 / ncomms2327. PMID 23299881.
- ^ Lin, Z; Лю, Z; Фу, Вт; Дадни, штат Нью-Джерси; Лян, К. (2013). «Полисульфидофосфаты лития: семейство литий-проводящих соединений с высоким содержанием серы для литий-серных батарей» (PDF). Angewandte Chemie International Edition. 52 (29): 7460–7463. Дои:10.1002 / anie.201300680. PMID 23737078. Архивировано из оригинал (PDF) 10 сентября 2016 г.
- ^ Lin, Z .; Liu, Z .; Fu, W .; Дадни, Н. Дж .; Лян, К. (2013). «Полисульфидофосфаты лития: семейство литий-проводящих соединений с высоким содержанием серы для литий-серных батарей» (PDF). Angewandte Chemie International Edition. 52 (29): 7460–7463. Дои:10.1002 / anie.201300680. PMID 23737078. Архивировано из оригинал (PDF) 10 сентября 2016 г.
- ^ «Цельнотвердый литий-серный аккумулятор хранит в четыре раза больше энергии, чем литий-ионный». NewAtlas.com. 7 июня 2013 г.. Получено 2013-06-13.
- ^ «Новый литий-серный аккумулятор вдвое увеличивает удельную энергию литий-ионного». NewAtlas.com. 2 декабря 2013 г.. Получено 2013-12-04.
- ^ Лаварс, Ник (20 февраля 2014 г.). «Гибридный анод в четыре раза увеличивает срок службы литий-серных батарей». Получено 22 августа, 2016.
- ^ "Запах серы". Экономист. 3 января 2015 г.. Получено 22 августа, 2016.
- ^ «Компания OXIS Energy, производящая литий-ионные аккумуляторы, сообщает о 300 Вт⋅ч / кг и 25 Aч элементов, прогнозируя 33 Aч к середине 2015 года и 500 Втч / кг к концу 2018 года». Конгресс зеленых автомобилей. 12 ноября 2014 г.. Получено 22 августа, 2016.
- ^ Nguyen, D.-T .; Hoefling, A .; Yee, M .; Nguyen, T.H.G .; Theato, P .; Ли, Ю. Дж .; Песня, С.-В. (2019). «Обеспечение высокопроизводительных и безопасных литий-ионно-серных аккумуляторов за счет эффективного сочетания серно-сополимерного катода и твердоуглеродного анода». ChemSusChem. 12 (2): 480–486. Дои:10.1002 / cssc.201802430. PMID 30479038.
- ^ Юань, Чжэ; Пэн, Хун-Цзе; Хуан, Цзя-Ци; Лю Синь-Янь; Ван, Дай-Вэй; Чэн, Синь-Бин; Чжан, Цян (2014-10-01). «Иерархические отдельно стоящие бумажные электроды из углеродных нанотрубок со сверхвысоким содержанием серы для литий-серных батарей» (PDF). Современные функциональные материалы. 24 (39): 6105–6112. Дои:10.1002 / adfm.201401501. ISSN 1616-3028. Архивировано из оригинал (PDF) на 2020-01-03.
- ^ Нилон, Шон (2015-03-03). «Стеклянное покрытие для повышения производительности аккумулятора». НИОКР. Архивировано из оригинал на 2015-03-07. Получено 22 августа, 2016.
- ^ Нилон, Шон (2 марта 2015 г.). «Стеклянное покрытие улучшает характеристики аккумулятора». Phys.org. Получено 22 августа, 2016.
- ^ Копера, Дж. (Сентябрь 2014 г.) "Литий-серные батареи Sion Power обеспечивают питание псевдоспутниковых полетов на большой высоте" Пресс-релиз компании Sion Power
- ^ «Sion Power обеспечивает производительность аккумуляторов нового поколения за счет запатентованной технологии Licerion®». 2016-10-03. Получено 4 октября 2016.
- ^ https://sionpower.com/2018/sion-power-announces-launch-of-its-groundbreaking-licerion-rechargeable-lithium-battery/
- ^ «Anesco и OXIS выпустят хранилища для литиево-серных батарей к 2016 году» (пресс-релиз). OXIS Energy. 14 июля 2015 г.. Получено 22 августа, 2016.
- ^ «Аккумулятор OXIS питает беспилотный автомобиль для программы правительства Великобритании Smart City Gateway» (пресс-релиз). OXIS Energy. 22 февраля 2015 г. Архивировано с оригинал на 2016-04-29. Получено 22 августа, 2016.
- ^ Пропп, К .; Маринеску, М .; Auger, D. J .; и другие. (12 августа 2016 г.). «Мультитемпературная модель эквивалентной схемы разряда в зависимости от состояния для литий-серных батарей». J. Источники энергии. 328: 289–299. Bibcode:2016JPS ... 328..289P. Дои:10.1016 / j.jpowsour.2016.07.090.
- ^ «Серно-литиевые батареи будут впервые коммерциализированы к 2018 году в электрических велосипедах, где плотность энергии будет улучшена для последующего использования в электромобилях». nextbigfuture.com. 2016-06-10. Получено 2017-02-02.
- ^ "Батарея для монтажа в стойку OXIS" (PDF). OXIS Energy. Получено 20 мая, 2017.
- ^ «Презентация технологии литий-серных батарей OXIS Energy». OXIS Energy. 2016-11-03. Получено 20 мая, 2017.
- ^ "ECLIPSE project". ЗАТМЕНИЕ. Архивировано из оригинал 26 августа 2018 г.. Получено 26 мая, 2017.
- ^ «Аккумулятор Sony увеличивает время работы телефона на 40%». Nikkei Asian Обзор. 17 декабря 2015 г.. Получено 22 августа, 2016.
- ^ "'Самая эффективная в мире литий-серная батарея готова к запуску ". Инженер. 6 января 2020 г.. Получено 9 января, 2020.
внешняя ссылка
- "OXIS Energy". OXIS Energy. Получено 2013-10-30.
- «Полиплюс литий-сера». Polyplus.com. Архивировано из оригинал на 2013-04-20. Получено 2013-04-06.
- "Сион Сила". Сион Сила. Получено 2013-04-06.
- "Winston Battery Limited". En.winston-battery.com. Архивировано из оригинал на 2014-03-25. Получено 2013-04-06.
- "Аккумулятор EEMB". Аккумулятор EEMB. Проверено 13 апреля 2018.




![{ displaystyle fc = { frac {k _ { text {s}} q _ { text {up}} [S _ { text {tot}}]} {I_ {c}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/92767aff703c9811fcd59e4023389b4a8bdf304f)