Тяжелая цепь иммуноглобулина - Википедия - Immunoglobulin heavy chain
В тяжелая цепь иммуноглобулина (IgH) представляет собой большую полипептидную субъединицу антитело (иммуноглобулин). В геноме человека локусы гена IgH находятся на хромосоме 14.
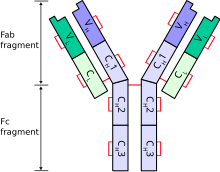
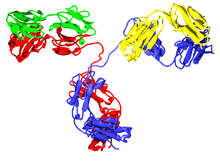
Типичное антитело состоит из двух тяжелых цепей иммуноглобулина (Ig) и двух Легкие цепи Ig. Существует несколько различных типов тяжелой цепи, которые определяют класс или изотип антитела. Эти типы тяжелых цепей различаются у разных животных. Все тяжелые цепи содержат ряд иммуноглобулиновые домены, обычно с одной переменной домен (VЧАС), что важно для привязки антиген и несколько постоянных областей (CЧАС1, ВЧАС2 и др.). Производство жизнеспособной тяжелой цепи является ключевым этапом созревания В-клеток. Если тяжелая цепь способна связываться с суррогатной легкой цепью и перемещаться к плазматической мембране, тогда развивающаяся В-клетка может начать продуцировать свою легкую цепь.[2]
Тяжелая цепь не всегда должна связываться с легкой цепью. Пре-В-лимфоциты могут синтезировать тяжелую цепь в отсутствие легкой цепи, что затем может позволить тяжелой цепи связываться с белком, связывающим тяжелую цепь.[3]
У млекопитающих
Классы
Существует пять типов тяжелой цепи иммуноглобулина млекопитающих: γ, δ, α, μ и ε.[4] Они определяют классы иммуноглобулинов: IgG, IgD, IgA, IgM и IgE, соответственно.
- Тяжелые цепи α и γ содержат примерно 450 аминокислот.
- Тяжелые цепи μ и ε содержат примерно 550 аминокислот.[4]
Регионы
Каждая тяжелая цепь имеет две области:
- а постоянная область (что одинаково для всех иммуноглобулинов одного класса, но различается между классами).
- а переменная область это отличается между разными В-клетки, но одинаков для всех иммуноглобулинов, продуцируемых одной и той же В-клеткой или В-клеткой. клон. Вариабельный домен любой тяжелой цепи состоит из одного иммуноглобулинового домена. Длина этих доменов составляет около 110 аминокислот.[6]
Коровы
Коровы, в частности Bos taurus, показывают вариант общей темы млекопитающих, в которой тяжелая цепь CDR H3 регион адаптирован для получения разнообразного набора антител, которые представляют собой поверхность взаимодействия антигена «ножка и выступ» вместо более привычной двухвалентной поверхности кончика.[7] CDR крупного рогатого скота необычайно длинная и содержит уникальные атрибуты последовательности, которые поддерживают производство парных цистеин остатки во время соматическая гипермутация.[7] Таким образом, если у людей стадия соматической гипермутации нацелена на V (D) J рекомбинация процесс, цель у коров - создание разнообразных дисульфидные связи и создание уникальных наборов петель, которые взаимодействуют с антигеном.[7] Предполагаемой эволюционной движущей силой этой вариации является наличие гораздо более разнообразной микробной среды в пищеварительной системе коровы в результате их существования. жвачные животные.[7]
В рыбе
Челюстная рыба по-видимому, самые примитивные животные, которые способны вырабатывать антитела, подобные тем, которые описаны для млекопитающих.[8] Однако у рыб нет того же набора антител, который есть у млекопитающих.[9] К настоящему времени идентифицированы три различные тяжелые цепи Ig в костлявая рыба.
- Первым идентифицированным был μ (или му) тяжелая цепь, которая присутствует у всех челюстных рыб и является тяжелой цепью того, что считается первичным иммуноглобулином. Полученное антитело IgM секретируется в виде тетрамер в костистость рыба вместо типичной пентамер встречается у млекопитающих и акул.[нужна цитата ]
- Тяжелая цепь (δ) для IgD была первоначально идентифицирована из канальный сом и Атлантический лосось и теперь хорошо документированы для многих костистых рыб.[10]
- Третий ген тяжелой цепи костистого иммуноглобулина Ig был идентифицирован совсем недавно и не похож ни на одну из тяжелых цепей, описанных до сих пор для млекопитающих. Эта тяжелая цепь, идентифицированная как в радужная форель (т)[11] и данио (ζ),[12] потенциально может образовывать отдельные антитела изотип (IgT или IgZ), которые могут предшествовать IgM с точки зрения эволюции.
Подобно ситуации, наблюдаемой для костистых рыб, три различных изотипа тяжелой цепи Ig были идентифицированы в хрящевые рыбы. За исключением μ, эти изотипы тяжелой цепи Ig, по-видимому, являются уникальными для хрящевых рыб. Полученные антитела обозначаются как IgW (также называемые IgX или IgNARC) и IgNAR (рецептор нового антигена иммуноглобулина).[13][14] Последний тип - это антитело тяжелой цепи, антитело, лишенное легких цепей, и может быть использовано для получения однодоменные антитела, которые по сути являются вариабельной областью (VНАР) IgNAR.[15][16][17] Однодоменные антитела акулы (VНАРs) к опухолевым или вирусным антигенам можно выделить от большой наивной акулы-няньки VНАР библиотека с использованием технология фагового дисплея.[16]
IgW теперь также был обнаружен в группе рыб с плавниками, включая латимерию и двоякодышащих рыб. IgW1 и IgW2 у целаканта имеют обычную (VD) структуру n-Jn-C, а также большое количество константных доменов.[18][19]
У амфибий
Лягушки могут синтезировать IgX и IgY. [20]
Смотрите также
Рекомендации
- ^ «Архивная копия». Архивировано из оригинал 19 апреля 2007 г.. Получено 20 апреля, 2007.CS1 maint: заархивированная копия как заголовок (связь)[требуется полная цитата ]
- ^ Mårtensson, I-L; Цередиг, Р. (2017-01-23). «Роль суррогатной легкой цепи и пре-B-клеточного рецептора в развитии B-клеток мыши». Иммунология. 101 (4): 435–441. Дои:10.1046 / j.1365-2567.2000.00151.x. ISSN 0019-2805. ЧВК 2327112. PMID 11122446.
- ^ Haas, Ingrid G .; Вабл, Матиас (1983). «Связывающий белок тяжелой цепи иммуноглобулина». Природа. 306 (5941): 387–9. Bibcode:1983Натура.306..387H. Дои:10.1038 / 306387a0. PMID 6417546.
- ^ а б c Джейнвей Калифорния младший; и другие. (2001). Иммунобиология (5-е изд.). Издательство Гарленд. ISBN 0-8153-3642-X. (полный текст в электронном виде через книжную полку NCBI).[страница нужна ]
- ^ Гав, Дженни М .; Бертон, Деннис Р. (2004). «Взаимодействия человеческого антитела и рецептора Fc, освещенные кристаллическими структурами». Nature Reviews Иммунология. 4 (2): 89–99. Дои:10.1038 / nri1266. PMID 15040582.
- ^ "Биологический проект". Структура антител. Университет Аризоны. Получено 27 мая, 2020.
- ^ а б c d Ван, Фэн; Ekiert, Damian C .; Ахмад, Инша; Ю, Венли; Чжан, Юн; Базирган, Омар; Торкамани, Али; Раудсепп, Терье; Мванги, Вайтхака; Criscitiello, Майкл Ф .; Уилсон, Ян А .; Шульц, Питер Г .; Смидер, Вон В. (2013). «Изменение разнообразия антител». Клетка. 153 (6): 1379–93. Дои:10.1016 / j.cell.2013.04.049. ЧВК 4007204. PMID 23746848.
- ^ Гены тяжелых и легких цепей рыб[требуется полная цитата ] В архиве 23 марта 2007 г. Wayback Machine
- ^ Бенгтен, Ева; Клем, Л. Уильям; Миллер, Норман У .; Уорр, Грегори У .; Уилсон, Мелани (2006). «Иммуноглобулины канального сома: репертуар и выражение». Развитие и сравнительная иммунология. 30 (1–2): 77–92. Дои:10.1016 / j.dci.2005.06.016. PMID 16153707.
- ^ Solem, Stein Tore; Стенвик, Йорген (2006). «Развитие репертуара антител у костистых насекомых - обзор с акцентом на лососевых и Gadus morhua L». Развитие и сравнительная иммунология. 30 (1–2): 57–76. Дои:10.1016 / j.dci.2005.06.007. PMID 16084588.
- ^ Hansen, J.D .; Landis, E.D .; Филлипс, Р. Б. (2005). «Открытие уникального изотипа тяжелой цепи Ig (IgT) у радужной форели: значение для отличительного пути развития В-клеток у костистых рыб». Труды Национальной академии наук. 102 (19): 6919–6924. Bibcode:2005PNAS..102.6919H. Дои:10.1073 / pnas.0500027102. JSTOR 3375456. ЧВК 1100771. PMID 15863615.
- ^ Данилова, Надя; Буссманн, Йерун; Jekosch, Kerstin; Штайнер, Лиза А (2005). «Локус тяжелой цепи иммуноглобулина у рыбок данио: идентификация и экспрессия ранее неизвестного изотипа, иммуноглобулина Z». Иммунология природы. 6 (3): 295–302. Дои:10.1038 / ni1166. PMID 15685175.
- ^ Дули, H .; Флайник, М.Ф. (2006). «Развитие репертуара антител у хрящевых рыб». Развитие и сравнительная иммунология. 30 (1–2): 43–56. Дои:10.1016 / j.dci.2005.06.022. PMID 16146649.
- ^ Симмонс, Дэвид П .; Abregu, Fiona A .; Кришнан, Уша В .; Пролл, Дэвид Ф .; Стрельцов, Виктор А .; Даути, Лариса; Хаттарки, Меган К .; Наттолл, Стюарт Д. (2006). «Стратегии димеризации для фрагментов однодоменных антител IgNAR акулы». Журнал иммунологических методов. 315 (1–2): 171–84. Дои:10.1016 / j.jim.2006.07.019. PMID 16962608.
- ^ Весоловски, Януш; Альзогарай, Ванина; Рейелт, Ян; Унгер, Мэнди; Хуарес, Карла; Уррутия, Мариэла; Кауэрхфф, Ана; Данкуа, Велбек; Риссик, Бьорн; Scheuplein, Феликс; Шварц, Николь; Адриуш, Сахиль; Бойер, Оливье; Семан, Мишель; Лики, Алексей; Серрез, Дэвид V .; Гольдбаум, Фернандо А .; Хааг, Фридрих; Кох-Нольте, Фридрих (2009). «Однодоменные антитела: перспективные экспериментальные и терапевтические инструменты в борьбе с инфекциями и иммунитетом». Медицинская микробиология и иммунология. 198 (3): 157–74. Дои:10.1007 / s00430-009-0116-7. ЧВК 2714450. PMID 19529959.
- ^ а б Фэн, Минцянь; Бянь, Хэцзяо; У, Сяолинь; Фу, Тяньюнь; Фу, Инь; Хонг, Джессика; Флеминг, Брайан Д .; Flajnik, Martin F .; Хо, Митчелл (январь 2019). «Создание и анализ секвенирования следующего поколения большой библиотеки однодоменных антител VNAR, представленной фагом, от шести наивных акул-нянек». Антитела терапия. 2 (1): 1–11. Дои:10.1093 / abt / tby011. ISSN 2516-4236. ЧВК 6312525. PMID 30627698.
- ^ Английский, Hejiao; Хонг, Джессика; Хо, Митчелл (2020). «Древние виды предлагают современную терапию: обновленная информация о последовательностях однодоменных антител к VNAR акулы, фаговых библиотеках и потенциальных клинических применениях». Антитела терапия. 3: 1–9. Дои:10.1093 / abt / tbaa001.
- ^ Чжан, Тяньи; Такчи, Лука; Вэй, Чжиго; Чжао, Яофэн; Салинас, Ирэн (2014). «Внутриклассовая диверсификация генов тяжелой цепи иммуноглобулинов у африканских двоякодышащих рыб». Иммуногенетика. 66 (5): 335–51. Дои:10.1007 / s00251-014-0769-2. ЧВК 4348116. PMID 24676685.
- ^ Ота, Т .; Rast, J.P .; Litman, G.W .; Амемия, К. Т. (2003). «Ограниченное по происхождению сохранение изотипа тяжелой цепи примитивного иммуноглобулина в Dipnoi обнаруживает эволюционный парадокс». Труды Национальной академии наук. 100 (5): 2501–6. Bibcode:2003ПНАС..100.2501О. Дои:10.1073 / pnas.0538029100. ЧВК 151370. PMID 12606718.
- ^ Du, Christina C .; Mashoof, Сара М .; Крисчитьелло, Майкл Ф. (2012). «Оральная иммунизация африканской когтистой лягушки (Xenopus laevis) активирует иммуноглобулин IgX слизистой оболочки». Ветеринарная иммунология и иммунопатология. 145 (1–2): 493–8. Дои:10.1016 / j.vetimm.2011.10.019. ЧВК 3273591. PMID 22100190.
внешняя ссылка
- Иммуноглобулин + Тяжелый + Цепи в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Образовательные ресурсы для анализа тяжелых цепей
