Полианилин - Polyaniline

Полианилин (ПАНИ) это проводящий полимер из полимерный полугибкий стержень семья. Хотя само соединение было открыто более 150 лет назад, только с начала 1980-х полианилин привлек пристальное внимание научного сообщества. Этот интерес связан с повторным открытием высокой электропроводности. Среди семейства проводящих полимеров и органические полупроводники, полианилин обладает многими привлекательными технологическими свойствами. Благодаря своему богатому химическому составу полианилин является одним из наиболее изученных проводящие полимеры за последние 50 лет.[2][3]
Историческое развитие
Полианилин был открыт в начале 1860-х годов Лайтфутом в ходе исследований окисления анилина, который был выделен всего 20 лет назад. Он разработал первый коммерчески успешный путь к красителю под названием Анилин Черный.[4][5] Первое окончательное сообщение о полианилине появилось только в 1862 г. электрохимический метод определения малых количеств анилина.[6]
С начала 20 века периодически публиковались отчеты о структуре ПАНИ.
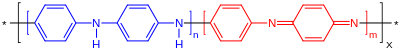
Полимеризован из недорогих анилин, полианилин можно найти в одном из трех идеализированных окисление состояния:[7]
- лейкоэмеральдин - белый / прозрачный и бесцветный (C6ЧАС4NH)п
- эмеральдин - зеленый для изумрудной соли, синий для изумрудной базы ([C6ЧАС4NH]2[C6ЧАС4N]2)п
- (пер) нигранилин - синий / фиолетовый (C6ЧАС4N)п
На рисунке Икс равняется половине степень полимеризации (ДП). Лейкомеральдин с n = 1, m = 0 - полностью восстановленное состояние. Пернигранилин - это полностью окисленное состояние (n = 0, m = 1) с я добываю ссылки вместо амин ссылки. Исследования показали, что большинство форм полианилина являются одним из трех состояний или физических смесей этих компонентов. Эмеральдиновая (n = m = 0,5) форма полианилина, часто называемая эмеральдиновым основанием (EB), является нейтральной, если допированная (протонированная) она называется эмералдиновой солью (ES), а иминные атомы азота протонированы кислотой. Протонирование помогает делокализовать захваченное в противном случае состояние дииминохинон-диаминобензола. Эмеральдиновое основание считается наиболее полезной формой полианилина из-за его высокой стабильности при комнатной температуре и того факта, что при допировании кислотой образующаяся форма соли эмеральдина полианилина обладает высокой электропроводностью.[5] Лейкоэмеральдин и пернигранилин - плохие проводники, даже если они легированы кислотой.
Изменение цвета, связанное с полианилином в различных степенях окисления, можно использовать в сенсорах и электрохромных устройствах.[8] Датчики полианилина обычно используют изменения электропроводности между различными состояниями окисления или уровнями легирования.[9] Обработка эмеральдина кислотами увеличивает электропроводность до десяти порядков. Нелегированный полианилин имеет проводимость 6.28×10−9 См / м, тогда как проводимости 4.60×10−5 См / м может быть достигнуто путем легирования 4% HBr.[10] Этот же материал можно получить окислением лейкоэмеральдина.
Синтез
Хотя синтетические методы получения полианилина довольно просты, механизм полимеризации, вероятно, сложен. Образование лейкоэмеральдина можно описать следующим образом, где [O] - общий окислитель:[11]
- п С6ЧАС5NH2 + [O] → [C6ЧАС4NH]п + H2О
Обычным окислителем является персульфат аммония через 1 M соляная кислота (можно использовать другие кислоты). Полимер осаждается в виде нестабильного разброс с частицами микрометрового размера.
(Пер) нигранилин получают окислением эмеральдинового основания с перкислота:[12]
- {[C6ЧАС4NH]2[C6ЧАС4N]2}п + RCO3H → [C6ЧАС4N]п + H2O + RCO2ЧАС
Обработка
Синтез полианилиновых наноструктур прост.[13]
С помощью поверхностно-активных добавок полианилин можно сделать диспергируемым и, следовательно, полезным для практического применения. Массовый синтез полианилиновые нановолокна, который был тщательно исследован.[14]
Предложена многоступенчатая модель формирования изумрудной базы. На первой стадии реакции формируется степень окисления соли ПС пернигранилина. На втором этапе пернигранилин уменьшенный в соль эмеральдина, поскольку мономер анилина окисляется до катион-радикал.[7] На третьей стадии этот катион-радикал соединяется с солью ES. За этим процессом может следовать рассеяние света анализ, позволяющий определить абсолютную молярная масса. Согласно одному исследованию на первой стадии DP 265 достигается при DP конечного полимера 319. Примерно 19% конечного полимера состоит из анилинового катиона-радикала, который образуется во время реакции.[15]
Полианилин обычно производится в форме агрегатов длинноцепочечных полимеров, дисперсий наночастиц, стабилизированных поверхностно-активными веществами (или допантами), или дисперсий нановолокон, не содержащих стабилизаторов, в зависимости от поставщика и способа синтеза. Дисперсии полианилина, стабилизированные поверхностно-активными веществами или добавками, доступны для коммерческой продажи с конца 1990-х годов.[16]
Возможные приложения
Основные приложения: печатная плата производство: окончательная отделка, используемая на миллионах м² каждый год, антистатический и Покрытия ESD, и защита от коррозии.[4][16] Полианилин и его производные также используются в качестве прекурсора для производства углеродных материалов с примесью азота посредством высокотемпературной термообработки.[17]
Рекомендации
- ^ М. Эвен, С. Куиллард, Б. Корраз, В. Ван, А. Г. МакДиармид (2002). «Тетрамер анилина с концевыми фенильными группами». Acta Crystallogr. E. 58 (3): o343 – o344. Дои:10.1107 / S1600536802002532.CS1 maint: использует параметр авторов (связь)
- ^ Окамото, Ёсикуко; Бреннер, Уолтер (1964). «Глава 7: Органические полупроводники». Полимеры. Райнхольд. С. 125–158.CS1 maint: использует параметр авторов (связь)
- ^ Хигер, Алан (2001). «Нобелевская лекция: Полупроводники и металлические полимеры: четвертое поколение полимерных материалов». Обзоры современной физики. 73 (3): 681–700. Bibcode:2001RvMP ... 73..681H. CiteSeerX 10.1.1.208.7569. Дои:10.1103 / RevModPhys.73.681.
- ^ а б Хорст Бернет (2002). «Азиновые красители». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a03_213.pub2.
- ^ а б МакДиармид, Алан Г. (2001). ""Синтетические металлы ": новая роль органических полимеров (Нобелевская лекция)". Angewandte Chemie International Edition. 40 (14): 2581–2590. Дои:10.1002 / 1521-3773 (20010716) 40:14 <2581 :: AID-ANIE2581> 3.0.CO; 2-2.
- ^ Летеби, Х. (1862 г.). «XXIX.-О получении синего вещества электролизом сульфата анилина». Журнал химического общества. 15: 161–163. Дои:10.1039 / JS8621500161.
- ^ а б Feast, W.J .; Tsibouklis, J .; Pouwer, K.L .; Groenendaal, L .; Meijer, E.W. (1996). «Синтез, обработка и свойства материалов сопряженных полимеров». Полимер. 37 (22): 5017. CiteSeerX 10.1.1.619.5832. Дои:10.1016/0032-3861(96)00439-9.
- ^ Хуанг, Ли-Мин; Чен, Чэн-Хоу; Вэнь, Тен-Чин (2006). «Разработка и характеристика гибких электрохромных устройств на основе полианилина и поли (3,4-этилендиокситиофена) -поли (стиролсульфоновой кислоты)». Electrochimica Acta. 51 (26): 5858. Дои:10.1016 / j.electacta.2006.03.031.
- ^ Вирджи, Шабнам; Хуанг, Цзясин; Канер, Ричард Б .; Вейллер, Брюс Х. (2004). "Газовые сенсоры из полианилина и нановолокна: исследование механизмов реакции". Нано буквы. 4 (3): 491. Bibcode:2004 НаноЛ ... 4..491В. Дои:10.1021 / nl035122e.
- ^ Хаммо, Шамиль М. (2012). «Влияние кислотных присадок на электропроводность полианилина». Тикритский журнал чистой науки. 17 (2).
- ^ Chiang, J.C .; МакДиармид, А. Г. (1986). "'Полианилин: легирование протонной кислотой изумеральдиновой формы в металлический режим ». Синтетические металлы. 1 (13): 193. Дои:10.1016/0379-6779(86)90070-6.
- ^ MacDiarmid, A.G .; Manohar, S.K .; Мастерс, J.G .; Sun, Y .; Weiss, H .; Эпштейн, А.Дж. (1991). «Полианилин: синтез и свойства пернигранилиновой основы». Синтетические металлы. 41 (1–2): 621–626. Дои:10.1016 / 0379-6779 (91) 91145-Z.
- ^ Чирич-Марьянович, Г. Полианилиновые наноструктуры, в наноструктурированных проводящих полимерах (под ред. А. Эфтехари), 2010, John Wiley & Sons, Ltd, Чичестер, Великобритания. Дои:10.1002 / 9780470661338.ch2 PDF
- ^ Хуанг, Цзясин; Вирджи, Шабнам; Weiller, Брюс H .; Канер, Ричард Б. (2003). «Нановолокна полианилина: легкий синтез и химические сенсоры» (PDF). Журнал Американского химического общества. 125 (2): 314–5. CiteSeerX 10.1.1.468.6554. Дои:10.1021 / ja028371y. PMID 12517126. Архивировано из оригинал (PDF) 22 июля 2010 г.
- ^ Kolla, Harsha S .; Surwade, Sumedh P .; Чжан, Синьюй; MacDiarmid, Alan G .; Манохар, Санджив К. (2005). «Абсолютный молекулярный вес полианилина». Журнал Американского химического общества. 127 (48): 16770–1. Дои:10.1021 / ja055327k. PMID 16316207.
- ^ а б Весслинг, Бернхард (2010). «Новое понимание морфологии и структуры органических металлических полианилинов». Полимеры. 2 (4): 786–798. Дои:10.3390 / polym2040786.
- ^ Инь, Си; Chung, Hoon T .; Мартинес, Улисес; Линь, Линг; Артюшкова, Екатерина; Зеленай, Петр (3 мая 2019 г.). "Катализаторы ORR, не содержащие PGM, разработаны путем создания шаблонов полимеров типа PANI, содержащих функциональные группы с высоким сродством к железу". Журнал Электрохимического общества. 166 (7): F3240 – F3245. Дои:10.1149 / 2.0301907jes. OSTI 1512751.
