Признаки рака - The Hallmarks of Cancer

Признаки рака включают шесть биологических возможностей, приобретенных в ходе многоступенчатого развития опухолей человека. Признаки представляют собой организующий принцип для рационализации сложностей неопластического заболевания. Они включают поддержание пролиферативной передачи сигналов, уклонение от супрессоров роста, сопротивление гибели клеток, обеспечение репликативного бессмертия, индукцию ангиогенеза и активацию инвазии и метастазирования. В основе этих отличительных черт лежит нестабильность генома, которая порождает генетическое разнообразие, ускоряющее их приобретение, и воспаление, которое способствует множеству отличительных функций. Концептуальный прогресс последнего десятилетия добавил к этому списку два новых признака потенциальной общности - перепрограммирование энергетического метаболизма и уклонение от иммунного разрушения. Помимо раковых клеток, опухоли демонстрируют еще одно измерение сложности: они содержат набор задействованных, якобы нормальных клеток, которые способствуют приобретению отличительных черт, создавая «микроокружение опухоли». Признание широкой применимости этих концепций будет во все большей степени влиять на разработку новых средств лечения рака человека.[1]
К ноябрю 2010 года на эту статью ссылались более 15000 раз в других исследовательских работах, и с 2004 по 2007 год ее загружали 20 000 раз в год.[2][самостоятельно опубликованный источник? ] По состоянию на март 2011 г. Клетка'самая цитируемая статья.[3]
В обновлении, опубликованном в 2011 году («Признаки рака: следующее поколение»), Вайнберг и Ханахан предложили два новых признака: (1) аномальные метаболические пути и (2) уклонение от иммунной системы, а также две благоприятные характеристики: (1) геном нестабильность и (2) воспаление.[4]
Список клейм
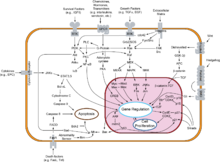
Раковые клетки имеют дефекты в механизмах контроля, которые определяют, как часто они делятся, и в системах обратной связи, которые регулируют эти механизмы контроля (т.е. гомеостаз ).
Нормальные клетки растут и делятся, но есть много средств контроля над этим ростом. Они растут только тогда, когда их стимулируют факторы роста. Если они повреждены, молекулярный тормоз не дает им делиться до тех пор, пока они не будут восстановлены. Если их невозможно восстановить, они совершают запрограммированную гибель клеток (апоптоз). Они могут делиться только ограниченное количество раз. Они являются частью тканевой структуры и остаются на своем месте. Им нужно кровоснабжение, чтобы расти.
Все эти механизмы необходимо преодолеть, чтобы клетка превратилась в рак. Каждый механизм контролируется несколькими белками. Важный белок должен работать со сбоями в каждом из этих механизмов. Эти белки становятся нефункциональными или неисправными, когда последовательность ДНК их генов повреждена в результате приобретенных или соматических заболеваний. мутации (мутации, которые не передаются по наследству, но возникают после зачатия). Это происходит в несколько этапов, которые Ханахан и Вайнберг называют отличительными чертами.
| Возможность | Простая аналогия |
|---|---|
| Самодостаточность в сигналах роста | "педаль акселератора застряла" |
| Нечувствительность к сигналам, препятствующим росту | "тормоза не работают" |
| Уклонение апоптоз | не умрет, когда тело обычно убивает дефектную клетку |
| Безграничный репликативный потенциал | бесконечные поколения потомков |
| Устойчивый ангиогенез | приказывая телу дать ему кровоснабжение |
| Тканевая инвазия и метастаз | мигрирует и распространяется на другие органы и ткани |
Самодостаточность в сигналах роста
- Раковые клетки не нуждаются в стимуляции от внешних сигналов (в виде факторы роста ) умножить.
Как правило, клеткам тела требуются гормоны и другие молекулы, которые действуют как сигналы для них. расти и делиться. Однако раковые клетки могут расти без этих внешних сигналов. Есть несколько способов, которыми раковые клетки могут это делать: производя сами эти сигналы, известные как аутокринная сигнализация; путем постоянной активации сигнальных путей, отвечающих на эти сигналы; или путем уничтожения «выключателей», которые предотвращают чрезмерное усиление этих сигналов (негативный отзыв ). Кроме того, деление нормальных, незлокачественных клеток строго контролируется. В раковых клетках эти процессы не регулируются, потому что белки, которые их контролируют, изменяются, что приводит к усилению роста и делению клеток внутри опухоли.[6][7]
Нечувствительность к сигналам, препятствующим росту
- Раковые клетки обычно устойчивы к сигналам, препятствующим росту, от своих соседей.


Чтобы жестко контролировать деление клеток, в клетках есть процессы, предотвращающие их рост и деление. Эти процессы управляются белками, известными как гены-супрессоры опухолей. Эти гены берут информацию от клетки, чтобы убедиться, что она готова к делению, и остановят деление, если нет (когда ДНК повреждена, Например). При раке эти белки-супрессоры опухолей изменяются так, что они не могут эффективно предотвращать деление клеток, даже если клетка имеет серьезные аномалии. Другой способ предотвращения чрезмерного деления клеток состоит в том, что нормальные клетки также перестают делиться, когда клетки заполняют пространство, в котором они находятся, и касаются других клеток; известный как контактное торможение. Раковые клетки не имеют контактного торможения и поэтому будут продолжать расти и делиться независимо от своего окружения.[6][8]
Как избежать запрограммированной гибели клеток
- Апоптоз это форма запрограммированная гибель клеток (клеточное самоубийство), механизм, с помощью которого клетки программируются на смерть в случае их повреждения. Раковые клетки обычно способны обходить этот механизм.
Клетки обладают способностью «самоуничтожаться»; процесс, известный как апоптоз. Это необходимо для нормального роста и развития организмов, для поддержания тканей тела, а также инициируется при повреждении или инфицировании клетки. Однако раковые клетки теряют эту способность; даже если клетки могут стать сильно ненормальными, они не подвергаются апоптозу. Раковые клетки могут делать это, изменяя механизмы, обнаруживающие повреждение или аномалии. Это означает, что не может происходить правильная передача сигналов, поэтому апоптоз не может активироваться. Они также могут иметь дефекты в самой нисходящей передаче сигналов или в белках, участвующих в апоптозе, каждый из которых также предотвращает собственно апоптоз.[6][9]
Безграничный репликативный потенциал
- Нераковые клетки умирают после определенное количество подразделений. Раковые клетки преодолевают этот предел и, по-видимому, способны к неограниченному росту и делению (бессмертие ). Но эти бессмертные клетки повредили хромосомы, которые могут стать злокачественными.
Клетки тела обычно не могут делиться бесконечно. У них есть ограниченное количество делений, прежде чем клетки станут неспособными делиться (старение ), или умри (кризис). Причина этих барьеров в первую очередь связана с ДНК на концах хромосом, известной как теломеры. Теломерная ДНК укорачивается с каждым делением клетки, пока не становится настолько короткой, что активирует старение, поэтому клетка перестает делиться. Раковые клетки обходят этот барьер, манипулируя ферментами (теломеразой), чтобы увеличить длину теломер. Таким образом, они могут делиться бесконечно, не вызывая старения.[6][10]
Клетки млекопитающих имеют внутреннюю программу, Лимит Хейфлика, что ограничивает их размножение примерно 60–70 удвоениями, после чего они достигают стадии старения.
Этот предел можно преодолеть, отключив их белки-супрессоры опухолей pRB и p53, что позволяет им продолжать удваиваться до тех пор, пока они не достигнут стадии, называемой кризисом, с апоптозом, кариотипическим расстройством и случайными (10−7) появление бессмертной клетки, которая может неограниченно удваиваться. Большинство опухолевых клеток бессмертно.
Счетным устройством для удвоения клеток является теломер, который уменьшается в размере (теряет нуклеотиды на концах хромосом) в течение каждого клеточного цикла. Около 85% случаев рака активируются теломераза чтобы удлинить свои теломеры, а остальные 15% используют метод, называемый Альтернативным удлинением теломер.[11]
Устойчивый ангиогенез
- Ангиогенез это процесс образования новых кровеносных сосудов. Раковые клетки, по-видимому, могут запустить этот процесс, обеспечивая постоянное снабжение таких клеток кислородом и другими питательными веществами.
В нормальных тканях тела проходят кровеносные сосуды, доставляющие кислород из легких. Клетки должны находиться близко к кровеносным сосудам, чтобы получать достаточно кислорода для выживания. Новые кровеносные сосуды образуются во время развития эмбриона, во время заживления ран и во время женского репродуктивного цикла. Расширяющейся опухоли требуются новые кровеносные сосуды для доставки адекватного кислорода к раковым клеткам, и, таким образом, эти нормальные физиологические процессы используются в своих интересах. Для этого раковые клетки приобретают способность управлять образованием новой сосудистой сети, активируя «ангиогенный переключатель». При этом они контролируют незлокачественные клетки, присутствующие в опухоли, которые могут образовывать кровеносные сосуды, за счет снижения выработки факторов, подавляющих образование кровеносных сосудов, и увеличения выработки факторов, способствующих образованию кровеносных сосудов.[6][12]
Тканевая инвазия и метастазирование
- Раковые клетки могут оторваться от своего участка или орган происхождения, чтобы проникать в окружающие ткани и распространяться (метастазировать ) к отдаленным частям тела.
Одно из наиболее известных свойств раковых клеток - их способность проникать в соседние ткани. Это то, что определяет, является ли опухоль доброкачественной или злокачественной, и это свойство, которое делает возможным их распространение по всему телу. Раковые клетки должны претерпеть множество изменений, чтобы они приобрели способность метастазировать в многоступенчатом процессе, который начинается с локального вторжения клеток в окружающие ткани. Затем они должны вторгнуться в кровеносные сосуды, выжить в суровых условиях кровеносной системы, выйти из этой системы и затем начать деление в новой ткани.[6][13]
Обновления
В своем выступлении на конференции NCRI 2010 года Ханахан предложил два новых признака и две новые характеристики. Позже они были систематизированы в обновленной обзорной статье под названием «Признаки рака: следующее поколение».[4]
Новые клейма
Дерегулированный метаболизм
Большинство раковых клеток используют альтернативу метаболические пути для выработки энергии, факт, ценимый с начала двадцатого века с постулатом Гипотеза Варбурга,[14][15] но только сейчас к ним возобновляется исследовательский интерес.[16] Раковые клетки, проявляющие Эффект варбурга активизировать гликолиз и молочнокислое брожение в цитозоль и предотвратить митохондрии от завершения нормального аэробного дыхания (окисление пируват, то цикл лимонной кислоты, а электронная транспортная цепь ). Вместо того, чтобы полностью окислять глюкозу, чтобы производить столько же АТФ насколько возможно, раковые клетки скорее превратят пируват в строительные блоки для большего количества клеток. Фактически, низкое соотношение АТФ: АДФ, вызванное этим эффектом, вероятно, способствует дезактивации митохондрий. Потенциал митохондриальной мембраны гиперполяризован для предотвращения чувствительные к напряжению переходные поры проницаемости (PTP) от срабатывания апоптоз.[17][18]
В кетогенная диета исследуется в качестве адъювантной терапии некоторых видов рака,[19][20][21] включая глиому,[22][23] из-за неэффективности рака в метаболизме кетоновые тела.
Уклонение от иммунной системы
Несмотря на то, что раковые клетки вызывают усиление воспаления и ангиогенеза, они также, по-видимому, способны избегать взаимодействия с иммунной системой организма за счет потери интерлейкина-33. иммунная система. (Видеть иммунология рака )
Разрешающие характеристики
В обновленном документе также определены две новые характеристики. Они помечены как таковые, поскольку их приобретение приводит к развитию гипотетических «отличительных черт».
Нестабильность генома
Раковые клетки обычно имеют тяжелые хромосомные аномалии которые усугубляются по мере прогрессирования болезни. Клетки HeLa, например, чрезвычайно плодовиты и имеют тетраплоидия 12, трисомия 6, 8 и 17, а также модальный номер хромосомы 82 (а не нормальное диплоидное число 46).[24] Скорее всего, начинаются небольшие генетические мутации. туморогенез, но как только клетки начинают цикл разрушения-плавления (BFB), они могут мутировать гораздо быстрее. (Видеть нестабильность генома )
Воспаление
Недавние открытия подчеркнули роль местных хронических заболеваний. воспаление в индукции многих видов рака. Воспаление приводит к ангиогенезу и еще большей иммунной реакции. Деградация внеклеточный матрикс необходим для образования новых кровеносных сосудов, увеличивает вероятность метастазирования. (Видеть воспаление при раке )
Критика
Статья в Обзоры природы Рак в 2010 году указали, что пять «отличительных черт» также были характерны для доброкачественные опухоли.[25] Единственным признаком злокачественного заболевания была его способность проникать и метастазировать.[25]
Статья в Журнал биологических наук в 2013 году утверждал, что исходные данные по большинству этих признаков отсутствуют.[26] Он утверждал, что рак - это заболевание на тканевом уровне, и эти признаки на клеточном уровне вводят в заблуждение.
Примечания и ссылки
- ^ https://www.cell.com/fulltext/S0092-8674(11)00127-9#:~:text=The%20hallmarks%20constitute%20an%20organizing,and%20activating%20invasion%20and%20metastasis. Отсутствует или пусто
| название =(помощь) - ^ Признаки рака, Блог UK Science Update по исследованию рака, ноябрь 2010 г.
- ^ "Ученые пересматривают признаки рака"'". Science Daily. 16 марта 2011 г.. Получено 4 апреля 2011.
- ^ а б Hanahan, D .; Вайнберг, Р. А. (2011). «Признаки рака: следующее поколение». Клетка. 144 (5): 646–674. Дои:10.1016 / j.cell.2011.02.013. PMID 21376230.
- ^ Ячейка 100: 59
- ^ а б c d е ж Hanahan, D; Вайнберг, РА (4 марта 2011 г.). «Признаки рака: следующее поколение». Клетка. 144 (5): 646–74. Дои:10.1016 / j.cell.2011.02.013. PMID 21376230.
- ^ Эван, Джи; Vousden, KH (17 мая 2001 г.). «Пролиферация, клеточный цикл и апоптоз при раке». Природа. 411 (6835): 342–8. Bibcode:2001Натура.411..342E. Дои:10.1038/35077213. PMID 11357141.
- ^ Макклатчи, AI; Яп, А.С. (октябрь 2012 г.). «Контактное ингибирование (распространения) редукции». Текущее мнение в области клеточной биологии. 24 (5): 685–94. Дои:10.1016 / j.ceb.2012.06.009. PMID 22835462.
- ^ Элмор, С. (июнь 2007 г.). «Апоптоз: обзор запрограммированной гибели клеток». Токсикологическая патология. 35 (4): 495–516. Дои:10.1080/01926230701320337. ЧВК 2117903. PMID 17562483.
- ^ Гринберг, РА (март 2005 г.). «Теломеры, кризис и рак». Современная молекулярная медицина. 5 (2): 213–8. Дои:10.2174/1566524053586590. PMID 15974875.
- ^ Чезаре, Энтони Дж .; Реддел, Роджер Р. (2010). «Альтернативное удлинение теломер: модели, механизмы и последствия». Природа Обзоры Генетика. 11 (5): 319–330. Дои:10.1038 / nrg2763. PMID 20351727.
- ^ Бергерс, G; Бенджамин, Л. Е. (июнь 2003 г.). «Онкогенез и ангиогенный переключатель». Обзоры природы. Рак. 3 (6): 401–10. Дои:10.1038 / nrc1093. PMID 12778130.
- ^ van Zijl, F; Крупица, Г; Микулиц, W (2011). «Начальные этапы метастазирования: инвазия клеток и эндотелиальная трансмиграция». Мутационные исследования. 728 (1–2): 23–34. Дои:10.1016 / j.mrrev.2011.05.002. ЧВК 4028085. PMID 21605699.
- ^ Альфарук, нокаут; Verduzco, D; Rauch, C; Муддатир, AK; Адиль, HH; Эльхассан, GO; Ибрагим, Мэн; Дэвид Поло Ороско, Дж; Кардоне, РА; Решкин, SJ; Харгинди, S (2014). «Гликолиз, метаболизм опухоли, рост и распространение рака. Новая этиопатогенная перспектива на основе pH и терапевтический подход к старому вопросу рака». Онкология. 1 (12): 777–802. Дои:10.18632 / oncoscience.109. ЧВК 4303887. PMID 25621294.
- ^ О. Варбург, К. Позенер, Э. Негелейн: "Ueber den Stoffwechsel der Tumoren" Biochemische Zeitschrift, 152, стр. 319–344, 1924. (нем.). Перепечатано на английском языке в книге О метаболизме опухолей О. Варбург, Издательство: Констебль, Лондон, 1930.
- ^ «Ориентация на метаболизм опухоли». Обзоры природы Drug Discovery. 9 (7): 503–504. 2010. Дои:10.1038 / nrd3215. ISSN 1474-1776. PMID 20592733.
- ^ Форрест MD. «Почему раковые клетки обладают более гиперполяризованным потенциалом митохондриальной мембраны и открываются новые перспективы терапии». bioRxiv 10.1101/025197.
- ^ Готлиб Э., Армор С.М., Харрис М.Х., Томпсон С.Б. (2003). «Потенциал митохондриальной мембраны регулирует конфигурацию матрикса и высвобождение цитохрома с во время апоптоза». Разница в гибели клеток. 10 (6): 709–717. Дои:10.1038 / sj.cdd.4401231. PMID 12761579.
- ^ Шварц, L; Супуран, CT; Альфарук, КО (2017). «Эффект Варбурга и признаки рака». Противораковые средства в медицинской химии. 17 (2): 164–170. Дои:10.2174/1871520616666161031143301. PMID 27804847.
- ^ Бараньяно К.В., Хартман А.Л. (2008). «Кетогенная диета: применение при эпилепсии и других неврологических заболеваниях». Варианты лечения Curr Neurol. 10 (6): 410–9. Дои:10.1007 / s11940-008-0043-8. ЧВК 2898565. PMID 18990309.
- ^ Аллен Б.Г., Бхатия С.К., Андерсон С.М. и др. (Октябрь 2011 г.). «Кетогенные диеты как адъювантная терапия рака: история и потенциальный механизм». Редокс Биол. 2C (3): 327–337. Дои:10.1016 / j.eplepsyres.2011.09.022. PMID 22019313.
- ^ Шварц, L; Сейфрид, Т; Альфарук, нокаут; Да Вейга Морейра, Дж .; Фейс, С. (апрель 2017 г.). «Эффект вне Варбурга: эффективное лечение рака, направленное на специфический метаболизм опухоли и нарушение регуляции pH». Семинары по биологии рака. 43: 134–138. Дои:10.1016 / j.semcancer.2017.01.005. PMID 28122260.
- ^ Шек А.С., Абдельвахаб М.Г., Фентон К.Э., Стаффорд П. (октябрь 2011 г.). «Кетогенная диета для лечения глиомы: выводы из генетического профилирования». Эпилепсия Res. 100 (3): 327–37. Дои:10.1016 / j.eplepsyres.2011.09.022. PMID 22019313.
- ^ «Лизат ядерного экстракта HeLa (ab14655)». abcam.
- ^ а б Лазебник Ю. (апрель 2010). «Какие признаки рака?». Nat. Преподобный Рак. 10 (4): 232–3. Дои:10.1038 / nrc2827. PMID 20355252.
- ^ Sonnenschein C, Soto AM (сентябрь 2013 г.). «Старение обзоров по признакам рака 2000 и 2011 годов: критика» (PDF). Дж. Биоски. 38 (3): 651–63. Дои:10.1007 / s12038-013-9335-6. ЧВК 3882065. PMID 23938395.
Библиография
- Ханахан Д., Вайнберг Р.А. (январь 2000 г.). «Признаки рака». Клетка. 100 (1): 57–70. Дои:10.1016 / S0092-8674 (00) 81683-9. PMID 10647931..
- Ханахан Д., Вайнберг Р.А. (март 2011 г.). «Признаки рака: следующее поколение». Клетка. 144 (5): 646–74. Дои:10.1016 / j.cell.2011.02.013. PMID 21376230..
