Тетрафторборат триэтилоксония - Triethyloxonium tetrafluoroborate
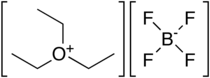 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Тетрафторборат триэтилоксония | |
| Идентификаторы | |
3D модель (JSmol ) | |
| 3598090 | |
| ChemSpider | |
| ECHA InfoCard | 100.006.096 |
PubChem CID | |
| UNII | |
| Номер ООН | 3261 |
| |
| |
| Характеристики | |
| C6ЧАС15BF4О | |
| Молярная масса | 189.99 г · моль−1 |
| Температура плавления | От 91 до 92 ° C (от 196 до 198 ° F, от 364 до 365 K) |
| Реагирует | |
| Опасности | |
Классификация ЕС (DSD) (устарело) | |
| R-фразы (устарело) | R14, R34 |
| S-фразы (устарело) | S22, S26, S36 / 37/39 |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
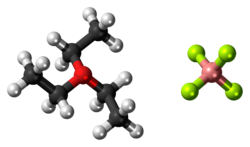
Тетрафторборат триэтилоксония это органический оксоний соединение с формулой [(CH3CH2)3O] BF4. Его часто называют Реактив Меервейна или же Соль Меервейна после его первооткрывателя Ганс Меервейн.[1][2] Также хорошо известны и коммерчески доступны родственные тетрафторборат триметилоксония. Эти соединения представляют собой белые твердые вещества, растворяющиеся в полярных органических растворителях. Они сильные алкилирующие агенты. Помимо BF−
4 соль, доступно множество родственных производных.[3]
Синтез и реакционная способность
Тетрафторборат триэтилоксония получают из трифторид бора, диэтиловый эфир и эпихлоргидрин:[4]
- 4 Et2O · BF3 + 2 Et2O + 3 C2ЧАС3(O) CH2Cl → 3 Et3О+BF−
4 + B [(OCH (CH2Cl) CH2OEt]3
Соль триметилоксония доступна от диметиловый эфир по аналогичному маршруту.[5] Эти соли не имеют длительного срока хранения при комнатной температуре. Они разлагаются при гидролизе:
- [(CH3CH2)3O]+BF−
4 + H2O → (CH3CH2)2O + CH3CH2ОН + HBF4
Склонность солей триалкилоксония к алкильному обмену может быть благоприятной. Например, тетрафторборат триметилоксония, который медленно реагирует из-за его низкой растворимости в большинстве совместимых растворителей, может быть преобразован in situ в более высокий алкил / более растворимый оксоний, тем самым ускоряя реакции алкилирования.[6]
Структура
Соединение имеет пирамидальный катион оксония, изоэлектронный с триэтиламин, и тетраэдрический фторборат-анион. Отражая свой ионный характер, соль растворяется в полярных, но инертных растворителях, таких как дихлорметан, диоксид серы, и нитрометан.
Безопасность
Тетрафторборат триэтилоксония является сильным алкилирующим агентом, хотя опасность уменьшена, поскольку он нелетуч. При контакте с водой выделяет сильную кислоту. Свойства метильного производного аналогичны.
Рекомендации
- ^ Х. Меервейн; Г. Хинц; П. Хофманн; Э. Кронинг и Э. Пфейл (1937). "Über Tertiäre Oxoniumsalze, I". Journal für Praktische Chemie. 147 (10–12): 257. Дои:10.1002 / prac.19371471001.
- ^ Х. Меервейн; Э. Беттенберг; H. Gold; Э. Пфейл и Г. Уиллфанг (1940). "Über Tertiäre Oxoniumsalze, II". Journal für Praktische Chemie. 154 (3–5): 83. Дои:10.1002 / prac.19391540305.
- ^ Хартвиг Перст, Дэйв Г. Сипи «Триэтилоксониум тетрафторборат» в энциклопедии реагентов для органического синтеза John Wiley & Sons, Нью-Йорк, 2008. Дои:10.1002 / 047084289X.rt223.pub2. Дата публикации статьи в Интернете: 14 марта 2008 г.
- ^ Х. Меервейн (1973). «Триэтилоксония фторборат». Органический синтез.; Коллективный объем, 5, п. 1080
- ^ Т. Дж. Керфи (1988). «Тетрафторборат триметилоксония». Органический синтез.; Коллективный объем, 6, п. 1019
- ^ Вартак А.П., Крукс П.А. (2009). «Масштабируемый энантиоселективный синтез альфа2-адренергического агониста, лофексидина». Орг. Процесс Res. Dev. 13 (3): 415–419. Дои:10.1021 / op8002689.
