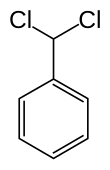
Бензал хлорид - Benzal chloride
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC (Дихлорметил) бензол | |||
Другие имена
| |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| 1099407 | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.002.463 | ||
| Номер ЕС |
| ||
| КЕГГ | |||
| MeSH | Соединения Бензилиденовые соединения | ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1886 2810 | ||
| |||
| |||
| Характеристики | |||
| C7ЧАС6Cl2 | |||
| Молярная масса | 161,03 г / моль | ||
| Внешность | Бесцветная жидкость | ||
| Плотность | 1,254 г / см3, жидкость | ||
| Температура плавления | От −17 до −15 ° C (от 1 до 5 ° F; от 256 до 258 K) | ||
| Точка кипения | 205 ° С (401 ° F, 478 К) (82 ° С при 10 мм рт. Ст.) | ||
| 0,25 г / л при 39 ° C | |||
| Давление газа | 0,6 кПа (45 ° C) | ||
| Опасности | |||
| Пиктограммы GHS |     | ||
| Сигнальное слово GHS | Опасность | ||
| H302, H315, H318, H331, H335, H351 | |||
| P201, P202, P261, P264, P270, P271, P280, P281, P301 + 312, P302 + 352, P304 + 340, P305 + 351 + 338, P308 + 313, P310, P311, P312, P321, P330, P332 + 313, P362, P403 + 233, P405, P501 | |||
| точка возгорания | 93 ° С (199 ° F, 366 К) | ||
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Бензал хлорид является органическое соединение с формула C6ЧАС5CHCl2.[1] Эта бесцветная жидкость представляет собой слезоточивый и используется как строительный блок в органический синтез.
Приготовление и использование
Бензал хлорид производится свободный радикал хлорирование из толуол, которому в процессе предшествует бензилхлорид (C6ЧАС5CH2Cl), а затем бензотрихлорид (C6ЧАС5CCl3):
- C6ЧАС5CH3 + Cl2 → С6ЧАС5CH2Cl + HCl
- C6ЧАС5CH2Cl + Cl2 → С6ЧАС5CHCl2 + HCl
- C6ЧАС5CHCl2 + Cl2 → С6ЧАС5CCl3 + HCl
Бензильные галогениды обычно сильны алкилирующие агенты, и по этой причине хлористый бензал считается опасным соединением.
Обработка бензала хлорида натрий дает стильбен.
Бензал хлорид в основном используется в промышленности в качестве предшественника бензальдегид. Это преобразование включает гидролиз при наличии базы:[2]
- C6ЧАС5CHCl2 + H2О → С6ЧАС5CHO + 2 HCl
Рекомендации
- ^ «БЕНЗАЛЬ ХЛОРИД». Международная программа химической безопасности. Получено 2007-10-30.
- ^ Липпер, Карл-Август; Лезер, Экхард. «Бензилхлорид и другие хлорированные ароматические углеводороды с боковыми цепями». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.o04_o01.