Циклобутанон - Википедия - Cyclobutanone
 | |
| Идентификаторы | |
|---|---|
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.013.405 |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C4ЧАС6О | |
| Молярная масса | 70.091 г · моль−1 |
| Внешность | Бесцветная жидкость |
| Плотность | 0,9547 г / см3 (0 ° С)[1] |
| Температура плавления | -50,9 ° С (-59,6 ° F, 222,2 К)[1] |
| Точка кипения | 99,75 ° С (211,55 ° F, 372,90 К)[1] |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Циклобутанон является органическое соединение с молекулярная формула (CH2)3CO. Это четырехчленный циклический кетон (циклоалканон). Это бесцветная летучая жидкость при комнатной температуре. С циклопропанон очень чувствителен, циклобутанон - самый маленький, легко обрабатываемый циклический кетон.
Подготовка
Русский химик Николай Кишнер Впервые получил циклобутанон в 1905 году.[2][3] Он синтезировал циклобутанон с низким выходом из циклобутанкарбоновая кислота в несколько этапов реакции. По сегодняшним меркам этот процесс обременительн и неэффективен.
 Синтез циклобутанона из циклобутанкарбоновой кислоты.
Синтез циклобутанона из циклобутанкарбоновой кислоты.
С тех пор были разработаны более эффективные и высокоэффективные синтезы.[4] Одна из стратегий включает деградацию пятиуглеродных строительных блоков. Например, окислительный декарбоксилирование циклобутанкарбоновой кислоты был улучшен за счет использования других реагентов и методов. П. Липп и Р. Кёстер обнаружили более новый, более эффективный препарат циклобутанона, в котором раствор диазометан в диэтиловый эфир реагирует с кетен.[5] Эта реакция основана на кольцевом расширении циклопропанон первоначально образуется промежуточное соединение, в котором отщепляется молекулярный азот. В механизм реакции было подтверждено реакцией с использованием 14C-меченый диазометан.[6]
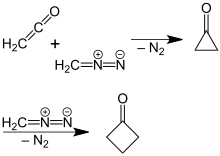 Получение циклобутанона из диазометана и кетена через циклопропанон
Получение циклобутанона из диазометана и кетена через циклопропанон
Другой синтез циклобутанона включает катализируемую литием перегруппировку оксаспиропентана, который образуется эпоксидирование легкодоступных метиленциклопропан.[7][8]
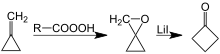 Получение циклобутанона перегруппировкой
Получение циклобутанона перегруппировкой
Циклобутанон также может быть получен двухстадийной процедурой диалкилированием 1,3-дитиан с 1-бром-3-хлорпропаном с последующим снятием защиты с кетона с помощью хлорид ртути (HgCl2) и карбонат кадмия (CdCO3).[9]
Реакции
При температуре около 350 ° C циклобутанон разлагается на этилен и кетен.[10] В энергия активации для этой [2 + 2] циклореверсии - 52 ккал / моль. Реакция реверсии, [2 + 2] циклоприсоединение кетена и этилена никогда не наблюдались.
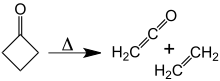 Разложение циклобутанона
Разложение циклобутанона
Смотрите также
Другие циклические кетоны:
Рекомендации
- ^ а б c CRC Справочник по химии и физике. 90. Бока-Ратон, Флорида: CRC Press.
- ^ Н. Кишнер (1905). "'Über die Einwirkung von Brom auf die Amide α-bromsubstituierter Säuren ". Journal der Russischen Physikalisch-Chemischen Gesellschaft. 37: 103–105.
- ^ Н. Кишнер (1905). "Über das Cyklobutanon". Journal der Russischen Physikalisch-Chemischen Gesellschaft. 37: 106–109.
- ^ Дитер Зеебах (1971). "Isocyclische Vierringverbindungen". В Хубене; Вейль; Мюллер (ред.). Methoden der Organischen Chemie. IV / 4. Штутгарт: Георг Тиме Верлаг.
- ^ П. Липп и Р. Кёстер (1931). "Ein neuer Weg zum Cyclobutanon". Berichte der Deutschen Chemischen Gesellschaft. 64 (11): 2823–2825. Дои:10.1002 / cber.19310641112.
- ^ Semenow, Dorothy A .; Кокс, Юджин Ф .; Робертс, Джон Д. (1956). «Соединения с малым кольцом. XIV. Радиоактивный циклобутанон из кетена и диазометана-14C1». Журнал Американского химического общества. 78 (13): 3221–3223. Дои:10.1021 / ja01594a069.
- ^ Salaün, J. R .; Кониа, Дж. М. (1971). «Оксаспиропентан. Быстрый путь к циклобутанону». Журнал химического общества D: Химические коммуникации (23): 1579b-1580. Дои:10.1039 / C2971001579B.
- ^ Дж. Р. Салаун, Дж. Чемпион, Дж. М. Кониа (1977). «Циклобутанон из метиленциклопропана через оксаспиропентан». Органический синтез. 57: 36. Дои:10.15227 / orgsyn.057.0036.CS1 maint: несколько имен: список авторов (связь); Коллективный объем, 6, п. 320
- ^ Д. Сибах, А. К. Бек (1971). «Циклические кетоны из 1,3-дитиана: циклобутанон». Органический синтез. 51: 76. Дои:10.15227 / orgsyn.051.0076.; Коллективный объем, 6, п. 316
- ^ Das, M. N .; Kern, F .; Coyle, T.D .; Уолтерс, В. Д. (1954). «Термическое разложение циклобутанона1». Журнал Американского химического общества. 76 (24): 6271–6274. Дои:10.1021 / ja01653a013.




