Дегидроаланин - Dehydroalanine
 | |
 | |
| Имена | |
|---|---|
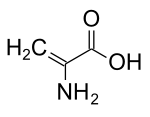
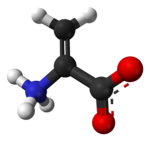
| Название ИЮПАК 2-аминопроп-2-еновая кислота | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| DrugBank | |
| КЕГГ | |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C3ЧАС5Нет2 | |
| Молярная масса | 87,08 г / моль |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Дегидроаланин (Cα, β-дидегидроаланин, α, β-дигидроаланин, 2-аминоакрилат, или же 2,3-дидегидроаланин) это дегидроаминовая кислота. Его не существует в свободной форме, но он встречается в природе в виде остатка, обнаруженного в пептиды из микробный происхождение.[1] В качестве аминокислотного остатка он необычен, поскольку имеет ненасыщенный позвоночник.[2]
Структура и реакционная способность
Как большинство первичных енамины, дегидроаланин нестабилен. Дегидроаланин гидролизуется до пируват.
N-Ацилированные производные дегидроаланина, такие как пептиды и родственные соединения, стабильны. Например, метил 2-ацетамидоакрилат представляет собой N-ацетилированное производное сложного эфира. В виде остатка в пептиде он образуется пост-переводная модификация. Требуемые прекурсоры: серин или цистеин остатки, которые подвергаются опосредованной ферментами потере воды и сероводород, соответственно.
Большинство аминокислотных остатков не реагируют по отношению к нуклеофилы, но те, которые содержат дегидроаланин или некоторые другие дегидроаминокислоты, являются исключением. Эти электрофильный из-за α, β-ненасыщенный карбонил,[2] и может, например, алкилировать другие аминокислоты. Эта деятельность сделала ДГК синтетически полезной для приготовления лантионин.
Вхождение
Остаток дегидроаланина впервые был обнаружен в низин, а циклический пептид с антимикробной активностью.[2] Дегидроаланин также присутствует в некоторых лантибиотики и микроцистины.
DHA может быть образована из цистеина или серина путем простого основного катализа без необходимости использования фермента, что может произойти во время приготовления пищи и щелочной процессы приготовления пищи. Затем он может алкилировать другие аминокислотные остатки, такие как лизин, образуя лизиноаланин перекрестные ссылки и рацемизация исходного аланина. Получающиеся в результате белки имеют более низкую питательную ценность для некоторых видов, но более высокую питательную ценность для других. Некоторые лизиноаланины также могут вызывать увеличение почек у крыс.[3]
Многие пептиды, содержащие дегидроаланин, токсичны.[2]

Долгое время считалось, что остаток дегидроаланина является важным электрофильным каталитическим остатком в гистидин-аммиак-лиаза и фенилаланин аммиак-лиаза ферменты, но позже было обнаружено, что активный остаток представляет собой другое ненасыщенное производное аланина - 3,5-дигидро-5-метилдиен-4ЧАС-имидазол-4-он - что еще более электрофильно.[4][5]
Рекомендации
- ^ Даунс, DM; Эрнст, округ Колумбия (апрель 2015 г.). «От микробиологии до биологии рака: семейство белков Rid предотвращает повреждение клеток, вызванное эндогенно генерируемыми химически активными формами азота». Молекулярная микробиология. 96 (2): 211–9. Дои:10,1111 / ммi,12945. ЧВК 4974816. PMID 25620221.
- ^ а б c d Сиодлак, Давид (2015). «α, β-Дегидроаминокислоты в природных пептидах». Аминокислоты. 47 (1): 1–17. Дои:10.1007 / s00726-014-1846-4. ЧВК 4282715. PMID 25323736.
- ^ Фридман, Мендель (1999). «Лизиноаланин в пище и в антимикробных белках». В Джексоне, Лорен С .; Knize, Mark G .; Морган, Джеффри Н. (ред.). Влияние обработки на безопасность пищевых продуктов. Успехи экспериментальной медицины и биологии. 459. Springer. С. 145–159. Дои:10.1007/978-1-4615-4853-9_10. ISBN 978-1-4615-4853-9. PMID 10335374.
- ^ Рети, Янош (2003). «Открытие и роль метилиденимидазолона, высоко электрофильной простетической группы». Biochimica et Biophysica Acta (BBA) - Белки и протеомика. 1647 (1–2): 179–184. Дои:10.1016 / S1570-9639 (03) 00091-8. PMID 12686130.
- ^ Calabrese JC, Jordan DB, Boodhoo A, Sariaslani S, Vannelli T (сентябрь 2004 г.). «Кристаллическая структура фенилаланина аммиаклиазы: множественные спиральные диполи, участвующие в катализе». Биохимия. 43 (36): 11403–16. Дои:10.1021 / bi049053 +. PMID 15350127.
