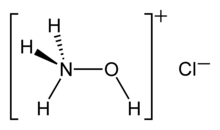
Гидроксиламмоний хлорид - Hydroxylammonium chloride
 | |
 | |
 | |
| Имена | |
|---|---|
| Другие имена Гидроксиламин гидрохлорид | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.024.362 |
| Номер ЕС |
|
| КЕГГ | |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| |
| |
| Свойства | |
| [NH3OH] Cl | |
| Молярная масса | 69,49 г / моль |
| Внешность | белое кристаллическое твердое вещество |
| Плотность | 1,67 г / см3 |
| Температура плавления | От 155 до 157 ° C (от 311 до 315 ° F; от 428 до 430 K) разлагается |
| Опасности | |
| Паспорт безопасности | [1] |
| Пиктограммы GHS |      |
| Сигнальное слово GHS | Опасность |
| H290, H301, H302, H312, H315, H317, H319, H351, H373, H400 | |
| P201, P202, P234, P260, P261, P264, P270, P272, P273, P280, P281, P301 + 310, P301 + 312, P302 + 352, P305 + 351 + 338, P308 + 313, P312, P314, P321, P322, P330, P332 + 313, P333 + 313, P337 + 313, P362 | |
| NFPA 704 (огненный алмаз) | |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Гидроксиламмоний хлорид это соль соляной кислоты из гидроксиламин. Гидроксиламин является биологическим промежуточным продуктом в нитрификация (биологическое окисление аммиака кислородом до нитрита) и в анаммокс (биологическое окисление нитрита и аммония до газообразного азота), которые важны для азотный цикл в почве и в станции очистки сточных вод.
Приложения
Хлорид гидроксиламмония используется в органический синтез для подготовки оксимы и гидроксамовые кислоты от карбоновые кислоты, N- и O-замещенные гидроксиамины и реакции присоединения двойной углерод-углеродной связи.
В процессе извлечения бромистым ацетилом лигнин от лигноцеллюлозная биомасса, хлорид гидроксиламмония можно использовать для удаления бром и полибромид из раствора.
При обработке поверхностей он используется для подготовки средства против кожных покровов, ингибиторы коррозии, и чистящие добавки. Это также исходный материал для производства фармацевтических препаратов и агрохимикатов. В резиновой и пластмассовой промышленности это антиоксидант, вулканизация ускоритель и радикальный мусорщик.
Он также используется в качестве фиксатора для текстильных красителей, вспомогательного средства в некоторых процессах окрашивания, в качестве вспомогательного средства для извлечения металлов и флотации, в качестве антиоксиданта в жирные кислоты и мыла, а также в качестве стабилизатора цвета и эмульсионной добавки в цветных пленках.
Он также используется в аналитической химии при анализе железа в воде в сочетании с α, α-дипиридил. Хлорид гидроксиламмония превращает все железо в Fe2+, который затем образует координационный комплекс с дипиридилом.
использованная литература
- Фукусима, РС; Dehority, B.A .; Loerch, S.C. (1 января 1991 г.). «Модификация колориметрического анализа лигнина и его использование при изучении ингибирующего действия лигнина на переваривание кормов микроорганизмами рубца». J. Anim. Sci. 69 (1): 295–304. Дои:10,2527 / 1991,691295x. PMID 2005024. Архивировано из оригинал 10 октября 2008 г.
- Elstner, E.F .; Хеупель, А. (февраль 1976 г.). «Ингибирование образования нитрита из гидроксиламмонийхлорида: простой анализ супероксиддисмутазы». Анальный. Биохим. 70 (2): 616–20. Дои:10.1016/0003-2697(76)90488-7. PMID 817618.

