Калиевый канал KcsA - KcsA potassium channel
KcsA (K cканал sтрептомицеты А) является прокариотическим калиевый канал из почвенных бактерий Streptomyces lividans который был широко изучен в ионный канал исследование. В pH[1] активированный белок обладает двумя трансмембранные сегменты и высокоселективная область пор, отвечающая за стробирование и перемещение K+ ионы из клетки.[2] Аминокислотная последовательность, обнаруженная в фильтре селективности KcsA, высококонсервативна как среди прокариотических, так и среди эукариотических K+ каналы напряжения;[1][3] в результате исследования KcsA предоставили важную структурную и механистическую информацию о молекулярной основе K+ ионный отбор и проводимость. Как один из наиболее изученных ионных каналов по сей день, KcsA является шаблоном для исследований K+ функция канала и его выясненная структура лежат в основе компьютерного моделирования динамики канала как для прокариот, так и для эукариотических видов.[4]
| KcsA Калиевый канал | |||||||||
|---|---|---|---|---|---|---|---|---|---|
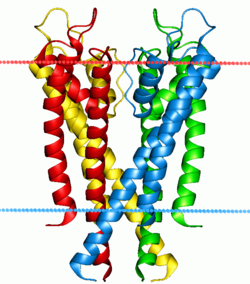 Четыре субъединицы, образующие канал, нарисованы разными цветами. Они окружают центральную пору, защищенную фильтром селективности, состоящим из P-петель каждой из субъединиц. Синие и красные точки обозначают границы липидный бислой. | |||||||||
| Идентификаторы | |||||||||
| Символ | KcsA | ||||||||
| Pfam | PF07885 | ||||||||
| ИнтерПро | IPR013099 | ||||||||
| SCOP2 | 1bl8 / Объем / СУПФАМ | ||||||||
| OPM суперсемейство | 8 | ||||||||
| Белок OPM | 1r3j | ||||||||
| |||||||||
История
KcsA был первым ионным каналом калия, который был охарактеризован с использованием рентгеновская кристаллография от Родерик Маккиннон и его коллегами в 1998 году. В годы, предшествовавшие этому, исследования структуры K+ Каналы были сосредоточены на использовании связывания малых токсинов для выявления местоположения пор и фильтра селективности среди остатков каналов. Группа Маккиннона выдвинула теорию тетрамерный расположение трансмембранный сегментов, и даже предположил наличие порообразующих «петель» в области фильтра, состоящих из коротких сегментов аминокислот, которые взаимодействуют с K+ ионы проходящий через канал[5] Открытие сильной последовательности гомология между KcsA и другими каналами семейства Kv, включая Шейкер белок, привлек внимание научного сообщества, особенно потому, что K+ последовательность подписи канала стала появляться в других прокариотический гены. Простота двух трансмембранных спиралей в KcsA, в отличие от шести во многих эукариотический ионных каналов, также предоставили метод для понимания механизмов K+ каналы проводимости на более рудиментарном уровне, тем самым обеспечивая даже большой импульс для изучения KcsA.
Кристаллическая структура KcsA была решена группой Маккиннона в 1998 году после открытия, что удаление C-конец цитоплазматический домен нативного белка (остатки 126-158) увеличивает стабильность кристаллизованных образцов. Была создана модель KcsA с разрешением 3,2А, которая подтвердила тетрамерное расположение белка вокруг центральной поры, при этом одна спираль каждой субъединицы обращена к внутренней оси, а другая - наружу.[6] Три года спустя Мораис-Кабрал и Чжоу выпустили модель с более высоким разрешением. моноклональный Fab Фрагменты были прикреплены к кристаллам KcsA для дальнейшей стабилизации канала.[7] В начале 2000-х годов свидетельства заполнения фильтра селективности двумя K+ атом во время процесса переноса возник на основе энергетических и электростатических расчетов, сделанных для моделирования области поры. Продолжение исследований различных открытых и закрытых, неактивных и активных конформаций KcsA другими методами визуализации, такими как ssNMR и EPR с тех пор предоставили еще больше информации о структуре канала и силах, управляющих переключением от инактивации канала к проводимости.
В 2007 году Riek et. Al. показал, что открытие канала в результате титрование ионный канал от pH 7 до pH 4 соответствует конформационным изменениям в двух областях: переходу в ионообменное состояние фильтра селективности и открытию расположения TM2 в C-конец.[8] Эта модель объясняет способность KcsA одновременно выбирать для K+ ионы при этом также регулируется электрическая проводимость. В 2011 г. кристаллическая структура полноразмерного KcsA была разрешена, чтобы выявить, что препятствие со стороны ранее усеченных остатков позволяет только прямое расширение области межклеточного прохождения ионов белка. Это исследование позволяет более подробно изучить движение отдельных участков канала при ионной проводимости.[9] В настоящее время исследования KcsA сосредоточены на использовании прокариотического канала в качестве модели динамики канала более крупных эукариотических K+ каналы, в том числе hERG.
Структура

Структура KcsA - это перевернутая конус, с центральной порой, идущей вниз по центру, состоящей из двух трансмембранных спирали (внешняя спираль M1 и внутренняя спираль M2), которые охватывают липидный бислой. Сам канал является тетрамер состоящий из четырех идентичных однодоменных субъединиц (каждая с двумя α-спиралями), расположенных так, что одна спираль M2 обращена к центральной поре, а другая спираль M1 обращена к липидная мембрана. Внутренние спирали наклонены примерно на 25 ° по отношению к липидная мембрана и слегка изогнуты, раскрываясь наружу клетки, как цветок.[6] Эти две спирали TM связаны входящей петлей, симметрично распределенной вокруг общей оси, соответствующей центральной оси. поры. Область пор охватывает примерно 30 аминокислотных остатков и может быть разделена на три части: селективный фильтр на внеклеточной стороне, расширенный, заполненный водой полость в центре и закрытые ворота возле цитоплазматической стороны, образованные четырьмя упакованными спиралями M2.[6] Обнаружено, что эта архитектура очень консервативна в калиевых канальная семья[10][11] в обоих эукариоты и прокариоты.
Общая длина поры составляет 45 Å, а ее диаметр значительно варьируется в различных областях внутреннего туннеля. Путешествие из внутриклеточный область наружу (снизу вверх на картинке) поры начинается с области ворот, образованной спиралями M2 диаметром 18 Å, а затем открывается в широкую полость (∼10 Å в поперечнике) около середины мембраны.[6] В этих регионах K+ ионы находятся в контакте с окружающими молекулами воды, но когда они входят в канал из фильтра селективности вверху, полость настолько узкая, что K+ ионы должны избавляться от гидратирующих вод, чтобы попасть в клетку.[6] Что касается аминокислота состав остатков выстилки пор внутри KcsA, боковые цепи, выстилающие внутреннюю пору и полость, преимущественно гидрофобный, но в фильтре селективности полярный аминокислоты, которые контактируют с дегидратированным K+ ионы.
Фильтр селективности
Более широкий конец конуса соответствует внеклеточный устье канала, состоящее из спиралей пор, плюс фильтр селективности который формируется TVGYG последовательность (треонин, валин, глицин, тирозин, глицин), характерная для калиевых каналов.[12] В этой области координация между аминокислотами TVGYG и поступающим K+ Ионы позволяют проводить ионы через канал. Фильтр селективности KcsA содержит четыре сайта связывания ионов, хотя предполагается, что только два из этих четырех положений заняты одновременно. Фильтр селективности имеет диаметр около 3 Å.[13] хотя молекулярная динамика моделирование предполагает, что фильтр гибкий.[14] Присутствие TVGYG в фильтрующей области KcsA сохраняется даже в более сложных эукариотических каналах, что делает KcsA оптимальной системой для изучения K+ проводимость каналов между видами.
Функция

Канал KcsA считается модельным канал поскольку структура KcsA обеспечивает основу для понимания K+ канал проводимости, который состоит из трех частей: Калий избирательность стробирование канала с помощью чувствительности к pH и инактивация канала с регулируемым напряжением. K+ ион проникновение происходит в верхней области фильтра селективности поры, а pH гейтинг поднимается из протонирование из трансмембранный спирали на конце поры. При низком pH спираль M2 протонируется, смещая ионный канал из закрытой в открытую конформацию.[15] Считается, что когда ионы проходят через канал, механизмы стробирования напряжения вызывают взаимодействия между Glu71 и Asp80 в фильтре селективности, которые дестабилизируют проводящую конформацию и облегчают переход в долгоживущее непроводящее состояние, которое напоминает инактивацию типа C каналы, зависимые от напряжения.[16]
В непроводящей конформации KcsA при pH 7 K+ тесно связан с координирующими атомами кислорода селективного фильтра и четырех TM2 спирали сходятся около цитоплазматический переход, чтобы заблокировать прохождение любых ионов калия.[8] Однако при pH 4 KcsA претерпевает конформационные обмены в миллисекундном масштабе времени, фильтруя проницаемые и непроницаемые состояния, а также между открытой и закрытой конформациями спиралей M2.[8] Хотя эти отчетливые конформационные изменения происходят в отдельных областях канала, молекулярное поведение каждой области связано как электростатические взаимодействия и аллостерия.[8] Динамика этих обменных стереохимических конфигураций в фильтре обеспечивает физическую основу для одновременного K+ проводимость и стробирование.
K+избирательность
Последовательность TVGYG особенно важна для поддержания калиевой специфичности KcsA. Глицины в этой последовательности фильтров селективности имеют двугранные углы, которые позволяют карбонильным атомам кислорода в белковой основе фильтра указывать в одном направлении, к ионам вдоль поры.[5] Глицины и треонин координируются с K+ ion, в то время как боковые цепи валина и тирозина направлены в ядро белка, чтобы наложить геометрические ограничения на фильтр. В результате тетрамер KcsA содержит четыре одинаковых K+ места связывания, каждая сторона которых состоит из клетки, образованной восемью атомами кислорода, которые находятся в вершинах куба. Атомы кислорода, окружающие K+ ионы в фильтре расположены как молекулы воды, которые окружают гидратированный K+ ионы в полости канала; это говорит о том, что центры координации и связывания кислорода в фильтре селективности оплачивают энергетические затраты K+ обезвоживание.[5] Поскольку ион Na + слишком мал для этих K+-размерные сайты связывания, энергия дегидратации не компенсируется и, таким образом, фильтр осуществляет селекцию против других посторонних ионов.[5] Кроме того, канал KcsA заблокирован CS+ ионы и ворота требует наличия Mg2+ ионы.[1]
чувствительность pH
PH-зависимая проводимость KcsA указывает на то, что открытие ионного канала происходит, когда белок подвергается воздействию более кислой среды. Исследования ЯМР, проведенные группой Riek, показывают, что чувствительность к pH проявляется как в C-концевой области TM2 белка, так и в остатках Tyr78 и Gly79 в фильтре селективности. Есть основания полагать, что основной датчик pH находится в цитоплазматическом домене. Замена отрицательно заряженных аминокислот на нейтральные сделала канал KcsA нечувствительным к pH, даже несмотря на отсутствие аминокислотных изменений в трансмембранной области.[17][18] Кроме того, при pH от 6 до 7 гистидин является одной из немногих титруемых боковых цепей гистидинов; они отсутствуют в трансмембранных и внеклеточных сегментах TM2, но присутствуют на C-конце KcsA. Это подчеркивает возможный механизм медленного открытия KcsA, который особенно чувствителен к pH, особенно потому, что конформационное распространение сигнала открытия канала от C-конца к фильтру селективности может быть важным для координации структурных изменений, необходимых для проводимости по всей поре. .
Исследования ЯМР также предполагают, что сложная сеть водородных связей между Tyr78, Gly79, Glu71 и Asp80 существует в области фильтра KcsA и, кроме того, действует как pH-чувствительный триггер для проводимости. Мутация ключевых остатков в этом регионе, включая E71A, приводит к большим энергетическим затратам - 4 ккал / моль.−1, что эквивалентно потере водородной связи между Glu71 и Tyr78 и опосредованной водой водородной связи между Glu71 и Asp80 в KcsA (E71A). Эти исследования дополнительно подчеркивают роль гейтирования pH в функции канала KcsA.
Стробирование напряжения
В 2006 году группа Perozo предложила механистическое объяснение влияния полей напряжения на стробирование KcsA. После добавления в канал деполяризующего тока происходит переориентация Glu71 по направлению к внутриклеточной поре, тем самым разрушая карбоксилкарбоксилатную пару Glu71-Asp80, которая изначально стабилизирует фильтр селективности. Сжатие области фильтра предотвращает вход в неактивное состояние или облегчает выход из него.[16] Glu71, ключевая часть последовательности сигнатуры фильтра селективности, которая сохраняется среди K+ ионных каналов, играет ключевую роль в стробировании, так как его способность переориентировать себя в направлении трансмембранного поля напряжения способна объяснить события стробирования напряжения в KcsA. Ориентация аминокислот в фильтрующей области может играть важную физиологическую роль в модуляции потоков калия у эукариот и прокариот в стационарных условиях.[16]
Исследование
Функция
Точный механизм селективности калиевых каналов остается открытым. изучал и обсуждал и несколько моделей используются для описания различных аспектов избирательности. Модели, объясняющие селективность на основе концепции напряженности поля, разработанной Джорджем Эйзенманом[19] на основе Закон Кулона были применены к KcsA.[14][20] Альтернативное объяснение избирательности KcsA основано на модели плотного прилегания (также известной как модель плотного прилегания), разработанной Benzanilla и Армстронг.[21] В основная цепь карбонильные атомы кислорода, составляющие селективный фильтр, удерживаются в точном положении, которое позволяет им заменять молекулы воды в гидратированная оболочка из калий ион, но они слишком далеки от натрий ион. Дальнейшая работа посвящена изучению термодинамических различий в связывании ионов,[22] топологические соображения,[23][24] и количество участков непрерывного связывания ионов.[25]
Кроме того, основное ограничение исследования кристаллической структуры и симуляции еще предстоит обсудить: наиболее разрешенная и наиболее применяемая кристаллическая структура KcsA, по-видимому, представляет собой «закрытую» форму канала. Это разумно, так как закрытое состояние канала благоприятно для нейтральный pH, при котором кристаллическая структура решалась методом Рентгеновская кристаллография. Однако динамическое поведение KcsA затрудняет анализ канала, поскольку кристаллическая структура неизбежно обеспечивает статическое, усредненное по пространству и времени изображение канала. Чтобы преодолеть разрыв между молекулярной структурой и физиологическим поведением, необходимо понимание динамики атомного разрешения калиевых каналов.
Приложения
Из-за высокого сходства последовательностей поры KcsA и других эукариотических K+ белков ионных каналов, KcsA предоставил важную информацию о поведении других важных проводящих напряжение белков, таких как дрозофилла -производный Шейкер и человек hERG калиевый канал. KcsA использовался в мутагенез исследования по моделированию взаимодействия между hERG и различные лекарственные соединения. Такие тесты могут выявить взаимодействия наркотиков и каналов hERG, которые вызывают приобретенный синдром удлиненного интервала QT, необходимы для определения сердечного безопасность новых лекарств.[26] Кроме того, модели гомологии, основанные на кристаллической структуре KcsA с замкнутым состоянием, были сгенерированы с помощью вычислений для построения представления нескольких состояний сердечного K hERG.+ канал. Такие модели показывают гибкость канала hERG и могут последовательно предсказывать сродство связывания набора различных лигандов, взаимодействующих с ионным каналом. Анализ сложных структур лиганд-hERG может быть использован для управления синтезом аналогов лекарств с пониженной предрасположенностью к hERG на основе структуры лекарственного средства и потенциала стыковки.[27]
Смотрите также
использованная литература
- ^ а б c Schrempf H, Schmidt O, Kümmerlen R, Hinnah S, Müller D, Betzler M, Steinkamp T., Wagner R (ноябрь 1995 г.). «Прокариотический ионный канал калия с двумя предсказанными трансмембранными сегментами из Streptomyces lividans». Журнал EMBO. 14 (21): 5170–8. Дои:10.1002 / j.1460-2075.1995.tb00201.x. ЧВК 394625. PMID 7489706.
- ^ Мейзер Д., Сплитт Х., Вагнер Р., Шремпф Х. (1999). «Изучение открытой поры калиевого канала от Streptomyces lividans". Письма FEBS. 462: 447–452. Дои:10.1016 / S0014-5793 (99) 01579-3.
- ^ Ю. Ф. Х., Яров-Яровой В., Гутман Г. А., Каттералл В. А. (декабрь 2005 г.). «Обзор молекулярных отношений в суперсемействе потенциалзависимых ионных каналов». Фармакологические обзоры. 57 (4): 387–95. Дои:10.1124 / пр.57.4.13. PMID 16382097.
- ^ Ру Б (2005). «Ионная проводимость и селективность в K (+) каналах». Ежегодный обзор биофизики и структуры биомолекул. 34: 153–71. Дои:10.1146 / annurev.biophys.34.040204.144655. PMID 15869387.
- ^ а б c d Родерик Маккиннон. «Нобелевская лекция: Калиевые каналы и атомные основы селективной ионной проводимости». Nobelprize.org. Nobel Media AB.
- ^ а б c d е Дойл Д.А., Мораис Кабрал Дж., Пфуэцнер Р.А., Куо А., Гулбис Дж.М., Коэн С.Л., Чайт Б.Т., Маккиннон Р. (апрель 1998 г.). «Строение калиевого канала: молекулярная основа K+ проводимость и избирательность ». Наука. 280 (5360): 69–77. Bibcode:1998 Наука ... 280 ... 69D. Дои:10.1126 / science.280.5360.69. PMID 9525859.
- ^ Чжоу Ю., Мораис-Кабрал Дж. Х., Кауфман А., Маккиннон Р. (ноябрь 2001 г.). "Химия ионной координации и гидратации, выявленная методом K+ комплекс канал-Фаб в разрешении 2,0 А ». Природа. 414 (6859): 43–8. Bibcode:2001Натура 414 ... 43Z. Дои:10.1038/35102009. PMID 11689936.
- ^ а б c d Бейкер К.А., Цицилонис К., Квятковски В., Чхве С., Рик Р. (ноябрь 2007 г.). «Конформационная динамика калиевого канала KcsA определяет вентильные свойства». Структурная и молекулярная биология природы. 14 (11): 1089–95. Дои:10.1038 / nsmb1311. ЧВК 3525321. PMID 17922011.
- ^ Uysal S, Cuello LG, Cortes DM, Koide S, Kossiakoff AA, Perozo E (июль 2011 г.). «Механизм активации стробирования в полноразмерном KcsA K+ канал ". Труды Национальной академии наук Соединенных Штатов Америки. 108 (29): 11896–9. Bibcode:2011PNAS..10811896U. Дои:10.1073 / pnas.1105112108. ЧВК 3141920. PMID 21730186.
- ^ Лу З., Клем А.М., Раму Й. (октябрь 2001 г.). «Пора ионной проводимости сохраняется среди калиевых каналов». Природа. 413 (6858): 809–13. Дои:10.1038/35101535. PMID 11677598.
- ^ Choe S (февраль 2002 г.). «Структуры калиевых каналов». Обзоры природы. Неврология. 3 (2): 115–21. Дои:10.1038 / nrn727. PMID 11836519.
- ^ Хилле Б., Армстронг К.М., Маккиннон Р. (октябрь 1999 г.). «Ионные каналы: от идеи к реальности». Природа Медицина. 5 (10): 1105–9. Дои:10.1038/13415. PMID 10502800.
- ^ Хилле Б. (июнь 1973 г.). «Калиевые каналы в миелинизированном нерве. Избирательная проницаемость для малых катионов». Журнал общей физиологии. 61 (6): 669–86. Дои:10.1085 / jgp.61.6.669. ЧВК 2203488. PMID 4541077.
- ^ а б Носков С.Ю., Ру Б. (декабрь 2006 г.). «Ионная селективность в калиевых каналах». Биофизическая химия. 124 (3): 279–91. Дои:10.1016 / j.bpc.2006.05.033. PMID 16843584.
- ^ Томпсон А. Н., Посон Д. Д., Парса П. В., Нимиджин С. М. (май 2008 г.). «Молекулярный механизм определения pH в калиевых каналах KcsA». Труды Национальной академии наук Соединенных Штатов Америки. 105 (19): 6900–5. Дои:10.1073 / pnas.0800873105. ЧВК 2383984. PMID 18443286.
- ^ а б c Кордеро-Моралес Дж. Ф., Куэлло Л. Г., Чжао Ю., Джогини В., Кортес Д. М., Ру Б., Перозо Е. (апрель 2006 г.). «Молекулярные детерминанты стробирования на фильтре селективности калиевого канала». Структурная и молекулярная биология природы. 13 (4): 311–8. Дои:10.1038 / nsmb1069. PMID 16532009.
- ^ Хирано М., Ониши Ю., Янагида Т., Иде Т. (ноябрь 2011 г.). «Роль цитоплазматического домена канала KcsA в pH-зависимом гейтинге». Биофизический журнал. 101 (9): 2157–62. Bibcode:2011BpJ ... 101.2157H. Дои:10.1016 / j.bpj.2011.09.024. ЧВК 3207171. PMID 22067153.
- ^ Ючи З., Пау В.П., Ян Д.С. (декабрь 2008 г.). «GCN4 увеличивает стабильность порового домена калиевого канала KcsA». Журнал FEBS. 275 (24): 6228–36. Дои:10.1111 / j.1742-4658.2008.06747.x. PMID 19016844.
- ^ Эйзенман Г (март 1962 г.). «Катионоселективные стеклянные электроды и режим их работы». Биофизический журнал. 2 (2, ч. 2): 259–323. Дои:10.1016 / S0006-3495 (62) 86959-8. ЧВК 1366487. PMID 13889686.
- ^ Носков С.Ю., Бернеш С., Ру Б. (октябрь 2004 г.). «Управление ионной селективностью в калиевых каналах с помощью электростатических и динамических свойств карбонильных лигандов». Природа. 431 (7010): 830–4. Bibcode:2004Натура 431..830Н. Дои:10.1038 / природа02943. PMID 15483608.
- ^ Безанилла Ф., Армстронг К.М. (ноябрь 1972 г.). «Отрицательная проводимость, вызванная попаданием ионов натрия и цезия в калиевые каналы аксонов кальмаров». Журнал общей физиологии. 60 (5): 588–608. Дои:10.1085 / jgp.60.5.588. ЧВК 2226091. PMID 4644327.
- ^ Варма С., Ремпе С.Б. (август 2007 г.). «Настройка архитектуры ионной координации для обеспечения селективного разделения». Биофизический журнал. 93 (4): 1093–9. Bibcode:2007BpJ .... 93.1093V. Дои:10.1529 / biophysj.107.107482. ЧВК 1929028. PMID 17513348.
- ^ Томас М., Джаятилака Д., Корри Б. (октябрь 2007 г.). «Преобладающая роль координационного числа в селективности калиевых каналов». Биофизический журнал. 93 (8): 2635–43. Bibcode:2007BpJ .... 93.2635T. Дои:10.1529 / biophysj.107.108167. ЧВК 1989715. PMID 17573427.
- ^ Бостик Д.Л., Брукс С.Л. (май 2007 г.). «Селективность в K+ каналов обусловлено топологическим контролем согласованного состояния проникающего иона ». Труды Национальной академии наук Соединенных Штатов Америки. 104 (22): 9260–5. Bibcode:2007ПНАС..104.9260Б. Дои:10.1073 / pnas.0700554104. ЧВК 1890482. PMID 17519335.
- ^ Деребе М.Г., Зауэр Д.Б., Цзэн В., Алам А., Ши Н., Цзян Ю. (январь 2011 г.). «Настройка ионной селективности тетрамерных катионных каналов путем изменения числа сайтов связывания ионов». Труды Национальной академии наук Соединенных Штатов Америки. 108 (2): 598–602. Bibcode:2011ПНАС..108..598D. Дои:10.1073 / pnas.1013636108. ЧВК 3021048. PMID 21187421.
- ^ Sanguinetti MC, Mitcheson JS (март 2005 г.). «Прогнозирование взаимодействий наркотиков и каналов hERG, которые вызывают синдром приобретенного удлиненного интервала QT». Тенденции в фармакологических науках. 26 (3): 119–24. Дои:10.1016 / j.tips.2005.01.003. PMID 15749156.
- ^ Rajamani R, Tounge BA, Li J, Reynolds CH (март 2005 г.). "Модель с двумя состояниями гомологии hERG K+ канал: приложение к связыванию лиганда ». Письма по биоорганической и медицинской химии. 15 (6): 1737–41. Дои:10.1016 / j.bmcl.2005.01.008. PMID 15745831.
