Типирование ткани - Tissue typing
Типирование ткани это процедура, при которой ткани предполагаемого донора и реципиента проверяются на совместимость до трансплантация. Несоответствие тканей донора и реципиента может привести к отторжению тканей. Существует несколько методов тканевого типирования.
Обзор

Во время типирования тканей индивидуальные человеческие лейкоцитарные антигены (HLA) идентифицированы.[1] Молекулы HLA представлены на поверхности клеток и способствуют взаимодействию между иммунными клетками (например, дендритные клетки и Т-клетки ), которые приводят к адаптивные иммунные ответы.[2] Если HLA от донора распознается иммунной системой реципиента как отличный от собственного HLA реципиента, может быть запущен иммунный ответ против донорских тканей.[3] В частности, несоответствие HLA между донорами органов и реципиентами может привести к развитию анти-HLA. донор-специфические антитела (DSA).[4] DSA тесно связаны с отторжением донорских тканей у реципиента, и их присутствие считается показателем опосредованного антителами отторжения.[5] Когда HLA донора и реципиента совпадают, донорские ткани значительно более вероятно будут приняты иммунной системой реципиента.[3] Во время типирования ткани необходимо типировать ряд генов HLA как у донора, так и у реципиента, включая HLA класса I А, B, и C гены, а также HLA класса II DRB1, DRB3, DRB4, DRB5, DQA1, DQB1, DPA1, и DPB1 гены.[6] HLA-типирование осложняется тем фактом, что область HLA является наиболее генетически изменчивой областью в геноме человека.[7]
Методы тканевого типирования
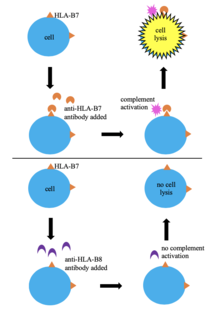
Одним из первых методов тканевого типирования было серологическое типирование. В этом методе клетки донорской крови HLA набирается путем смешивания их с сыворотка содержащий анти-HLA антитела. Если антитела узнают свои эпитоп на HLA донора, затем дополнять происходит активация приводит к клетке лизис и смерть, позволяя клеткам впитывать краситель (трипановый синий ). Это позволяет идентифицировать HLA клеток, косвенно основываясь на специфичности известных антител в сыворотке. Этот метод широко используется, поскольку он простой, быстрый и недорогой; однако огромное разнообразие HLA аллели означает, что сыворотка, содержащая антитела, специфичные к HLA тестируемых клеток, может быть недоступна.[6][8] Серологическое типирование не дает четкой картины региона HLA и не всегда приводит к успешному типированию HLA, поэтому многие лаборатории отказались от его использования в пользу более эффективных методов.[6][9]
В последнее время появились другие более эффективные подходы, в том числе использование полимеразной цепной реакции (ПЦР ) на основе праймеров, специфичных для последовательности (SSP), или специфичных для последовательности олигонуклеотид зонды (SSOP).[3][6] Однако SSP-PCR может потребовать как времени, так и ресурсов.[9] SSOP-PCR лучше подходит для HLA-типирования большого числа людей, например большого числа доноров для регистров костного мозга.[9] ОТ-ПЦР - еще один подход к HLA-типированию, быстрый и универсальный, но дорогой.[6]
Опосредованный эталонной цепью конформационный анализ (RSCA) - еще один метод, используемый для HLA-типирования. В этом методе образец неизвестного HLA смешивается с эталонным аллелем и прогоняется в геле с помощью электрофорез.[9] RSCA ограничивается количеством доступных референсных аллелей HLA, поскольку область HLA очень разнообразна.[9]
Прямой Секвенирование ДНК в настоящее время считается лучшим методом HLA-типизации, либо Секвенирование по Сэнгеру или же секвенирование следующего поколения, хотя это также может занять много времени и является одним из самых дорогих методов.[6][9] Секвенирование РНК также можно использовать, но многие лаборатории этого не делают, поскольку РНК нестабильна и подвержена деградации.[9]
Рекомендации
- ^ Mulley, William R .; Хадсон, Фиона; Ли, Даррен; Холдсуорт, Ронда Ф. (2019). «Тканевое типирование при трансплантации почки для общего нефролога». Нефрология. 24 (10): 997–1000. Дои:10.1111 / nep.13637. ISSN 1440-1797. PMID 31335997.
- ^ Назахах, М .; Ко, М. Б. С. (2015). «Типирование тканей и его роль в трансплантации». Научная серия ISBT. 10 (S1): 115–123. Дои:10.1111 / voxs.12168. ISSN 1751-2824.
- ^ а б c Махди, Батул Мутар (23 февраля 2013 г.). «Свечение HLA-типирования при трансплантации органов». Клиническая и трансляционная медицина. 2 (1): 6. Дои:10.1186/2001-1326-2-6. ISSN 2001-1326. ЧВК 3598844. PMID 23432791.
- ^ Аргани, Хасан (январь 2019 г.). «Антитело против HLA: роль эпитопов в трансплантации органов». Экспериментальная и клиническая трансплантация. 17 (Дополнение 1): 38–42. Дои:10.6002 / ect.MESOT2018.L41. PMID 30777521.
- ^ Чжан, Рубин (06.01.2018). «Донор-специфические антитела у реципиентов трансплантата почки». Клинический журнал Американского общества нефрологов. 13 (1): 182–192. Дои:10.2215 / CJN.00700117. ISSN 1555-9041. ЧВК 5753302. PMID 28446536.
- ^ а б c d е ж Деальо, Сильвия; Аморосо, Антонио; Ринальди, Мауро; Боффини, Массимо (13 февраля 2020 г.). «HLA-типирование при трансплантации легких: всем ли подходит высокое разрешение?». Анналы трансляционной медицины. 8 (3): 45. Дои:10.21037 / атм.2020.01.45. ISSN 2305-5847. ЧВК 7036624. PMID 32154803.
- ^ Кишор, Амит; Петрек, Мартин (2018). «Типирование HLA на основе секвенирования нового поколения: расшифровка иммуногенетических аспектов саркоидоза». Границы генетики. 9: 503. Дои:10.3389 / fgene.2018.00503. ISSN 1664-8021. ЧВК 6210504. PMID 30410504.
- ^ Махди, Батул Мутар (23 февраля 2013 г.). «Свечение HLA-типирования при трансплантации органов». Клиническая и трансляционная медицина. 2 (1): 6. Дои:10.1186/2001-1326-2-6. ISSN 2001-1326. ЧВК 3598844. PMID 23432791.
- ^ а б c d е ж грамм Данн, П. П. Дж. (2011). «Типирование лейкоцитарного антигена человека: методы и технологии, критическая оценка». Международный журнал иммуногенетики. 38 (6): 463–473. Дои:10.1111 / j.1744-313X.2011.01040.x. ISSN 1744–313X. PMID 22059555.
