Неоднородность опухоли - Tumour heterogeneity
Неоднородность опухоли описывает наблюдение, что разные опухолевые клетки может показать отчетливый морфологический и фенотипический профили, включая морфологию клетки, экспрессию генов, метаболизм, подвижность, пролиферацию и метастатический потенциал.[1] Это явление происходит как между опухолями (межопухолевая гетерогенность), так и внутри опухолей (внутриопухолевая гетерогенность). Минимальный уровень внутриопухолевой гетерогенности - простое следствие несовершенства Репликация ДНК: всякий раз, когда клетка (нормальная или злокачественная) делится, несколько мутации приобретены[2]- ведущая к разнообразной популяции раковых клеток.[3] В неоднородность раковых клеток представляет серьезные проблемы при разработке эффективных стратегий лечения. Однако исследования в области понимания и характеристики неоднородности могут позволить лучше понять причины и прогрессирование заболевания. В свою очередь, это может привести к созданию более совершенных стратегий лечения, которые включают знания о неоднородности для повышения эффективности.[4]
Неоднородность опухоли наблюдалась в лейкемии,[5] грудь,[6] предстательная железа,[7][8][9] двоеточие,[10][11][12] мозг,[13] пищевод,[14] Голова и шея,[15] мочевой пузырь[16] и гинекологические карциномы,[17] липосаркома,[18] и множественная миелома.[19]
Модели неоднородности
Есть две модели, используемые для объяснения неоднородности опухолевых клеток. Эти раковые стволовые клетки модель и клональная эволюция модель. Модели не исключают друг друга, и считается, что обе они вносят свой вклад в неоднородность в разной степени в разных типах опухолей.[20]
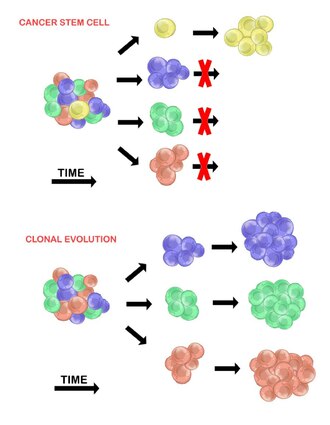
Раковые стволовые клетки
Модель раковых стволовых клеток утверждает, что в популяции опухолевых клеток существует лишь небольшое подмножество клеток, которые онкогенный (способны образовывать опухоли). Эти клетки называются раковыми стволовыми клетками (CSC), и отмечены способностью как к самообновлению, так и к дифференцировке в неопухолевое потомство. Модель CSC утверждает, что наблюдаемая гетерогенность между опухолевыми клетками является результатом различий в стволовых клетках, из которых они произошли. Вариабельность стволовых клеток часто вызвана: эпигенетический изменений, но также может быть результатом клональной эволюции популяции CSC, где благоприятные генетические мутации могут накапливаться в РСК и их потомстве (см. ниже).[20]
Доказательства модели раковых стволовых клеток были продемонстрированы на множестве типов опухолей, включая лейкемии,[21][22] глиобластома,[23] рак молочной железы,[24] и рак простаты.[25]
Однако существование CSC все еще обсуждается. Одна из причин этого заключается в том, что маркеры CSC трудно воспроизводить в нескольких опухолях. Кроме того, в методах определения опухолевого потенциала используются ксенотрансплантат модели. Эти методы страдают от присущих им ограничений, таких как необходимость контролировать иммунный ответ у трансплантата животного, а также значительные различия в условиях окружающей среды от первичного очага опухоли до участка ксенотрансплантата (например отсутствие необходимых экзогенных молекул или кофакторов).[26] Это вызвало некоторые сомнения в точности результатов CSC и выводов о том, какие клетки обладают опухолевым потенциалом.
Клональная эволюция
Модель клональной эволюции была впервые предложена в 1976 г. Питер Новелл.[27] В этой модели опухоли возникают из одной мутировавшей клетки, накапливая дополнительные мутации по мере своего развития. Эти изменения приводят к появлению дополнительных субпопуляций, и каждая из этих субпопуляций имеет возможность делиться и мутировать дальше. Эта неоднородность может привести к появлению субклонов, обладающих эволюционное преимущество над другими внутри опухолевая среда, и со временем эти субклоны могут стать доминирующими в опухоли.[28][29] Когда эта модель была предложена, она позволила понять рост опухоли, неэффективность лечения и агрессию опухоли, которая происходит во время естественного процесса образования опухоли.[28]
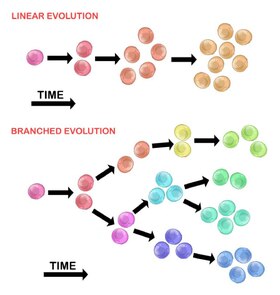
Эволюция исходной опухолевой клетки может происходить двумя способами:
Линейное расширение
Последовательно упорядоченные мутации накапливаются в генах-драйверах, гены-супрессоры опухолей, и Ремонт ДНК ферменты, приводящие к клональной экспансии опухолевых клеток. Линейное расширение с меньшей вероятностью отражает конечную точку злокачественной опухоли.[30] потому что в гетерогенных опухолях накопление мутаций является стохастическим.
Разветвленное расширение
Экспансия на несколько субклональных популяций происходит за счет механизма расщепления.[28] Этот метод больше связан с неоднородностью опухоли, чем с линейным расширением. Приобретение мутаций происходит случайно в результате увеличения геномная нестабильность с каждым последующим поколением. Длительное мутационное накопление может обеспечить селективное преимущество на определенных этапах прогрессирования опухоли. В микросреда опухоли может также способствовать разрастанию опухоли, поскольку он способен изменять селективное давление, которому подвергаются опухолевые клетки.[30]
Виды и причины неоднородности
Между опухолевыми клетками наблюдались множественные типы гетерогенности, обусловленные как генетической, так и негенетической изменчивостью.[31]
Генетическая гетерогенность
Генетическая гетерогенность является общей чертой опухолевых геномов и может происходить из нескольких источников. Некоторые виды рака возникают, когда экзогенные факторы вызывают мутации, такие как ультрафиолетовое излучение (рак кожи) и табак (рак легких). Более частым источником является геномная нестабильность, которая часто возникает, когда в клетках нарушаются ключевые регуляторные пути. Некоторые примеры включают слабых Ремонт ДНК механизмы, которые могут привести к увеличению количества ошибок репликации и дефектов в митоз оборудование, позволяющее получить крупную прибыль или потерять все хромосомы.[32] Кроме того, некоторые методы лечения рака могут дополнительно увеличить генетическую изменчивость (например лечение с темозоломид и другие химиотерапия наркотики).[33][34]
Мутационная гетерогенность опухоли относится к вариациям частоты мутаций в различных генах и образцах и может быть исследована MutSig. Этиология мутационных процессов может значительно различаться между образцами опухолей одного или разных типов рака и может проявляться в различных контекстно-зависимых мутационных профилях. Его можно изучить COSMIC мутационные сигнатуры или же MutaGene.
Другая неоднородность
Опухолевые клетки также могут демонстрировать гетерогенность между профилями экспрессии. Это часто вызвано лежащими в основе эпигенетический изменения.[31]Изменения в сигнатуре экспрессии были обнаружены в различных областях образцов опухоли у человека. Исследователи показали, что конвергентные мутации, влияющие на H3K36 метилтрансфераза SETD2 и гистон H3K4 деметилаза KDM5C возникли в пространственно разделенных срезах опухоли. По аналогии, MTOR, ген, кодирующий регуляторную клетку киназа, показал себя постоянно активным, тем самым увеличивая S6 фосфорилирование. Этот активный фосфорилирование может служить биомаркер при светлоклеточном раке.[30]
Механохимический неоднородность - признак жизни эукариотический клетки. Это влияет на эпигенетический генная регуляция. Гетерогенные динамические механохимические процессы регулируют взаимоотношения внутри группы клеточных поверхностей посредством адгезия.[35] Развитие и распространение опухоли сопровождается изменением неоднородной хаотическая динамика процесса механохимического взаимодействия в группе клеток, включая клетки внутри опухоли, и является иерархическим для хозяина больных раком.[36] Биологические явления механохимической неоднородности могут быть использованы для дифференциальной рак желудка диагностика пациентов с воспаление из слизистая желудка[37] и для повышения антиметастатической активности дендритные клетки на основе вакцина при механической гетерогенизации микрочастицы опухолевых клеток используются для их загрузки.[38] Существует также возможный методический подход, основанный на одновременной диагностике и терапии ультразвуковой визуализацией, касающийся механохимического воздействия на конгломераты наночастиц с лекарствами в опухоли.
Микроокружение опухоли
Неоднородность между опухолевыми клетками может быть дополнительно увеличена из-за гетерогенности в микросреда опухоли. Региональные различия опухоли (например доступность кислорода) оказывают различное избирательное давление на опухолевые клетки, что приводит к более широкому спектру доминирующих субклонов в различных пространственных областях опухоли. Влияние микросреды на клональное доминирование также является вероятной причиной гетерогенности между первичным и метастатический опухоли, наблюдаемые у многих пациентов, а также неоднородность между опухолями, наблюдаемая между пациентами с одним и тем же типом опухоли.[39]
Последствия и проблемы
Устойчивость к лечению
Гетерогенные опухоли могут проявлять различную чувствительность к цитотоксические препараты среди различных клональных популяций. Это связано с клональными взаимодействиями, которые могут подавлять или изменять терапевтическую эффективность, что создает проблему для успешного лечения гетерогенных опухолей (и их гетерогенных метастазов).[1]
Применение лекарств при гетерогенных опухолях редко убивает все опухолевые клетки. Начальная популяция гетерогенных опухолей может горлышко бутылки, так что немногие устойчивые к лекарствам клетки (если таковые имеются) выживут. Это позволяет популяциям устойчивых опухолей реплицироваться и выращивать новую опухоль посредством механизма ветвления эволюции (см. Выше). Образовавшаяся в результате репопуляция опухоль гетерогенная и устойчивая к применяемой начальной лекарственной терапии. Повторно заселенная опухоль также может вернуться более агрессивным образом.
Администрация цитотоксические препараты часто приводит к первоначальному уменьшению опухоли. Это представляет собой разрушение исходных неустойчивых субклональных популяций в гетерогенной опухоли, оставляя только устойчивые клоны. Эти устойчивые клоны теперь обладают избирательным преимуществом и могут реплицироваться для повторного заселения опухоли. Репликация, вероятно, будет происходить в результате эволюции ветвления, что способствует гетерогенности опухоли. Повторно заселенная опухоль может оказаться более агрессивной. Это объясняется селективным преимуществом опухолевых клеток в отношении устойчивости к лекарствам.

Открытие биомаркера
Из-за генетических различий внутри опухолей и между ними, биомаркеры которые могут предсказать ответ на лечение или прогноз, могут не иметь широкого применения. Однако было высказано предположение, что уровень гетерогенности сам по себе может использоваться в качестве биомаркера, поскольку более гетерогенные опухоли могут с большей вероятностью содержать устойчивые к лечению субклоны.[31] Дальнейшие исследования по разработке биомаркеров, учитывающих гетерогенность, все еще продолжаются.
Модельные системы
В современных модельных системах обычно отсутствует гетерогенность, наблюдаемая при раке человека.[40] Чтобы точно изучить гетерогенность опухоли, мы должны разработать более точные доклинические модели. Одна из таких моделей, ксенотрансплантат опухоли, полученный от пациента, показал отличную полезность в сохранении неоднородности опухолей, позволяя при этом детально изучить движущие силы клональной приспособленности.[41] Однако даже эта модель не может охватить всю сложность рака.
Текущие стратегии
Хотя проблема выявления, характеристики и лечения неоднородности опухоли все еще активно исследуется, были предложены некоторые эффективные стратегии, включая как экспериментальные, так и вычислительные решения.
Экспериментальный
- Целенаправленный подход: анализ конкретного генетического локус или набор локусов. Это может происходить путем обнаружения аллельного дисбаланса (ДНК опухоли сравнивают с ДНК зародышевой линии), амплификации участков хромосомы (РЫБЫ ), и / или секвенирования определенных генов. Этот метод используется для отслеживания эволюции конкретной интересующей мутации или для подтверждения мутации, которую исследователи могут заподозрить в опухоли.[1]
- Преимущество: позволяет анализировать определенные гены (т.е. гены-драйверы, супрессоры опухолей). Процесс прост с прямой интерпретацией результатов. РЫБЫ и иммунофлуоресценция позволяет сосредоточиться на подтипах опухолевых клеток.[1]
- Недостаток: при ограниченном анализе будут упущены дополнительные важные мутации и модели клональной экспансии. Аллельный дисбаланс может быть трудно проверить с помощью микросателлитных маркеров, поэтому требуется проверка независимым методом (т.е. РЫБЫ). РЫБЫ требует большого количества ячеек и трудоемок.[1]
- Полногеномный подход: анализ всего генома в образцах опухолей. Это можно сделать через кариотипирование или же сравнительная геномная гибридизация (CGH) для выявления хромосомных аномалий. Секвенирование биопсии опухоли становится все более распространенным явлением.[1]
- Преимущество: не полагается на предварительные знания для определения вариантов. кариотипирование определяет области крупных хромосомных аномалий. CGH обеспечивает беспристрастный охват и позволяет обнаруживать мелкомасштабные аллельные дисбалансы (Массивы SNP). Секвенирование позволит выявить любые варианты, которые способствуют гетерогенности опухоли.[1]
- Недостаток: сложно определить функциональное влияние вариантов (т.е. нейтральный или патогенный). Ограниченное разрешение. Кариотипирование культивируемых клеток может быть смещено в сторону преимущественного роста выбранных субпопуляций опухолевых клеток. Ограниченное разрешение в обоих методах.[1] Полногеномный подход может генерировать большие объемы данных и быть трудным для интерпретации.
- Стратегия мультирегиональной выборки: обычно требуется несколько послеоперационных образцов опухоли из отдельных участков микродиссекции опухоли. Важно избегать заражения незлокачественных клеток, чтобы гарантировать точное представление экспрессии генов и генетического состава только в опухолевых клетках. Анализ ДНК опухоли в пространственно разделенных областях позволяет построить трехмерную эволюционную модель неоднородности опухоли.[1] Мультирегиональная выборка часто используется в сочетании с общегеномным подходом для создания этой трехмерной модели расширения неоднородности.
- Продольный отбор: из-за прогрессирования опухоли или прогрессирования лечения в некоторых случаях использовалось получение образцов опухоли в несколько моментов времени. Это было предложено как надежный метод отслеживания клональной эволюции.[34][42][43] Однако на практике этот метод оказывается проблематичным, поскольку требует периодической инвазивной биопсии. Новое исследование использования циркулирующей внеклеточной опухолевой ДНК в крови может обеспечить неинвазивный способ выявления биомаркеров на протяжении всего лечения.[44] Продольный отбор образцов, используемый в сочетании с общегеномным подходом, позволит идентифицировать накопленные мутации опухолевых клеток с течением времени. Это, в свою очередь, может идентифицировать ключевые мутации драйвера (наблюдаемые в исходных образцах опухолей).
- Адаптивная терапия может использоваться для предотвращения дальнейшего роста опухоли путем корректировки дозы лекарства и времени введения лекарства на основе реакции опухоли. Предполагается, что эта стратегия предотвращает доминирование устойчивых вариантов в опухоли. Тем не менее, необходимы дополнительные исследования его применимости.[45]
Последовательность действий
- Массовое секвенирование опухоли может использоваться, когда ДНК извлекается из смеси опухолевых клеток и анализируется сразу. Наличие гетерогенных популяций опухолей (субклонов) создает дополнительные проблемы, такие как:
- Невозможность обнаружить мутации в редких субклонах. Поскольку эти мутации будут происходить с низкой частотой в объединенной выборке, они могут быть неотличимы от фонового шума. Тем не менее, активно разрабатываются многие вызывающие варианты, специально разработанные для данных о раке и направленные на выявление редких вариантов, присутствующих в более мелких субклональных популяциях.[46][47][48][49] Обычно они используют совпадающую нормальную ДНК как средство различения истинных соматическая вариация из вариация зародышевой линии и фоновая ошибка последовательности.
- Невозможность определить, какие субклоны содержат каждую мутацию. Поскольку данные объединены, неясно, какие мутации возникают одновременно и из каких популяций они происходят. Разрабатываются новые инструменты, которые пытаются разрешить клональную структуру с помощью частоты аллелей для наблюдаемых мутаций.[50]
- Секвенирование одной клетки это новый метод, который ценен для оценки неоднородности опухоли, поскольку он может характеризовать отдельные опухолевые клетки. Это означает, что весь мутационный профиль нескольких отдельных клеток может быть определен без неоднозначности. Несмотря на то, что с использованием современных технологий трудно оценить достаточно большое количество отдельных клеток для получения статистической мощности, данные об одноклеточных опухолях имеют множество преимуществ, в том числе:
- Умение построить филогенетическое дерево показывая эволюцию популяций опухолей. Использование полногеномных последовательностей или SNP на основе псевдопоследовательностей отдельных клеток, можно оценить эволюцию субклонов. Это позволяет идентифицировать популяции, которые сохраняются с течением времени, и может сузить список мутаций, которые потенциально могут дать преимущество роста или устойчивость к лечению для определенных субклонов.[51] Алгоритмы для вывода филогении опухоли из данных секвенирования одноклеточной ДНК включают SCITE,[52] ОнкоНЕМ,[53] SiFit,[54] SiCloneFit,[55] PhISCS,[56] и PhISCS-BnB.[57]
- Последовательность секций может быть проведено на нескольких участках одной солидной опухоли, а изменение частот мутаций на участках может быть проанализировано, чтобы сделать вывод о клональной структуре. Преимущества этого подхода перед однократным секвенированием включают большую статистическую мощность и доступность более точной информации о пространственном расположении образцов. Последние можно использовать для определения частоты клонов в срезах и получения информации о том, как опухоль развивается в космосе. Чтобы вывести генотипы клонов и филогенетические деревья, моделирующие эволюцию опухоли во времени, было разработано несколько вычислительных методов.[58][59][60] включая Clomial,[61] cloneHD,[62] PhyloWGS,[63] PyClone,[64] Глоя,[65] phyC,[66] Навес,[67] TargetClone, ddClone,[68] ПАСТРИ,[69] GLClone,[70] Черта,[71] WSCUnmix,[72] B-SCITE.,[73] ThetA,[74] SIFA,[75] Sclust,[76] SeqClone,[77] КОЛДЕР,[78] БАМСЭ,[79], Мелтос[80], SubMARine[81], и RNDCLONE.[82]
Смотрите также
Рекомендации
- ^ а б c d е ж грамм час я Марусык, А; Поляк, К (2010). «Гетерогенность опухоли: причины и последствия». Biochimica et Biophysica Acta (BBA) - Обзоры на рак. 1805 (1): 105–117. Дои:10.1016 / j.bbcan.2009.11.002. ЧВК 2814927. PMID 19931353.
- ^ Фогельштейн, Берт; Papadopoulos, N .; Велкулеску, В.Е .; Чжоу, S .; Diaz, L.A .; Кинзлер, К. (2013). "Пейзажи генома рака". Наука. 373 (6127): 1546–1556. Bibcode:2013Научный ... 339.1546V. Дои:10.1126 / наука.1235122. ЧВК 3749880. PMID 23539594.
- ^ Хеппнер, Г.А. (1984). «Неоднородность опухоли». Исследования рака. 44 (6): 2259–2265. PMID 6372991.
- ^ Reiter, Johannes G; Макохон-Мур, Элвин П.; Джеральд, Джеффри М; Хейде, Александр; Аттие, Марк А.; Кохутек, Захари А; Tokheim, Collin J; Браун, Алексия; ДеБласио, Рейн; Ниязов, Юлиана; Цукер, Аманда; Карчин, Рэйчел; Кинзлер, Кеннет В. Якобуцио-Донахью, Кристина А; Фогельштейн, Берт; Новак, Мартин А. (2018). «Минимальная гетерогенность функционального гена-водителя среди нелеченных метастазов». Наука. 361 (6406): 1033–1037. Дои:10.1126 / science.aat7171. ЧВК 6329287. PMID 30190408.
- ^ Кэмпбелл, П. Дж .; Pleasance, E.D .; Стивенс, П. Дж .; Дикс, E; Ранс, R; Гудхед, я; Следует, Г. А .; Green, A.R .; Futreal, P. A .; Страттон, М. Р. (2008). «Субклональные филогенетические структуры рака, выявленные с помощью сверхглубокого секвенирования». Труды Национальной академии наук. 105 (35): 13081–13086. Bibcode:2008PNAS..10513081C. Дои:10.1073 / pnas.0801523105. ЧВК 2529122. PMID 18723673.
- ^ Шипицин, М; Кэмпбелл, Л. Л .; Argani, P; Weremowicz, S; Bloushtain-Qimron, N; Яо, Дж; Никольская, Т; Серебряная, Т; Бероухим, Р; Ху, М; Галушка, М.К .; Сукумар, S; Паркер, Л. М .; Андерсон, К. С .; Harris, L.N .; Гарбер, Дж. Э .; Richardson, A. L .; Schnitt, S.J .; Никольский, У; Гельман, Р. С .; Поляк, К (2007). «Молекулярное определение неоднородности опухоли груди». Раковая клетка. 11 (3): 259–273. Дои:10.1016 / j.ccr.2007.01.013. PMID 17349583.
- ^ MacIntosh, C.A .; Стоуэр, М; Reid, N; Мейтленд, Н. Дж. (1998). «Точная микродиссекция рака простаты человека выявляет генотипическую гетерогенность». Исследования рака. 58 (1): 23–28. PMID 9426051.
- ^ Альварадо, К; Beitel, L.K .; Sircar, K; Априкян, А; Трифиро, М; Готтлиб, Б. (2005). «Соматический мозаицизм и рак: микрогенетическое исследование роли гена рецептора андрогена в раке простаты». Исследования рака. 65 (18): 8514–8518. Дои:10.1158 / 0008-5472.CAN-05-0399. PMID 16166332.
- ^ Кониши, Н; Hiasa, Y; Мацуда, H; Тао, М; Цузуки, Т; Хаяси, я; Китахори, Y; Сираиси, Т; Yatani, R; Симадзаки Дж. (1995). «Внутриопухолевая клеточная гетерогенность и изменения онкогена ras и гена-супрессора опухоли p53 в карциноме простаты человека». Американский журнал патологии. 147 (4): 1112–1122. ЧВК 1871010. PMID 7573356.
- ^ Гонсалес-Гарсия, I; Solé, R. V .; Коста, Дж. (2002). «Динамика метапопуляции и пространственная неоднородность при раке». Труды Национальной академии наук. 99 (20): 13085–13089. Bibcode:2002PNAS ... 9913085G. Дои:10.1073 / pnas.202139299. ЧВК 130590. PMID 12351679.
- ^ Samowitz, W. S .; Слэттери, М. Л. (1999). «Региональная воспроизводимость микросателлитной нестабильности при спорадическом колоректальном раке». Гены, хромосомы и рак. 26 (2): 106–114. Дои:10.1002 / (SICI) 1098-2264 (199910) 26: 2 <106 :: AID-GCC2> 3.0.CO; 2-F. PMID 10469448.
- ^ Джаретти, Вт; Монако, Р; Pujic, N; Рапалло, А; Нигро, S; Гейдо, Э (1996). «Внутриопухолевая гетерогенность мутаций K-ras2 при колоректальных аденокарциномах: ассоциация со степенью анеуплоидии ДНК». Американский журнал патологии. 149 (1): 237–245. ЧВК 1865212. PMID 8686748.
- ^ Хеппнер, Г. Х. (1984). «Неоднородность опухоли». Исследования рака. 44 (6): 2259–2265. PMID 6372991.
- ^ Maley, C.C .; Galipeau, P.C .; Finley, J.C .; Wongsurawat, V.J .; Ли, Х; Sanchez, C.A .; Paulson, T. G .; Blount, P. L .; Risques, R.A .; Рабинович, П. С .; Рид, Б. Дж. (2006). «Генетическое клональное разнообразие предсказывает прогрессирование аденокарциномы пищевода». Природа Генетика. 38 (4): 468–473. Дои:10,1038 / ng1768. PMID 16565718.
- ^ Калифано, Дж; Van Der Riet, P; Вестра, Вт; Nawroz, H; Clayman, G; Piantadosi, S; Corio, R; Ли, Д; Гринберг, B; Кох, Вт; Сидранский, Д (1996). «Модель генетической прогрессии рака головы и шеи: последствия для полевой канцеризации». Исследования рака. 56 (11): 2488–2492. PMID 8653682.
- ^ Sauter, G; Moch, H; Gasser, T. C .; Mihatsch, M. J .; Вальдман, Ф. М. (1995). «Неоднородность хромосомы 17 и числа копий гена erbB-2 при первичном и метастатическом раке мочевого пузыря». Цитометрия. 21 (1): 40–46. Дои:10.1002 / cyto.990210109. PMID 8529469.
- ^ Fujii, H; Йошида, М; Гонг, З. X .; Мацумото, Т; Хамано, Y; Фукунага, М; Hruban, R.H .; Габриельсон, Э; Шираи, Т. (2000). «Частая генетическая гетерогенность в клональной эволюции гинекологической карциносаркомы и ее влияние на фенотипическое разнообразие». Исследования рака. 60 (1): 114–120. PMID 10646862.
- ^ Horvai, A.E .; Devries, S; Рой, Р. О'Доннелл, Р. Дж .; Уолдман, Ф (2009). «Сходство в генетических изменениях между парными хорошо дифференцированными и дедифференцированными компонентами дедифференцированной липосаркомы». Современная патология. 22 (11): 1477–1488. Дои:10.1038 / modpathol.2009.119. PMID 19734852.
- ^ Pantou, D; Ризу, H; Царуха, H; Пули, А; Папанастасиу, К; Стамателлоу, М; Трангас, Т; Пандис, Н. Барди, Г. (2005). «Цитогенетические проявления неоднородности множественной миеломы». Гены, хромосомы и рак. 42 (1): 44–57. Дои:10.1002 / gcc.20114. PMID 15495197.
- ^ а б Шеклтон, М; Кинтана, E; Fearon, E. R .; Моррисон, С. Дж. (2009). «Неоднородность рака: раковые стволовые клетки против клональной эволюции». Клетка. 138 (5): 822–829. Дои:10.1016 / j.cell.2009.08.017. PMID 19737509.
- ^ Лапидот, Т; Сирар, C; Формор, Дж; Мердок, B; Хоанг, Т; Касерес-Кортес, Дж; Минден, М; Патерсон, Б; Калиджури, М. А .; Дик, Дж. Э. (1994). «Клетка, инициирующая острый миелоидный лейкоз человека после трансплантации мышам SCID». Природа. 367 (6464): 645–648. Bibcode:1994Натура.367..645L. Дои:10.1038 / 367645a0. PMID 7509044.
- ^ Wang, J. C .; Лапидот, Т; Cashman, J.D .; Doedens, M; Адди, L; Sutherland, D. R .; Nayar, R; Ларая, П; Минден, М; Китинг, А; Карнизы, A. C .; Eaves, C.J .; Дик, Дж. Э. (1998). «Высокий уровень приживления мышей NOD / SCID примитивными нормальными и лейкемическими гемопоэтическими клетками от пациентов с хроническим миелоидным лейкозом в хронической фазе». Кровь. 91 (7): 2406–2414. Дои:10.1182 / blood.V91.7.2406. PMID 9516140.
- ^ Сингх, С. К .; Хокинс, C; Clarke, I.D .; Squire, J. A .; Баяни, Дж; Hide, T; Хенкельман, Р. М .; Cusimano, M.D .; Диркс, П. Б. (2004). «Идентификация клеток-инициаторов опухоли головного мозга человека». Природа. 432 (7015): 396–401. Bibcode:2004Натура.432..396S. Дои:10.1038 / природа03128. PMID 15549107.
- ^ Аль-Хадж, М; Wicha, M. S .; Бенито-Эрнандес, А; Моррисон, С. Дж .; Кларк, М. Ф. (2003). «Проспективная идентификация онкогенных клеток рака груди». Труды Национальной академии наук. 100 (7): 3983–3988. Bibcode:2003ПНАС..100.3983А. Дои:10.1073 / пнас.0530291100. ЧВК 153034. PMID 12629218.
- ^ Maitland, N.J .; Коллинз, А. Т. (2008). «Стволовые клетки рака простаты: новая мишень для терапии». Журнал клинической онкологии. 26 (17): 2862–2870. Дои:10.1200 / JCO.2007.15.1472. PMID 18539965.
- ^ Meacham, C.E .; Моррисон, С. Дж. (2013). «Неоднородность опухоли и пластичность раковых клеток». Природа. 501 (7467): 328–337. Bibcode:2013Натура.501..328М. Дои:10.1038 / природа12624. ЧВК 4521623. PMID 24048065.
- ^ Новелл П. С. (1976). «Клональная эволюция популяций опухолевых клеток». Наука. 194 (4260): 23–28. Bibcode:1976Научный ... 194 ... 23N. Дои:10.1126 / science.959840. PMID 959840.
- ^ а б c Суантон, С. (2012). «Внутриопухолевая неоднородность: эволюция в пространстве и времени». Исследования рака. 72 (19): 4875–4882. Дои:10.1158 / 0008-5472.CAN-12-2217. ЧВК 3712191. PMID 23002210.
- ^ Мерло, Л. М. Ф .; Pepper, J. W .; Reid, B.J .; Мали, К. С. (2006). «Рак как эволюционно-экологический процесс». Обзоры природы Рак. 6 (12): 924–935. Дои:10.1038 / nrc2013. PMID 17109012.
- ^ а б c Герлингер, М; Роуэн, А. Дж .; Хорсвелл, S; Ларкин, Дж; Эндесфельдер, Д; Gronroos, E; Мартинес, П.; Мэтьюз, N; Стюарт, А; Tarpey, P; Варела, я; Филлимор, B; Бегум, S; McDonald, N.Q .; Батлер, А; Джонс, Д.; Рейн, К; Латимер, К; Santos, C. R .; Нохадани, М; Eklund, A.C .; Спенсер-Ден, Б. Кларк, G; Пикеринг, L; Штамп, G; Гор, М; Салласи, Z; Вниз, Дж; Futreal, P. A .; Суантон, С. (2012). «Внутриопухолевая гетерогенность и разветвленная эволюция, выявленные с помощью мультирегионального секвенирования». Медицинский журнал Новой Англии. 366 (10): 883–892. Дои:10.1056 / NEJMoa1113205. ЧВК 4878653. PMID 22397650.
- ^ а б c Марусык, А; Альмендро, V; Поляк, К (2012). «Внутриопухолевая гетерогенность: зеркало для рака?». Обзоры природы Рак. 12 (5): 323–334. Дои:10.1038 / nrc3261. PMID 22513401.
- ^ Burrell, R.A .; McGranahan, N; Бартек, Дж; Суантон, С. (2013). «Причины и последствия генетической неоднородности в развитии рака». Природа. 501 (7467): 338–345. Bibcode:2013Натура.501..338Б. Дои:10.1038 / природа12625. PMID 24048066.
- ^ Johnson, B.E .; Mazor, T; Hong, C; Барнс, М; Айхара, К; McLean, C.Y .; Fouse, S.D .; Ямамото, S; Ueda, H; Тацуно, К; Asthana, S; Jalbert, L.E .; Nelson, S.J .; Bollen, A. W .; Gustafson, W.C .; Charron, E; Weiss, W. A .; Смирнов, И. В .; Song, J. S .; Ольшен, А.Б .; Ча, S; Чжао, Y; Moore, R.A .; Mungall, A.J .; Джонс, С. Дж .; Херст, М; Marra, M. A .; Сайто, N; Aburatani, H; Мукаса, А (2014). «Мутационный анализ раскрывает происхождение и обусловленную терапией эволюцию рецидивирующей глиомы». Наука. 343 (6167): 189–193. Bibcode:2014Научный ... 343..189J. Дои:10.1126 / science.1239947. ЧВК 3998672. PMID 24336570.
- ^ а б Дин, Л; Ley, T. J .; Larson, D.E .; Miller, C.A .; Koboldt, D.C .; Welch, J. S .; Ritchey, J. K .; Янг, М. А .; Лампрехт, Т; McLellan, M.D .; McMichael, J. F .; Wallis, J. W .; Лу, С; Шен, Д; Harris, C.C .; Dooling, D. J .; Fulton, R. S .; Fulton, L.L .; Чен, К; Шмидт, H; Калицки-Вейзер, Дж; Магрини, В. Дж .; Повар, л; McGrath, S.D .; Vickery, T. L .; Wendl, M.C .; Хит, S; Watson, M. A .; Link, D. C .; Томассон, М. Х. (2012). «Клональная эволюция при рецидиве острого миелоидного лейкоза, выявленная с помощью полногеномного секвенирования». Природа. 481 (7382): 506–510. Bibcode:2012Натура.481..506D. Дои:10.1038 / природа10738. ЧВК 3267864. PMID 22237025.
- ^ Г. М. Эдельман (1989). «Топобиология». J. Scientific American. 260 (5): 76–88. Дои:10.1038 / scientificamerican0589-76. PMID 2717916.
- ^ В.Э. Орел; Н. Н. Дзятковская; М.И. Данко; СРЕДНИЙ. Романов; Ю.И. Мельник; Ю.А. Гриневич; С.В. Мартыненко (2004). «Пространственный и механоэмиссионный хаос механически деформированных опухолевых клеток». J. Журнал механики в медицине и биологии. 4 (1): 31–45. Дои:10.1142 / s0219519404000886.
- ^ В.Э. Орёл; СРЕДНИЙ. Романов; Н.Н. Дзятковская; Ю.И. Мельник (2002). «Устройство и алгоритм оценки механоэмиссонного хаоса в крови больных раком желудка». J. Медицинская инженерия и физика. 24 (5): 365–371. Дои:10.1016 / с1350-4533 (02) 00022-х. PMID 12052364.
- ^ Н. Храновская; В. Орел; Ю. Гриневич; О. Алексеенко; А. Романов; О. Скачкова; Н. Дзятковская; А. Бурлака; С.Лукин (2012). «Механическая гетерогенизация клеток карциномы легких Льюиса может улучшить антиметастатический эффект дендритных клеток». J. Журнал механики в медицине и биологии. 3 (12): 22. Дои:10.1142 / S0219519411004757.
- ^ Junttila, M. R .; Де Соваж, Ф. Дж. (2013). «Влияние неоднородности микросреды опухоли на терапевтический ответ». Природа. 501 (7467): 346–354. Bibcode:2013Натура.501..346J. Дои:10.1038 / природа12626. PMID 24048067.
- ^ Ауман, Джеймс Тодд; Маклеод, Ховард Л. (01.01.2010). «Клеточные линии колоректального рака не обладают молекулярной гетерогенностью клинических колоректальных опухолей». Клинический колоректальный рак. 9 (1): 40–47. Дои:10.3816 / ccc.2010.n.005. PMID 20100687.
- ^ Кэссиди, Джон В .; Калдас, Карлос; Бруна, Алехандра (2015-08-01). «Поддержание гетерогенности опухоли в ксенотрансплантатах опухолей, полученных от пациентов». Исследования рака. 75 (15): 2963–2968. Дои:10.1158 / 0008-5472.CAN-15-0727. ISSN 0008-5472. ЧВК 4539570. PMID 26180079.
- ^ Бай Х., Харманджи А.С., Эрсон-Омай АЗ., Ли Дж., Когкун С., Саймон М. и др. (Ноя 2015). «Комплексная геномная характеристика злокачественного прогрессирования глиомы с мутантным IDH1». Природа Генетика. 48 (1): 59–66. Дои:10,1038 / нг.3457. ЧВК 4829945. PMID 26618343.
- ^ Bedard, P. L .; Hansen, A. R .; Ratain, M. J .; Сиу, Л. Л. (2013). «Неоднородность опухоли в клинике». Природа. 501 (7467): 355–364. Bibcode:2013Натура.501..355Б. Дои:10.1038 / природа12627. ЧВК 5224525. PMID 24048068.
- ^ Доусон, С. Дж.; Tsui, D.W .; Муртаза, М; Биггс, Н; Rueda, O.M .; Чин, С. Ф .; Даннинг, М. Дж .; Гейл, D; Форшью, Т; Малер-Араужо, B; Раджан, S; Хамфрей, S; Бекк, Дж; Halsall, D; Уоллис, М. Бентли, Д; Caldas, C; Розенфельд, Н. (2013). «Анализ циркулирующей опухолевой ДНК для мониторинга метастатического рака груди». Медицинский журнал Новой Англии. 368 (13): 1199–1209. Дои:10.1056 / NEJMoa1213261. PMID 23484797.
- ^ Гатенби, Р. А .; Silva, A. S .; Gillies, R.J .; Фриден, Б. Р. (2009). «Адаптивная терапия». Исследования рака. 69 (11): 4894–4903. Дои:10.1158 / 0008-5472.CAN-08-3658. ЧВК 3728826. PMID 19487300.
- ^ Цибульскис, К; Лоуренс, М. С .; Carter, S.L .; Сиваченко А; Jaffe, D; Sougnez, C; Габриэль, S; Мейерсон, М; Lander, E. S .; Гетц, Г. (2013). «Чувствительное обнаружение соматических точечных мутаций в нечистых и гетерогенных образцах рака». Природа Биотехнологии. 31 (3): 213–219. Дои:10.1038 / nbt.2514. ЧВК 3833702. PMID 23396013.
- ^ Koboldt, D.C .; Чжан, Q; Larson, D.E .; Шен, Д; McLellan, M.D .; Линь, L; Miller, C.A .; Mardis, E. R .; Дин, Л; Уилсон, Р. К. (2012). "Вар Сканировать 2: Открытие соматической мутации и изменения числа копий при раке путем секвенирования экзома ". Геномные исследования. 22 (3): 568–576. Дои:10.1101 / гр.129684.111. ЧВК 3290792. PMID 22300766.
- ^ Saunders, C.T .; Wong, W. S .; Свами, S; Бекк, Дж; Мюррей, Л. Дж .; Читам, Р. К. (2012). «Стрелка: точный соматический вызов малых вариантов из секвенированных пар опухоль-нормальный образец». Биоинформатика. 28 (14): 1811–1817. Дои:10.1093 / биоинформатика / bts271. PMID 22581179.
- ^ Carter, S.L .; Цибульскис, К; Helman, E; Маккенна, А; Шэнь, H; Зак, Т; Laird, P.W .; Онофрио, Р. С.; Винклер, Вт; Weir, B.A .; Бероухим, Р; Пеллман, Д; Левин, Д. А .; Lander, E. S .; Мейерсон, М; Гетц, Г. (2012). «Абсолютная количественная оценка изменений соматической ДНК при раке человека» (PDF). Природа Биотехнологии. 30 (5): 413–421. Дои:10.1038 / nbt.2203. ЧВК 4383288. PMID 22544022.
- ^ Shah, S.P .; Рот, А; Гойя, Р. Oloumi, A; Ха, Г; Чжао, Y; Турашвили, Г; Дин, Дж; Це, К; Haffari, G; Башашати, А; Prentice, L.M .; Khattra, J; Берли, А; Яп, Д; Бернар, V; Макферсон, А; Шуманский, К; Крисан, А; Giuliany, R; Херави-Муссави, А; Рознер, Дж; Проложенный; Бироль, I; Varhol, R; Там, А; Дхалла, N; Цзэн, Т; Ма, К; Чан, С. К. (2012). «Спектр клональной и мутационной эволюции первичного тройного отрицательного рака груди». Природа. 486 (7403): 395–399. Bibcode:2012Натура.486..395S. Дои:10.1038 / природа10933. ЧВК 3863681. PMID 22495314.
- ^ Навин, Н; Кендалл, Дж; Troge, J; Andrews, P; Роджерс, L; МакИнду, Дж; Повар, К; Степанский, А; Леви, Д; Эспозито, Д; Muthuswamy, L; Красниц, А; McCombie, W. R .; Хикс, Дж; Виглер, М (2011). «Эволюция опухоли на основании секвенирования одной клетки». Природа. 472 (7341): 90–94. Bibcode:2011Натура 472 ... 90N. Дои:10.1038 / природа09807. ЧВК 4504184. PMID 21399628.
- ^ Ян, Катарина (2016). «Вывод дерева для данных с одной ячейкой». Геномная биология. 17: 86. Дои:10.1186 / s13059-016-0936-х. ЧВК 4858868. PMID 27149953.
- ^ Росс, Эдит (2016). «OncoNEM: вывод об эволюции опухоли на основании данных секвенирования отдельных клеток». Геномная биология. 17: 69. Дои:10.1186 / s13059-016-0929-9. ЧВК 4832472. PMID 27083415.
- ^ Зафар, Хамим (2017). «SiFit: вывод опухолевых деревьев из данных секвенирования отдельных клеток в рамках моделей с конечным числом участков». Геномная биология. 18 (1): 178. Дои:10.1186 / s13059-017-1311-2. ЧВК 5606061. PMID 28927434.
- ^ Зафар, Хамим (2019). «SiCloneFit: Байесовский вывод популяционной структуры, генотипа и филогении опухолевых клонов на основе данных секвенирования одноклеточного генома». Геномные исследования. 29 (11): 1847–1859. Дои:10.1101 / гр.243121.118. ЧВК 6836738. PMID 31628257.
- ^ Маликич, Салем; Рашиди Мехрабади, Фарид (2019). "PhISCS: комбинаторный подход к реконструкции неполной филогении опухоли посредством комплексного использования данных одноклеточного и массового секвенирования". Геномные исследования. 29 (11): 1860–1877. Дои:10.1101 / гр.234435.118. PMID 31628256.
- ^ Садеки Азер, Эрфан; Рашиди Мехрабади, Фарид (2020). «PhISCS-BnB: быстрый алгоритм ветвлений и границ для идеальной реконструкции филогении опухоли». Биоинформатика. 36 (Приложение_1): i169 – i176. Дои:10.1093 / биоинформатика / btaa464. PMID 32657358.
- ^ Койперс, Джек (2017). «Достижения в понимании эволюции опухолей посредством секвенирования отдельных клеток». Biochimica et Biophysica Acta (BBA) - Обзоры на рак. 1867 (2): 127–138. Дои:10.1016 / j.bbcan.2017.02.001. ЧВК 5813714. PMID 28193548.
- ^ Шварц, Рассел (13 февраля 2017 г.). «Эволюция филогенетики опухолей: принципы и практика». Природа Обзоры Генетика. 18 (4): 213–229. Дои:10.1038 / nrg.2016.170. ЧВК 5886015. PMID 28190876.
- ^ Фарахани, Хоссейн; де Соуза, Камила П. Э .; Биллингс, Рэвин; Яп, Дамиан; Шуманский, Карей; Ван, Адриан; Лай, Даниэль; Мес-Массон, Анн-Мари; Апарисио, Самуэль; П. Шах, Сохраб (18 октября 2017 г.). «Разработанные in vitro смеси клеточных линий и надежная оценка вычислительных методов для клонального разложения и продольной динамики при раке». Научные отчеты. 7 (1): 13467. Bibcode:2017НатСР ... 713467F. Дои:10.1038 / s41598-017-13338-8. ЧВК 5647443. PMID 29044127.
- ^ Заре, Хабил (2014). «Вывод клональной композиции из нескольких срезов рака груди». PLOS вычислительная биология. 10 (7): e1003703. Bibcode:2014PLSCB..10E3703Z. Дои:10.1371 / journal.pcbi.1003703. ЧВК 4091710. PMID 25010360.
- ^ Фишер, Андрей (2014). «Реконструкция с высоким разрешением клонального состава при раке». Отчеты по ячейкам. 7 (5): 1740–1752. Дои:10.1016 / j.celrep.2014.04.055. ЧВК 4062932. PMID 24882004.
- ^ Дешвар, Амит (2015). «Мониторинг прогрессирования хронического лимфоцитарного лейкоза путем секвенирования всего генома выявляет гетерогенные модели клональной эволюции». Геномная биология. 16: 35. Дои:10.1186 / s13059-015-0602-8. ЧВК 4359439. PMID 25786235.
- ^ Рот, Эндрю (2014). «PyClone: статистический вывод о структуре клональной популяции при раке». Методы природы. 11 (4): 396–398. Дои:10.1038 / nmeth.2883. ЧВК 4864026. PMID 24633410.
- ^ Марасс, Франческо (2015). «Филогенетическая модель скрытых признаков для клональной деконволюции». Летопись прикладной статистики. 10 (4): 2377–2404. arXiv:1604.01715. Дои:10.1214 / 16-AOAS986.
- ^ Мацуи, Юсуке (2016). "phyC: Кластеризация эволюционных деревьев рака". PLOS вычислительная биология. 13 (5): e1005509. Bibcode:2017PLSCB..13E5509M. bioRxiv 10.1101/069302. Дои:10.1371 / journal.pcbi.1005509. ЧВК 5432190. PMID 28459850.
- ^ Цзян, Ючао; Цю, Ю; Минн, Энди Дж .; Чжан, Нэнси Р. (29 августа 2016 г.). «Оценка внутриопухолевой гетерогенности и отслеживание продольной и пространственной истории эволюции клонов с помощью секвенирования следующего поколения». Труды Национальной академии наук. 113 (37): E5528–37. Дои:10.1073 / pnas.1522203113. ЧВК 5027458. PMID 27573852.
- ^ Салехи, Сохраб (2017). «ddClone: совместный статистический вывод клональных популяций на основе данных секвенирования единичных клеток и массивных опухолей». Геномная биология. 18 (1): 44. Дои:10.1186 / s13059-017-1169-3. ЧВК 5333399. PMID 28249593.
- ^ Сатас, Грайте (2017). «Вывод филогении опухоли с использованием выборки по важности с ограничениями по дереву». Биоинформатика. 33 (14): i152 – i160. Дои:10.1093 / биоинформатика / btx270. ЧВК 5870673. PMID 28882002.
- ^ Гэн, Ю (2017). «Выявление моделей гетерогенности аллельного дисбаланса на вариантах зародышевой линии для вывода клональной архитектуры». Международная конференция по интеллектуальным вычислениям. Конспект лекций по информатике. 10362: 286–297. Дои:10.1007/978-3-319-63312-1_26. ISBN 978-3-319-63311-4.
- ^ Рамазотти, Даниэле; Граудензи, Алекс; Сано, Лука Де; Антониотти, Марко; Караваджна, Джулио (4 сентября 2017 г.). «Изучение мутационных графиков индивидуальной эволюции опухоли из данных секвенирования с несколькими образцами». bioRxiv 10.1101/132183.
- ^ Роман, Теодор; Се, Лу; Шварц, Рассел; Рафаэль, Бенджамин Дж. (23 октября 2017 г.). «Автоматическая деконволюция структурированных смесей из данных генома гетерогенной опухоли». PLOS вычислительная биология. 13 (10): e1005815. arXiv:1604.02487. Bibcode:2017PLSCB..13E5815R. Дои:10.1371 / journal.pcbi.1005815. ЧВК 5695636. PMID 29059177.
- ^ Маликич, Салем (2017). «Интегративный вывод субклональной эволюции опухоли из данных одноклеточного и массового секвенирования». bioRxiv 10.1101/234914.
- ^ Эспер, Лейла; Махмуди, Ахмад; Рафаэль, Бенджамин Дж. (29 июля 2013 г.). «THetA: вывод внутриопухолевой гетерогенности на основе данных высокопроизводительного секвенирования ДНК». Геномная биология. 14 (7): R80. Дои:10.1186 / gb-2013-14-7-r80. ISSN 1474-760X. ЧВК 4054893. PMID 23895164.
- ^ Цзэн, By (2018). «Идентификация субклонов опухоли на основе филогенеза с использованием байесовской модели распределения признаков». arXiv:1803.06393 [stat.AP ].
- ^ Цунь, Юпэн; Ян, Цун-По; Ахтер, Виктор; Ланг, Ульрих; Пайфер, Мартин (24 мая 2018 г.). «Анализ числа копий и вывод о субклональных популяциях в геномах рака с использованием Sclust». Протоколы природы. 13 (6): 1488–1501. Дои:10.1038 / nprot.2018.033. ISSN 1754-2189. PMID 29844525.
- ^ Ван, Сяодун; Огундиджо, Ойетунджи Э. (01.12.2019). «SeqClone: последовательный вывод субклонов опухоли на основе Монте-Карло». BMC Bioinformatics. 20 (1): 6. Дои:10.1186 / s12859-018-2562-у. ISSN 1471-2105. ЧВК 6320595. PMID 30611189.
- ^ Рафаэль, Бенджамин Дж .; Satas, Gryte; Майерс, Мэтью А. (22 января 2019 г.). «Вывод эволюции опухоли из продольных образцов». bioRxiv: 526814. Дои:10.1101/526814.
- ^ Туси, Хосейн; Моейни, Али; Хаджирасулиха, Иман (6 июня 2019 г.). «BAMSE: выбор байесовской модели для вывода о филогении опухоли среди множества образцов». BMC Bioinformatics. 20 (11): 282. Дои:10.1186 / s12859-019-2824-3. ISSN 1471-2105. ЧВК 6551234. PMID 31167637.
- ^ Рикеттс, Камир; Сейдман, Даниэль; Попик, Виктория; Хормоздиари, Ферейдун; Бацоглоу, Серафим; Гаджирасулиха, Иман (4 октября 2019 г.). "Meltos: Реконструкция филогении множественных образцов опухолей для структурных вариантов". Биоинформатика. 36 (4): 1082–1090. Дои:10.1093 / биоинформатика / btz737. PMID 31584621.
- ^ Сандерманн, Линда. «Реконструкция истории эволюции опухоли и деревьев клонов в полиномиальное время с помощью SubMARine» (PDF). bioRxiv. Получено 22 июн 2020.
- ^ Чжоу, Тяньцзянь. «RNDCLONE: РЕКОНСТРУКЦИЯ СУБКЛОНА ОПУХОЛИ НА ОСНОВЕ ИНТЕГРАЦИИ ДАННЫХ О ПОСЛЕДОВАТЕЛЬНОСТИ ДНК И РНК» (PDF). Получено 23 августа 2020.
