Стереохимия алканов - Alkane stereochemistry
Стереохимия алканов касается стереохимия из алканы.Алкане конформеры являются одним из объектов стереохимии алканов.
Конформация алкана
Конформеры алканов возникают в результате вращения вокруг sp3 гибридизированный углерод углерода сигма-облигации. Наименьший алкан с такой химической связью, этан, существует как бесконечное число конформаций относительно вращения вокруг связи C – C. Два из них признаны минимумом энергии (шахматное строение ) и максимум энергии (затмение ) формы. Существование специфических конформаций связано с затрудненным вращением вокруг сигма-связей, хотя сверхсопряжение предлагается конкурирующей теорией.
Важность минимума энергии и максимума энергии видна при распространении этих концепций на более сложные молекулы, для которых стабильные конформации могут быть предсказаны как формы с минимальной энергией. Определение стабильных конформаций также сыграло большую роль в установлении концепции асимметричная индукция и способность предсказывать стереохимия реакций, контролируемых стерическими эффектами.
На примере шахматной этан в Проекция Ньюмана, атом водорода на одном атоме углерода имеет угол 60 ° крутильный угол или угол кручения [1] относительно ближайшего атома водорода на другом углероде, так что стерическое препятствие сводится к минимуму. Ступенчатое строение стабильнее на 12,5. кДж /моль чем затмил конформация, которая является максимумом энергии для этана. В затменной конструкции угол скручивания минимален.



В бутан, две расположенные в шахматном порядке конформации больше не эквивалентны и представляют собой два различных конформера: антиконформация (крайний слева внизу) и грубая форма (крайний справа внизу).

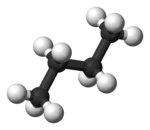

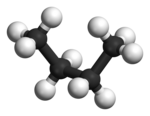
Обе конформации свободны от деформации кручения, но в гош-конформации две метил группы находятся ближе друг к другу, чем сумма их ван-дер-ваальсовых радиусов. Взаимодействие двух метильных групп отталкивающее (штамм Ван-дер-Ваальса ), и возникает энергетический барьер.
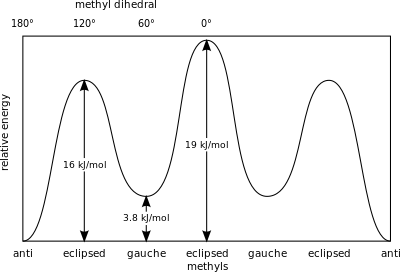
Мера потенциальная энергия хранящиеся в конформерах бутана с большими стерическими препятствиями, чем основное состояние «анти» конформеров, определяется следующими значениями:[2]
- Гош, конформер - 3,8 кДж / моль
- Затмение H и CH3 - 16 кДж / моль
- Затменный CH3 и CH3 - 19 кДж / моль.
Затменный метильные группы вызывают большее стерическое напряжение из-за их большей электронная плотность по сравнению с одиноким водород атомы.
Учебное объяснение существования максимума энергии для затменной конформации в этане таково: стерическое препятствие, но с C-C длина облигации 154 часа и Радиус Ван-дер-Ваальса для водорода 120 мкм атомы водорода в этане никогда не мешают друг другу. Вопрос о том, является ли стерическое препятствие причиной затменного максимума энергии, является предметом дискуссий по сей день. Одна альтернатива объяснению стерических препятствий основана на сверхсопряжение как анализируется в рамках Natural Bond Orbital.[3][4][5] В шахматном порядке один C-H сигма связывающая орбиталь жертвует электронную плотность разрыхляющая орбиталь другой связи C-H. Энергетическая стабилизация этого эффекта максимальна, когда две орбитали имеют максимальное перекрытие, происходящее в шахматной конформации. В затменной конформации нет перекрытия, что приводит к нежелательному максимуму энергии. С другой стороны, анализ в рамках количественного теория молекулярных орбиталей показывает, что 2-орбитально-4-электронное (стерическое) отталкивание преобладает над гиперконъюгацией.[6] А теория валентной связи исследование также подчеркивает важность стерических эффектов.[7]
Номенклатура
Названия алканов в соответствии со стандартами, перечисленными в Золотая книга ИЮПАК делается в соответствии с Система Клайна – Прелога для указания углов (называемых крутильными или двугранные углы ) между заместителями вокруг одинарной связи:[8]
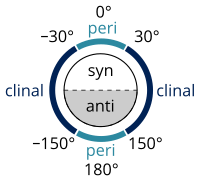
- угол кручения от 0 ° до ± 90 ° называется син (s)
- угол кручения от ± 90 ° до 180 ° называется анти (а)
- угол кручения от 30 ° до 150 ° или от -30 ° до -150 ° называется клинальный (c)
- угол кручения от 0 ° до ± 30 ° или от ± 150 ° до 180 ° называется перипланарный (п)
- угол кручения от 0 ° до ± 30 ° называется синперипланарный (sp), также называемый син- или цис- конформация
- угол кручения от 30 ° до 90 ° и от –30 ° до –90 ° называется синклинальный (sc), также называемый бестактный или перекос[9]
- угол кручения от 90 ° до 150 ° или от –90 ° до –150 ° называется антиклинальный (ac)
- угол кручения от ± 150 ° до 180 ° называется антиперипланарный (ap), также называемый анти- или транс- конформация
Деформация кручения возникает из-за сопротивления скручиванию связи.
Особые случаи
В п-пентан, терминал метил группы получают дополнительные пентановая интерференция.
Замена водорода на фтор в политетрафторэтилен изменяет стереохимию с зигзагообразной геометрии на стереохимию спираль за счет электростатического отталкивания атомов фтора в 1,3-позициях. Доказательства спиральной структуры в кристаллическом состоянии получены из Рентгеновская кристаллография и из ЯМР-спектроскопия и круговой дихроизм в растворе.[10]
Смотрите также
- В циклических алканах существует больше конформаций алканов; увидеть циклогексановые конформации.
- Подробнее о влиянии грубых взаимодействий; увидеть Эффект Гоша.
использованная литература
- ^ Золотая книга Ссылка на сайт
- ^ Органическая химия 6e, МакМюррей, Дж. Э., Брукс Коул (2003)
- ^ Гиперконъюгация нестерического отталкивания приводит к шахматной структуре этана. Пофристик В. и Гудман Л. Природа 411, 565–568 (2001)Абстрактные
- ^ Химия: новый поворот в молекулярной форме Франк Вайнхольд Природа 411, 539–541 (31 мая 2001)
- ^ Опровержение случая Бикельгаупта-Бэрендса стерического отталкивания, вызывающего шахматную конформацию этана. Weinhold, F. Angew. Chem. Int. Эд. 42, 4188–4194 (2003)
- ^ Случай стерического отталкивания, вызывающего ступенчатую конформацию этана. Бикельгаупт, Ф. И Baerends, E.J. Энгью. Chem. Int. Эд. 42, 4183–4188 (2003)
- ^ Величина гиперконъюгации в этане: взгляд из ab initio теории валентной связи. Мо, Ю. и другие. Энгью. Chem. Int. Эд. 43, 1986–1990 (2004)
- ^ ИЮПАК, Сборник химической терминологии, 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) "угол кручения ". Дои:10.1351 / goldbook.T06406
- ^ ИЮПАК, Сборник химической терминологии, 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) "бестактный ". Дои:10.1351 / goldbook.G02593
- ^ Конформационный анализ хиральных спиральных перфторалкильных цепей с помощью VCD Кендзи Монд, Нобуаки Миура, Май Хашимото, Тору Танигучи и Тамоцу Инабе Варенье. Chem. Soc.; 2006; 128 (18) pp 6000–6001; графическая абстракция
