Реакция Барджеллини - Википедия - Bargellini reaction
| Реакция Барджеллини | |
|---|---|
| Названный в честь | Гвидо Барджеллини |
| Тип реакции | Реакция сцепления |
В Реакция Барджеллини это химическая реакция открыт в 1906 году итальянцем химик Гвидо Барджеллини.[1] Исходная реакция представляла собой смесь реагентов. фенол, хлороформ, и ацетон в присутствии едкий натр решение.[2] До исследования Барджеллини продукт относился к этому многокомпонентная реакция (MCR) в то время описывалось как производное фенола в текстах по химии. Однако Барджеллини продемонстрировал, что карбоновая кислота производная была действительно правильной структурой.

Позже химики-органики использовали эту реакцию как общий метод органического синтеза для получения сильно затрудненных или объемных морфолинонов или пиперазинонов из кетоны (особенно ацетон ) и либо β-аминоспирты, либо диамины.

История
Гвидо Барджеллини был учеником Герман Эмиль Луи Фишер, немецкий химик и лауреат Нобелевской премии, известный благодаря одноименному Этерификация Фишера реакция. Барджеллини провел свои постдокторские лабораторные исследования в лаборатории Фишера. Большую часть своей карьеры он проработал химиком в Римский университет.
Его интерес к кумарины, недавно изолированное соединение, побудило Барджеллини экспериментировать с многокомпонентными реакциями (MCR) между фенолы, хлороформ, и ацетон в растворе едкий натр. Он обнаружил, что структура, данная соединению, дает карбоновая кислота вместо фенола, как считалось ранее. В 1894 году немецкий химик Линк опубликовал реакцию в Chemisches Zentralblatt и запатентовал это. Однако он написал, что продукт был либо кетон или фенол, в частности, он утверждал, что это «гидрпсифенилгидроксиизопропилкетон» или «гидроксиизобутирилфенол».[3] Когда Барджеллини провел тот же эксперимент и начал тестирование продукта, химические свойства не могли быть связаны с кетоном или фенолом. Вместо этого он был уверен, что это карбоновая кислота, а именно «α-феноксиизомасляная кислота». Сам Линк экспериментировал с реакциями в 1900 году, которые доказали, что его первоначальное утверждение было ошибочным, но оно так и не было изменено. Поскольку Барджеллини правильно определил продукт, его структуру и свойства, то опубликовал свои результаты в Gazzetta Chimica Italiana, реакция была названа его именем.
Однако важность реакции в органическом синтезе, а позже и в фармацевтической промышленности сделала ее важной исторически. Поскольку реакцию относительно легко провести - реагенты легко доступны, - спустя десятилетия были названы многие другие почти идентичные реакции. Это открытие проложило путь к новой реакции превращения, установленным в настоящее время реакциям типа Барджеллини, которые имели большое значение, особенно в фармацевтическая индустрия. Это также проложило путь для более поздних реакций на имя, таких как Реакция Йочика-Рива и Реакция Кори – Линка. Реакции Йочика – Рива и Кори – Линка почти всегда фигурируют вместе с реакцией Барджеллини в MCR. Сама реакция была модифицирована несколько раз, чтобы повысить эффективность или получить модифицированный продукт.
Адаптивность реакции - один из ее важнейших аспектов. Ни одно десятилетие не прошло без важного дополнения или поворота реакции. По словам автора, «первой фазой реакции, вероятно, является образование ацетонхлороформ - (который действительно может быть использован вместо хлороформа), на который затем действует гидроксид натрия в присутствии ацетона, давая α-гидроксиизомасляная кислота, который вместе с фенолом дает α-феноксиизомасляную кислоту. Хлороформ также можно заменить на бромоформ, бромальный, хлорал, или же четыреххлористый углерод или же тетрабромид. "В большинстве учебников реакция описывается как способ вызвать морфолиноны или же пиперазиноны, но его использование простирается гораздо дальше.
Сто лет спустя сама реакция Барджеллини была использована для конденсация из кумарины, иронический поворот в истории реакции, поскольку это было основное соединение интереса Барджеллини, и его собственная названная реакция произвела его.[4]
Реакции и механизмы реакции
Оригинальная реакция Барджеллини (1906 г.):
Механизм реакции оригинальной реакции Барджеллини (1906 г.):
Современная реакция Барджеллини используется для синтеза затрудненных морфолинонов или пиперазинонов из кетонов (в первую очередь ацетона) и 2-амино-2-метилпропан-1-ола (β-аминоспиртов) или 1,2-диаминопропанов (диаминов). Используемый растворитель дихлорметан (DCM), также известный как метиленхлорид с хлоридом бензилтриэтиламмония катализатор. Растворитель и катализатор часто меняют при использовании разных реагентов. Диамины имеют тенденцию давать более высокий выход продукта, чем β-аминоспирты, как показано в двух возможных сценариях ниже:
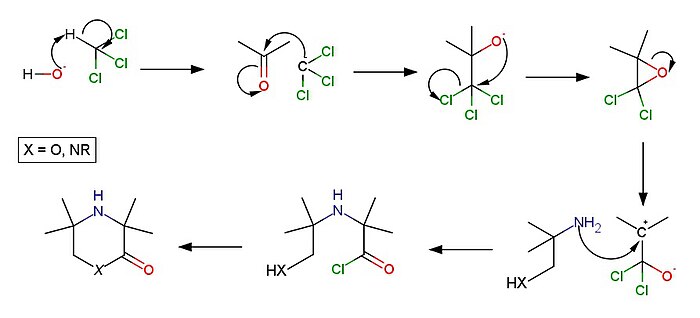
Механизм реакции Барджеллини:
Механизм реакции протекает, когда стерически доступный кетон, обычно ацетон, добавляют к раствору хлороформа (трихлорметана) в сильных щелочных условиях, создавая анион трихлорметида путем депротонирование. Это образует соответствующий трихлорметилкарбинол или -алкоксид, аналогично Реакция Гриньяра.[5]
Этот тригалогенированный продукт может быть добавлен посредством внутримолекулярной этерификации, вызванной основанием. самоцвет-дихлорэпоксид. Амин может атаковать оксиран за счет образования третичного карбокатион при нуклеофильном замещении SN1 согласовано отщепление одного атома хлора. Нуклеофильный промежуточный продукт является высокореактивным и региоселективным по α-углероду, что приводит к образованию α-замещенного хлорида карбоновой кислоты.
Заключительный этап происходит путем нуклеофильного ацильного замещения и сольволиз, где амино или гидроксильная группа атакует хлорангидрид, образуя соответствующий гетероцикл.[6] Конечный продукт представляет собой производное карбоновой кислоты (в первую очередь лактоны и амиды).
Рекомендации
- ^ Папео, Джанлука; Пулики, Маурицио (4 сентября 2013 г.). «Вклад итальянских химиков в названные реакции в органическом синтезе: историческая перспектива». Молекулы. 18 (9): 10870–10900. Дои:10.3390 / молекулы180910870. ЧВК 6270118. PMID 24008246.
- ^ Барджеллини, Гвидо (4 июня 1906 г.). "Azione del cloroformio e idrato sodico sui fenoli в растворе без ацетона" [Действие хлороформа и гидроксида натрия на фенолы в растворе ацетона]. Gazzetta Chimica Italiana.
- ^ "Органическая химия". Журнал химического общества, тезисы. 90: A617 – A720. Январь 1906 г. Дои:10.1039 / ca9069000617.
- ^ Sen, Prabir K .; Бисвас, Бидют; Венкатешваран, Раманатхапурам В. (2005-12-12). «Конденсация Барджеллини кумаринов. Оперативный синтез о-карбоксивинилфеноксиизомасляной кислоты». Буквы Тетраэдра. 46 (50): 8741–8743. Дои:10.1016 / j.tetlet.2005.10.045.
- ^ Ли, Джи Джек (2014). Название реакции - Спрингер. Дои:10.1007/978-3-319-03979-4. ISBN 978-3-319-03978-7. S2CID 93616494.
- ^ Тимоти С. Сноуден: Недавние применения промежуточных продуктов гем-дихлорэпоксида в синтезе. В: АРКИВОК. 2, 2012, С. 24–40