ДНК-полимераза вируса гепатита B - Hepatitis B virus DNA polymerase
| Белок P (ДНК-полимераза / РНКаза H) | |||||||
|---|---|---|---|---|---|---|---|
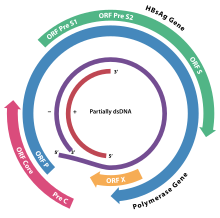 Геномная организация HBV; гены перекрываются. ORF P, выделенная синим цветом, кодирует ДНК-полимеразу вируса гепатита B. | |||||||
| Идентификаторы | |||||||
| Организм | |||||||
| Символ | п | ||||||
| UniProt | P03156 | ||||||
| |||||||
| Белок P | |
|---|---|
| Идентификаторы | |
| Символ | ? |
| ИнтерПро | IPR037531 |
ДНК-полимераза вируса гепатита B это гепатит Б вирусный белок.[1][2] Это ДНК-полимераза которые могут использовать шаблоны ДНК или РНК и рибонуклеаза H который разрезает РНК в дуплексе. Обе функции предоставляются обратная транскриптаза (RT) домен.
Структура
В гепаднавирус P-белок состоит из трех доменов: N-концевого домена (ИнтерПро: IPR000201 ), покрывающий терминал и спейсер, домен RT, связанный с каждым другим доменом RT, и C-концевой домен (ИнтерПро: IPR001462 ) регулирующие активность РНКазы Н.
Функция
В HBV пгРНК транслируется в вирусную полимеразу и коровые белки, а затем инкапсидируется и обратно транскрибируется с образованием новой молекулы ркДНК. На этом этапе полимераза HBV выполняет некоторые задачи и функции. Полимераза HBV представляет собой многофункциональный фермент с активностями РНК-зависимой и ДНК-зависимой полимеразы и РНКазы H.[3] Кроме того, полимеразы гепаднавирусов содержат домен концевого белка (ТР), который содержит остаток тирозина, который служит праймером для синтеза (-) цепи ДНК.[3]
На этапах обратной транскрипции наличие димеров корового белка HBV необходимо для упаковки комплекса пгРНК / полимераза. Затем, после того как вирусная полимераза связывается с сигналом упаковки (Hɛ), обнаруженным на 5'-конце пгРНК, они встраиваются в вирусный капсид.[3][4] Внутри капсида пгРНК подвергается обратной транскрипции, которая инициируется праймированием белка на тирозиновом остатке полимеразы HBV. Таким образом образуется (-) цепь ДНК.[4] В то же время деградация матрицы РНК происходит под действием РНКазы Н активности полимеразы. Короткая РНК примерно 15-18 нуклеотиды на 5'-конце пгРНК (включая 5'-последовательность DR1) не разлагается и используется в качестве праймера для синтеза (+) цепи ДНК.[3]
Полученная RC-ДНК является частично двухцепочечной. (-) цепь ДНК длиннее, чем длина генома, с ковалентно связанной полимеразой и избыточным лоскутом на 5'-конце. Однако синтез (+) цепи ДНК не завершается полимеразой, и существует разрыв до 3'-конца (+) цепи ДНК.[4]
Рекомендации
- ^ Оно-Нита С.К., Като Н., Ширатори Й., Масаки Т., Лан К.Х., Каррильо Ф.Дж., Омата М. (март 1999 г.). «Мотив YMDD в ДНК-полимеразе вируса гепатита В влияет на репликацию и устойчивость к ламивудину: исследование с помощью трансфекции полноразмерной вирусной ДНК in vitro». Гепатология. 29 (3): 939–45. Дои:10.1002 / hep.510290340. PMID 10051501.
- ^ Шоу Т., Мок СС, Локарнини С.А. (ноябрь 1996 г.). «Ингибирование ДНК-полимеразы вируса гепатита В энантиомерами пенцикловиртрифосфата и метаболическая основа для селективного ингибирования репликации HBV пенцикловиром». Гепатология. 24 (5): 996–1002. Дои:10.1002 / hep.510240504. PMID 8903366.
- ^ а б c d Менендес-Ариас Л., Альварес М., Пачеко Б. (октябрь 2014 г.). «Нуклеозидные / нуклеотидные аналоги ингибиторов полимеразы вируса гепатита В: механизм действия и резистентность». Текущее мнение в вирусологии. 8: 1–9. Дои:10.1016 / j.coviro.2014.04.005. PMID 24814823.
- ^ а б c Ян Х.С., Као Дж. Х. (сентябрь 2014 г.). «Персистенция ковалентно замкнутой кольцевой ДНК вируса гепатита В в гепатоцитах: молекулярные механизмы и клиническое значение». Новые микробы и инфекции. 3 (9): e64. Дои:10.1038 / emi.2014.64. ЧВК 4185362. PMID 26038757.
| Этот вирус -связанная статья является заглушка. Вы можете помочь Википедии расширяя это. |
