Теория Маркуса - Marcus theory
Теория Маркуса теория, первоначально разработанная Рудольф А. Маркус, начиная с 1956 г., чтобы объяснить тарифы из перенос электронов реакции - скорость, с которой электрон может двигаться или прыгать с одного химические вещества (называется донор электронов ) другому (называемому акцептор электронов ).[1] Первоначально он был сформулирован для решения перенос электронов во внешнюю сферу реакции, в которых два химических вещества изменяются только в своих обвинять с прыжком электрона (например, окисление иона, подобного Fe2+/ Fe3+), но не претерпевают больших структурных изменений. Он был расширен за счет включения перенос электронов внутри сферы вклады, в которых изменение расстояний или геометрии в сольватация или же координационные оболочки двух химических частиц (расстояния Fe-O в Fe (H2O)2+ и Fe (H2O)3+ разные).[2][3]
Для реакций переноса электрона без образования или разрыва связей Теория Маркуса занимает место Айринга теория переходного состояния[4][5] который был получен для реакций со структурными изменениями. Обе теории приводят к уравнениям ставок одного и того же экспоненциальный форма. Однако, в то время как в теории Эйринга партнеры реакции становятся прочно связанными в ходе реакции с образованием структурно определенного активированного комплекса, в теории Маркуса они слабо связаны и сохраняют свою индивидуальность. Это термически индуцированная реорганизация окружающей среды, растворителя (внешняя сфера) и оболочки растворителя или лигандов (внутренняя сфера), которые создают геометрически благоприятную ситуацию. прежний до и не зависит от скачка электрона.
Оригинальная классическая теория Маркуса для реакций переноса электрона во внешней сфере демонстрирует важность растворителя и открывает путь к расчету Свободная энергия Гиббса активации, используя поляризация свойства растворителя, размер реагентов, расстояние переноса и свободная энергия Гиббса окислительно-восстановительной реакции. Самым поразительным результатом теории Маркуса была «перевернутая область»: в то время как скорость реакции обычно увеличивается с увеличением эксергоничность реакции перенос электрона должен, согласно теории Маркуса, становиться медленнее в очень отрицательных домен. Ученые искали перевернутую область в поисках доказательства более медленной скорости переноса электронов в течение 30 лет, пока это не было однозначно экспериментально подтверждено в 1984 году.[6]
Р. А. Маркус получил Нобелевская премия по химии в 1992 г. за эту теорию. Теория Маркуса используется для описания ряда важных процессов в химии и биологии, в том числе фотосинтез, коррозия, некоторые виды хемилюминесценция, разделение зарядов в некоторых типах солнечные батареи и больше. Помимо приложений внутренней и внешней сфер, теория Маркуса была расширена для рассмотрения гетерогенных перенос электронов.
Одноэлектронная окислительно-восстановительная реакция
Химические реакции могут приводить к замене группы в молекуле или лиганда в комплексе, к удалению группы молекулы или лиганда или к перегруппировке молекулы или комплекса. Однако реакция переноса электрона может также вызвать простой обмен зарядами между реагентами, и эти окислительно-восстановительные реакции без образования или разрыва связи кажутся довольно простыми в неорганической химии для ионов и комплексов. Эти реакции часто проявляются в изменении цвета, например для ионов или комплексов ионов переходных металлов, но и органические молекулы могут изменить свой цвет, принимая или отдавая электрон (например, гербицид Паракват (N,N-диметил-4,4'-бипиридиния дихлорид), который становится синим при приеме электрона, отсюда альтернативное название метилвиологена). Для этого типа реакций с переносом электрона Р.А. Маркус разработал свою теорию. Здесь представлены аргументы и результаты. За математическое развитие и детализацию оригинальных статей.[7][8] следует проконсультироваться.
В окислительно-восстановительной реакции один партнер действует как донор электронов D, а другой - как акцептор A. Для того, чтобы реакция имела место, D и A должны диффундировать вместе. Они образуют комплекс-предшественник, обычно кинетический, нестабильный, сольватированный комплекс встречи, который путем переноса электрона преобразуется в комплекс-последователь, и, наконец, он разделяется путем диффузии. Для переноса одного электрона реакция
(D и A могут уже нести заряды). Здесь k12, k21 и k30 - постоянные диффузии, k23 и k32 константы скорости активированных реакций. Полная реакция может контролироваться диффузией (стадия переноса электрона происходит быстрее, чем диффузия, каждое столкновение приводит к реакции) или управляемой активацией (достигается «равновесие ассоциации», стадия переноса электрона является медленной, разделение последующего комплекса быстрый).
Перенос электрона во внешнюю сферу
Окислительно-восстановительные реакции предпочтительно проводят в полярных растворителях. Тогда донор и акцептор имеют оболочку из растворителя, а комплексы-предшественники и последователи также сольватированы. Ближайшие молекулы оболочки растворителя или лиганды в комплексах тесно связаны и составляют «внутреннюю сферу». Реакции, в которых они участвуют, называются окислительно-восстановительными реакциями внутренней сферы. Молекулы свободного растворителя составляют «внешнюю сферу». Окислительно-восстановительные реакции внешней сферы не изменяют внутреннюю сферу, связи не образуются и не разрушаются.
Это был Р.А. Маркус, который осознал роль растворителя, когда он работал над природой и величиной свободной энергии Гиббса активации окислительно-восстановительных реакций, точнее: реакций одноэлектронного переноса типа внешней сферы. Он опубликовал две фундаментальные статьи.[7][8] Идеи этих двух работ часто относятся к теории Маркуса, хотя более поздние работы Маркуса выходят далеко за их рамки.[1]
Проблема
Во внешнесферных окислительно-восстановительных реакциях связи не образуются и не разрываются; имеет место только перенос электрона (ПТ). Довольно простой пример - Fe2+/ Fe3+ окислительно-восстановительная реакция, реакция самообмена, которая, как известно, всегда происходит в водном растворе, содержащем как FeSO,4 и Fe2(ТАК4)3 (конечно, с равными и измеримыми скоростями в обоих направлениях и со свободной энергией реакции Гиббса ).
Из температурной зависимости скорости реакции энергия активации определяется, и эта энергия активации интерпретируется как энергия переходное состояние на диаграмме реакции. Последняя представлена, согласно Аррениусу и Эйрингу, в виде энергетической диаграммы с координатой реакции по оси абсцисс. Координата реакции описывает путь минимальной энергии от реагентов к продуктам, а точки этой координаты представляют собой комбинации расстояний и углов между реагентами и внутри них в процессе образования и / или разрыва связей. Максимум энергетической диаграммы, переходное состояние, характеризуется определенной конфигурацией атомов. Более того, в TST Айринга[4][5] довольно специфическое изменение ядерные координаты отвечает за пересечение точки максимума, следовательно, вибрация в этом направлении рассматривается как перенос.
Для окислительно-восстановительных реакций во внешней сфере не может быть такого пути реакции, но тем не менее наблюдается энергия активации. Уравнение скорости для реакций, контролируемых активацией, имеет ту же экспоненциальную форму, что и уравнение Эйринга:
- свободная энергия Гиббса образования переходного состояния, экспоненциальный член представляет вероятность его образования, A содержит вероятность перехода от комплекса-предшественника к комплексу-преемнику.
Модель Маркуса
Следствием переноса электрона является перегруппировка зарядов, и это сильно влияет на среду растворителя. Для диполярного растворителя молекулы перестраиваются в направлении поля зарядов (это называется ориентационной поляризацией), а также атомы и электроны в молекулах растворителя немного смещены (атомная и электронная поляризация соответственно). Это это поляризация растворителя которая определяет свободную энергию активации и, следовательно, скорость реакции.
Реакции замещения, элиминирования и изомеризации отличаются от окислительно-восстановительной реакции внешней сферы не только структурными изменениями, описанными выше, но и тем, что движения ядер и смещение зарядов (перенос заряда, CT) на пути реакций протекают непрерывно и согласованно: конфигурации ядер и распределение заряда всегда находятся «в равновесии». Это иллюстрируется SN2 замещение омыления алкилгалогенида, когда обратная сторона атакует ОН− ion выталкивает галогенид-ион, и здесь необходимо визуализировать переходное состояние с пятикоординированным атомом углерода. Система реагентов становится настолько тесно связанной во время реакции, что они образуют активированный комплекс как единое целое. Растворитель здесь оказывает незначительное влияние.
Напротив, во внешнесферных окислительно-восстановительных реакциях смещение ядер в реагентах невелико, здесь растворитель играет доминирующую роль. Донорно-акцепторная связь слабая, оба сохраняют свою идентичность во время реакции. Следовательно, электрон, будучи элементарной частицей, может «прыгать» только целиком (перенос электронов, ET). Если электрон прыгает, перенос происходит намного быстрее, чем движение больших молекул растворителя, в результате чего ядерные положения партнеров реакции и молекул растворителя одинаковы до и после скачка электрона (Принцип Франка – Кондона ).[9] Скачок электрона регулируется квантово-механическими правилами, он возможен только в том случае, если также энергия системы ET не изменяется «во время» прыжка.
Расположение молекул растворителя зависит от распределения заряда реагентов. Если конфигурация растворителя должна быть одинаковой до и после прыжка и энергия может не измениться, тогда растворитель не может находиться в сольватационном состоянии предшественника или в состоянии сольватации комплекса-преемника, поскольку они различны, он должен находиться где-то посередине. Для реакции самообмена по причинам симметрии, расположение молекул растворителя точно посередине молекул предшественника и комплекса-преемника будет соответствовать условиям. Это означает, что расположение растворителя с половиной электрона на доноре и акцепторе будет правильной средой для прыжка. Кроме того, в этом состоянии энергия предшественника и преемника в их среде растворителя будет одинаковой.
Однако электрон как элементарная частица не может быть разделен, он находится либо на доноре, либо на акцепторе и соответственно улаживает молекулы растворителя в равновесии. «Переходное состояние», с другой стороны, требует конфигурации растворителя, которая возникла бы в результате переноса половины электрона, что невозможно. Это означает, что реальное распределение заряда и требуемая поляризация растворителя не находятся в «равновесии». Однако возможно, что растворитель принимает конфигурацию, соответствующую «переходному состоянию», даже если электрон находится на доноре или акцепторе. Однако это требует энергии. Эта энергия может быть обеспечена тепловой энергией растворителя и тепловые колебания может обеспечить правильное состояние поляризации. Как только это будет достигнуто, электрон может прыгнуть. В творчество правильного расположения растворителя и скачок электронов не связаны и не происходят в синхронном процессе. Таким образом, энергия переходного состояния - это в основном энергия поляризации растворителя.
Теория Маркуса
Макроскопическая система: две проводящие сферы
На основании своих рассуждений Р.А. Маркус разработал классический теории с целью вычисления энергии поляризации указанного неравновесного состояния. Из термодинамики хорошо известно, что энергия такого состояния может быть определена, если найден обратимый путь к этому состоянию. Маркусу удалось найти такой путь с помощью двух обратимых этапов зарядки для подготовки «переходного состояния» от комплекса-предшественника.
Для модели, на которой основана теория, необходимы четыре элемента:
- Маркус использует классическую чисто электростатическую модель. Заряд (множество элементарных зарядов) может передаваться в любой части от одного тела к другому.
- Маркус разделяет поляризацию быстрых электронов Pе а медленный атом и ориентационная поляризация Pты растворителя из-за их постоянных времени, различающихся на несколько порядков.
- Маркус разделяет внутреннюю сферу (реагент + прочно связанные молекулы растворителя в комплексах + лиганды) и внешнюю сферу (свободный растворитель)
- В этой модели Маркус ограничивается вычислением энергии внешней сферы неравновесной поляризации «переходного состояния». Энергия внешней сферы часто намного больше, чем вклад внутренней сферы из-за далеко идущих электростатических сил (сравните Теория Дебая-Хюккеля электрохимии).
Инструмент Маркуса - теория диэлектрической поляризации в растворителях. Он решил задачу о переносе заряда между двумя телами произвольной формы с произвольной поверхностью и объемным зарядом в общем виде. Для реакции самообмена окислительно-восстановительная пара (например, Fe (H2O)63+ / Fe (H2O)62+) заменяется двумя макроскопическими проводящими сферами на определенном расстоянии, несущими указанные заряды. Между этими сферами происходит обратимый обмен определенного количества заряда.
На первом этапе энергия Wя перевода определенной суммы заряда, например для системы в состоянии, когда обе сферы несут половину количества заряда, которое должно быть передано. Это состояние системы может быть достигнуто путем передачи соответствующего заряда с донорной сферы в вакуум, а затем обратно на акцепторную сферу.[10] Затем сферы в этом состоянии заряда создают определенное электрическое поле в растворителе, которое создает общую поляризацию растворителя Pты + Pе. Точно так же эта поляризация растворителя взаимодействует с зарядами.
На втором этапе энергия WII обратимого (обратного) переноса заряда на первую сферу снова через вакуум. Тем не мение, атомная и ориентационная поляризация Pты фиксируется, только электронная поляризация Pе может адаптироваться к области нового распределения заряда и фиксированная Pты. После этого второго шага система находится в желаемом состоянии с электронной поляризацией, соответствующей начальной точке окислительно-восстановительной реакции, и атомной и ориентационной поляризацией, соответствующей «переходному состоянию». Энергия Wя + WII этого состояния есть, термодинамически говоря, свободная энергия Гиббса G.

Конечно, в этой классической модели возможен перенос любого произвольного количества заряда Δe. Таким образом, можно измерить энергию неравновесного состояния и, следовательно, энергию поляризации растворителя как функцию от Δe. Таким образом, Маркус очень элегантно сгруппировал координаты всех молекул растворителя в одну координату поляризации растворителя Δp, которая определяется величиной перенесенного заряда Δe. Таким образом, он упростил представление энергии до двух измерений: G = f (Δe). Результатом для двух проводящих сфер в растворителе является формула Маркуса
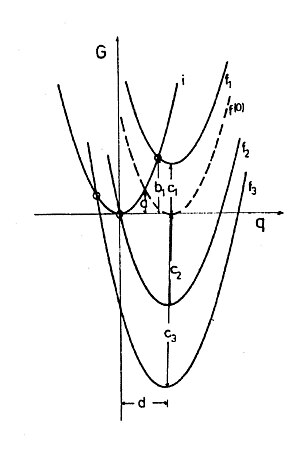
Где г1 и г2 - радиусы сфер, R - расстояние между ними, εs и εвыбрать - статическая и высокочастотная (оптическая) диэлектрическая проницаемость растворителя, Δe - величина переносимого заряда. График зависимости G от Δe представляет собой параболу (рис. 1). В теории Маркуса энергия, относящаяся к переносу единичного заряда (Δe = 1), называется энергией реорганизации (внешней сферы) λо, то есть энергия состояния, в котором поляризация соответствовала бы переносу единицы заряда, но реальное распределение заряда - это то, что было до передачи.[11] По направлению обмена система симметрична.
Микроскопическая система: донорно-акцепторная пара
Сжатие модели двух сфер до молекулярного уровня создает проблему, заключающуюся в том, что в реакции самообмена заряд больше не может передаваться в произвольных количествах, а только в виде одного электрона. Однако поляризация по-прежнему определяется общим ансамблем молекул растворителя и, следовательно, может рассматриваться классически, т.е. энергия поляризации не подлежит квантовым ограничениям. Следовательно, энергия реорганизации растворителя может быть рассчитана как обусловленная гипотетический перенос и обратный перенос частичного элементарного заряда по формуле Маркуса. Таким образом, энергия реорганизации для химических окислительно-восстановительных реакций, которая представляет собой свободную энергию Гиббса, также является параболической функцией Δe этого гипотетического переноса. Для реакции самообмена, где по причинам симметрии Δe = 0,5, свободная энергия активации Гиббса равна ΔG (0)‡ = λо/ 4 (см. Фиг. 1 и фиг. 2 пересечение парабол I и f, f (0) соответственно).
До сих пор все было физикой, теперь немного химии. Реакция самообмена является очень специфической окислительно-восстановительной реакцией, большинство окислительно-восстановительных реакций происходит между разными партнерами.[12] например
и они имеют положительную (эндергоническую) или отрицательную (экзергоническую) энергию реакции Гиббса. .
Расчеты Маркуса относятся исключительно к электростатическим свойствам растворителя (внешней сферы). и независимы друг от друга и поэтому могут быть просто суммированы. Это означает, что параболы Маркуса в системах с разными сдвинуты вверх или вниз в против. диаграмма (рис. 2). Вариация могут быть затронуты в экспериментах, предлагая разные акцепторы одному и тому же донору.
Несложные расчеты точек пересечения парабол i, , , и к дать Гиббсу свободную энергию активации
Пересечение этих парабол представляет собой энергию активации, а не энергию переходного состояния фиксированной конфигурации всех ядер в системе, как в случае замещения и других упомянутых реакций. Переходное состояние последних реакций должно соответствовать структурным и энергетическим условиям, окислительно-восстановительные реакции должны соответствовать только потребности в энергии. В то время как геометрия переходного состояния в других реакциях одинакова для всех пар реагентов, для окислительно-восстановительных пар многие поляризационные среды могут соответствовать энергетическим условиям.
Формула Маркуса показывает квадратичную зависимость свободной энергии активации Гиббса от свободной энергии Гиббса реакции. Из большого химического опыта известно, что реакции обычно тем быстрее, чем больше отрицательных . Во многих случаях обнаруживается даже линейная зависимость свободной энергии. Согласно формуле Маркуса, скорости возрастают также, когда реакции более экзэргонические, но только до тех пор, пока положительный или слегка отрицательный. Удивительно, что для окислительно-восстановительных реакций по формуле Маркуса энергия активации должна увеличиваться для очень экзергонической реакции, т.е. в случаях, когда отрицательно и его абсолютное значение больше, чем у . Эта область свободной энергии реакции Гиббса называется «перевернутой областью Маркуса». На рис.2 становится очевидным, что пересечение парабол i и f движется вверх в левой части графика, когда продолжает становиться все более негативным, а это означает увеличение энергии активации. Таким образом, общий график против. должно быть максимум.
Максимум ставки ET ожидается на Здесь и (Рис. 2), что означает, что электрон может перейти в комплекс-предшественник при его равновесной поляризации. Термическая активация не требуется: реакция безбарьерная. В перевернутой области поляризация соответствует трудно вообразимому представлению о распределении заряда, при котором донор получил заряд, а акцептор отдает заряд. Конечно, в реальном мире этого не происходит, критическую поляризацию создает не реальное распределение заряда, а тепловые флуктуации в растворителе. Эта поляризация, необходимая для передачи в инвертированной области, может быть создана с некоторой вероятностью так же, как и любая другая.[13] Электрон просто ждет, когда он прыгнет.
Перенос электронов во внутренней сфере
В модели внешней сферы донор или акцептор и прочно связанные сольватные оболочки или комплексные лиганды считались образующими жесткие структуры, которые не изменяются в процессе переноса электрона. Однако расстояния во внутренней сфере зависят от заряда донора и акцептора, например расстояния между центральными ионами и лигандами различны в комплексах, несущих разные заряды, и снова должен соблюдаться принцип Франка-Кондона: для того, чтобы электрон совершил прыжок, ядра должны иметь конфигурацию, идентичную конфигурации предшественника и предшественника. комплексы-преемники, конечно, сильно искажены. В этом случае потребность в энергии удовлетворяется автоматически.
В этом случае внутренней сферы действует концепция Аррениуса, переходное состояние определенной геометрической структуры достигается по геометрической координате реакции, определяемой движением ядер. Никакого дальнейшего движения ядра не требуется, чтобы сформировать последующий комплекс, только скачки электронов, что имеет значение для теории TST. Координата реакции для энергии внутренней сферы определяется вибрациями, и они различаются по окисленным и восстанавливающим частицам.[14]
Для системы самообмена Fe2+/ Fe3+ учитывается только симметричная дыхательная вибрация шести молекул воды вокруг ионов железа.[14] Предполагая гармонические условия, эта вибрация имеет частоты и , силовые постоянные fD и еА находятся и энергии
где q0 - нормальная координата равновесия и смещение по нормальной координате, множитель 3 происходит от 6 (H2O) · ½. Как и для внешнесферной энергии реорганизации, кривая потенциальной энергии квадратична, но здесь, однако, как следствие колебаний.
Нормальные координаты равновесия различаются величиной Fe (H2O)62+ и Fe (H2O)63+. Путем теплового возбуждения дыхательной вибрации может быть достигнута геометрия, общая как для донора, так и для акцептора, то есть кривые потенциальной энергии дыхательных колебаний D и A пересекаются здесь. Это ситуация, когда электрон может прыгнуть. Энергия этого переходного состояния есть энергия реорганизации внутренней сферы λв.
Для реакции самообмена расстояние металл-вода в переходном состоянии может быть вычислено[14]
Это дает энергию реорганизации внутренней сферы.
К счастью, выражения для энергий внешней и внутренней реорганизации имеют одинаковую квадратичную форму. Энергии реорганизации внутренней и внешней сферы независимы, поэтому их можно сложить, чтобы получить и вставлен в уравнение Аррениуса
Здесь можно увидеть, что A представляет вероятность скачка электрона, ехр [-Δграммв‡/kT] достижение переходного состояния внутренней сферы и ехр [-Δграммо‡/kT] регулировка внешней сферы.
Для несимметричных (перекрестных) реакций типа
выражение для также можно получить, но это более сложно.[14] Эти реакции имеют свободную энтальпию реакции ΔG0 который не зависит от энергии реорганизации и определяется различными окислительно-восстановительными потенциалами пары железа и кобальта. Следовательно, квадратное уравнение Маркуса справедливо также для энергии реорганизации внутренней сферы, включая предсказание перевернутой области. Это можно визуализировать следующим образом: (а) в нормальной области как начальное, так и конечное состояние должны иметь растянутые связи, (б) в Δ G‡ = 0, когда равновесная конфигурация начального состояния представляет собой растянутую конфигурацию конечного состояния, и (c) в перевернутой области начальное состояние имеет сжатые связи, тогда как конечное состояние имеет сильно растянутые связи. Аналогичные соображения справедливы для комплексов металлов, где лиганды больше, чем молекулы растворителя, а также для полиядерных комплексов с лигандными мостиками.
Вероятность скачка электрона
Сила электронной связи донора и акцептора определяет, будет ли реакция переноса электрона адиабатической или неадиабатической. В неадиабатическом случае связь слабая, т. Е. HAB на рис. 3 мала по сравнению с энергией реорганизации, а донор и акцептор сохраняют свою идентичность. В системе есть определенные вероятность для перехода от начальной к конечной кривой потенциальной энергии. В адиабатическом случае связь значительна, зазор 2 HAB больше, и система остается на более низкой кривой потенциальной энергии.[15]
Теория Маркуса, изложенная выше, представляет собой неадиабатический случай.[16] Следовательно, полуклассический Теория Ландау-Зинера может применяться, что дает вероятность взаимного превращения донора и акцептора за один проход системы через область пересечения кривых потенциальной энергии
где Hесли - энергия взаимодействия на пересечении, v скорость системы через область пересечения, sя и sж спусков есть.
Рис. 3 Энергетическая диаграмма для переноса электрона, включая реорганизацию внутренней и внешней сферы и электронное взаимодействие: вертикальная ось - это свободная энергия, а горизонтальная ось - «координата реакции» - упрощенная ось, представляющая движение всех ядер атомов (включая реорганизация растворителя)
Разрабатывая это, мы приходим к основному уравнению теории Маркуса.
куда - константа скорости переноса электрона, - электронная связь между начальным и конечным состояниями, это энергия реорганизации (как внутренняя, так и внешняя), и это общая Свободная энергия Гиббса изменение для реакции переноса электрона ( это Постоянная Больцмана и это абсолютная температура ).
Таким образом, теория Маркуса основывается на традиционном уравнении Аррениуса для скоростей химических реакций двумя способами: 1. Он предоставляет формулу для энергии активации, основанную на параметре, называемом энергией реорганизации, а также свободной энергии Гиббса. Энергия реорганизации определяется как энергия, необходимая для «реорганизации» структуры системы от начальных до конечных координат без передачи заряда. Он обеспечивает формулу для предэкспоненциального множителя в уравнении Аррениуса, основанную на электронной связи между начальным и конечным состояниями реакции переноса электрона (т. Е. Перекрытием электронных волновых функций двух состояний).
Результаты экспериментов
Маркус опубликовал свою теорию в 1956 году. В течение многих лет велись интенсивные поиски перевернутой области, которая могла бы стать доказательством теории. Но все эксперименты с сериями реакций все более отрицательных ΔG0 выявили только увеличение скорости реакции до диффузионного предела, т.е. до значения, указывающего на то, что каждый столкновение приводит к переносу электрона, и этот предел сохраняется также для очень отрицательных ΔG0 ценности (поведение Рема-Веллера).[17] Прошло около 30 лет, прежде чем Миллер, Калькатерра и Клосс однозначно обосновали перевернутую область для внутримолекулярного переноса электрона в молекуле, где донор и акцептор удерживаются на постоянном расстоянии с помощью жесткого спейсера (рис.4).[18]

Апостериори можно предположить, что в системах, где партнеры реакции могут свободно диффундировать, можно искать оптимальное расстояние для скачка электрона, т.е. расстояние, на котором ΔG‡ = 0 и ΔG0 = - λо. Для λо зависит от R, λо увеличивается при больших R и меньшем раскрытии параболы. Формально всегда можно замкнуть параболу на рис. 2 до такой степени, чтобы f-парабола пересекала i-параболу в вершине. Тогда всегда ΔG‡ = 0 и скорость k достигает максимального диффузионного значения для всех очень отрицательных ΔG0. Однако существуют и другие концепции этого явления,[1] например участие возбужденных состояний или уменьшение констант скорости будет настолько далеко в инвертированной области, что не поддается измерению.
Р. А. Маркус и его коллеги развили изложенную здесь теорию в нескольких аспектах. Они включали, помимо прочего, статистические аспекты и квантовые эффекты,[20] они применили теорию к хемилюминесценции[21] и электродные реакции.[22] Р. А. Маркус получил Нобелевскую премию по химии в 1992 году, и его Нобелевская лекция дает обширный обзор его работы.[1]
Смотрите также
Рекомендации
- ^ а б c d «Реакции переноса электрона в химии: теория и эксперимент». Nobelstiftung. 8 декабря 1992 г.. Получено 2 апреля 2007.
- ^ В отличие от подхода Маркуса теория переноса электронов во внутренней сфере Ноэль С. Хаш относится к непрерывный изменение концентрации электронов при переносе по геометрической координате (адиабатический case), а также учитывает влияние растворителя, как это сделал Маркус. Формулировка Хаша известна как теория Маркуса-Хаша.
- ^ Тише, Н. Пер. Faraday Soc. 1961 г., 57,557
- ^ а б П. В. Аткинс: Физическая химия, 6. Ред., Oxford University Press, Oxford, 1998, стр.830.
- ^ а б Р.С. Берри, С.А. Райс, Дж. Росс: Физическая химия, Wiley, New York 1980, S. 1147 и далее,
- ^ Миллер Дж. Р., Калькатерра Л. Т., Клосс Г. Л.: «Внутримолекулярный перенос электронов на большие расстояния в анион-радикалах. Влияние свободной энергии и растворителя на скорость реакции», J.Am.Chem.Soc. 1984, 106, 3047, Дои:10.1021 / ja00322a058
- ^ а б Маркус, Р.А. «К теории окислительно-восстановительных реакций с переносом электрона I» J.Chem.Phys.1956, 24, 966. Дои:10.1063/1.1742723 или же Открытый текст[постоянная мертвая ссылка ]
- ^ а б Маркус. «Электростатическая свободная энергия и другие свойства состояний с неравновесной поляризацией I. J.Chem.Phys.1956, 24, 979. Дои:10.1063/1.1742724 или же Открытый текст[постоянная мертвая ссылка ]
- ^ W.F. Либби, "Теория реакций электронного обмена в водном растворе" J.Phys.Chem. 1952, 56, 863
- ^ Маркус принимает вакуумное состояние реагентов как точку нулевой энергии. Поэтому многие из его уравнений содержат также энергию сольватации изолированной частицы Wiso и электростатическая энергия образования комплексов-предшественников и последователей.
- ^ Примечание: квадратичная зависимость энергии реорганизации внешней сферы имеет вид нет следствие вибрации реагентов или растворителя!
- ^ их часто называют перекрестными реакциями Маркуса.
- ^ Обратная реакция может поддерживать понимание: для этой реакции поляризации из-за гипотетической передачи заряда единичного электрона недостаточно для достижения поляризации, при которой энергии поляризации A / D и A−/ D+ равны. Это может произойти только при гипотетической передаче заряда более одного электрона.
- ^ а б c d Н. Сутин, «Теория реакций переноса электрона: взгляд в прошлое», Прогр. Неорг. Chem. 1083, г. 30, 441-448
- ^ В обычных химических реакциях, таких как замещения, которые протекают через переходное состояние, верхняя кривая потенциальной энергии идет настолько высоко, что ею пренебрегают.
- ^ Теория адиабатического переноса электрона с участием движения ядра (которое можно рассматривать как перенос заряда, а не скачок электрона) была разработана Хашем.
- ^ Рем, Д., Веллер, А. "Kinetik und Mechanismus der Elektronenübertragung bei der Fluoreszenzlöschung in Acetonitril" Бер. Bunsenges.Physik.Chem. 1969, 73, 834-839 охарактеризовали это поведение эмпирической формулой
- ^ Миллер Дж. Р., Калькатерра Л. Т., Клосс Г. Л.: «Внутримолекулярный перенос электронов на большие расстояния в анион-радикалах. Влияние свободной энергии и растворителя на скорость реакции», J.Am.Chem.Soc. 1984, 106, 3047, Дои:10.1021 / ja00322a058
- ^ Мы рекомендуем ссылаться на исходную статью, JACS не лицензирует Википедию для графиков.
- ^ Сидерс, П., Маркус, Р. А. "Квантовые эффекты в реакциях переноса электрона" J.Am.Chem.Soc. 1981,103, 741; Сидерс, П., Маркус, Р. А. «Квантовые эффекты для реакций переноса электрона в« инвертированной области »» J.Am.Chem.Soc. 1981,103,748
- ^ Маркус. Р.А. «К теории хемилюминесцентных реакций с переносом электрона» J.Chem.Phys. 1965,43,2654
- ^ Маркус, Р. А. "К теории реакции переноса электрона. VI. Унифицированное рассмотрение гомогенных и электродных реакций" J.Chem.Phys. 1965, 43,679
Ключевые документы Маркуса
- Маркус, Р.А. (1956). «К теории окислительно-восстановительных реакций с переносом электрона. I» (PDF). J. Chem. Phys. 24 (5): 966–978. Bibcode:1956ЖЧФ..24..966М. Дои:10.1063/1.1742723.
- Маркус, Р.А. (1956). «Свободная электростатическая энергия и другие свойства состояний с неравновесной поляризацией. I» (PDF). J. Chem. Phys. 24 (5): 979–989. Bibcode:1956ЖЧФ..24..979М. Дои:10.1063/1.1742724.
- Маркус, Р.А. (1957). "К теории окислительно-восстановительных реакций с участием переноса электрона. II. Приложения к данным о скоростях реакций изотопного обмена" (PDF). J. Chem. Phys. 26 (4): 867–871. Bibcode:1957ЖЧФ..26..867М. Дои:10.1063/1.1743423.
- Маркус, Р.А. (1957). «К теории окислительно-восстановительных реакций с участием переноса электрона. III. Приложения к данным о скоростях органических окислительно-восстановительных реакций» (PDF). J. Chem. Phys. 26 (4): 872–877. Bibcode:1957ЖЧФ..26..872М. Дои:10.1063/1.1743424.
- Маркус, Р.А. (1960). «Реакции обмена и реакции переноса электрона, включая изотопный обмен. Теория окислительно-восстановительных реакций с участием переноса электрона. Часть 4. Статистико-механическая основа для обработки вкладов растворителя, лигандов и инертной соли» (PDF). Обсуждать. Faraday Soc. 29: 21–31. Дои:10.1039 / df9602900021.
- Маркус, Р.А. (1963). «К теории окислительно-восстановительных реакций с участием электронного переноса. V. Сравнение и свойства электрохимических и химических констант скорости». J. Phys. Chem. 67 (4): 853–857. Дои:10.1021 / j100798a033. OSTI 4712863.
- Маркус, Р.А. (1964). «Химическая и электрохимическая теория переноса электрона». Анну. Rev. Phys. Chem. 15 (1): 155–196. Bibcode:1964ARPC ... 15..155M. Дои:10.1146 / annurev.pc.15.100164.001103.
- Маркус, Р.А. (1965). "К теории реакций с переносом электрона. VI. Единый подход к гомогенным и электродным реакциям" (PDF). J. Chem. Phys. 43 (2): 679–701. Bibcode:1965ЖЧФ..43..679М. Дои:10.1063/1.1696792.
- Marcus, R.A .; Сутин Н (1985). «Электронные переводы в химии и биологии». Биохим. Биофиз. Acta. 811 (3): 265. Дои:10.1016 / 0304-4173 (85) 90014-Х.


![{ displaystyle { ce {{D} + A <=> [k_ {12}] [k_ {21}] [D { dotsm} A] <=> [k_ {23}] [k_ {32}] [D + { dotsm} A ^ {-}] -> [k_ {30}] {D +} + {A ^ {-}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9011d1fe6f8639a87bf5c31e70967d0fcdf4bcc1)




![{ displaystyle { ce {{[Fe ^ {II} (CN) 6] ^ {4 -}} + {[Ir ^ {IV} Cl6] ^ {2 -}} <=> {[Fe ^ {III } (CN) 6] ^ {3 -}} + {[Ir ^ {III} Cl6] ^ {3-}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/31656dcef696dc00f999db7bf1e70e8747989c22)



























![{ Displaystyle { ce {{[Fe (H2O) 6] ^ {2} +} + {[Co (H2O) 6] ^ {3} +} <=> {[Fe (H2O) 6] ^ {3 } +} + {[Co (H2O) 6] ^ {2} +}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6cc3b6ef06cdd44100c25f3909ffaf574da148c0)

![{ displaystyle P_ {if} = 1- exp left [- { frac {4 pi ^ {2} {H_ {if} ^ {2}}} {hv mid (s_ {i} -s_ { f}) mid}} right]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/81a2e37aeda14be451b6848ad207200e6055cc1e)






