Метилэкгонидин - Methylecgonidine
 | |
| Имена | |
|---|---|
| Название ИЮПАК Метил (1S,5р) -8-метил-8-азабицикло [3.2.1] окт-3-ен-4-карбоксилат | |
| Другие имена Ангидрометилэкгонин Метиловый эфир ангидроэкгонина | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.164.719 |
PubChem CID | |
| UNII | |
| |
| |
| Свойства | |
| C10ЧАС15NО2 | |
| Молярная масса | 181.235 г · моль−1 |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Метилэкгонидин (ангидрометилэкгонин; метиловый эфир ангидроэкгонина; AEME) представляет собой промежуточное химическое соединение, полученное из экгонин или кокаин.
Метилэкгонидин - это пиролиз продукт образовался, когда кокаин курят, что делает это вещество полезным биомаркером для специального тестирования на использование крэк-кокаина, в отличие от порошкового кокаина, который не образует метилэкгонидин в качестве метаболит.[1] Метилэкгонидин имеет относительно короткий период полувыведения - 18–21 минуту, после чего он метаболизируется до экгонидин, что означает, что относительные концентрации двух соединений могут использоваться для оценки того, как недавно курили кокаин. Было показано, что метилэкгонидин особенно вреден для организма, чем другие побочные продукты кокаина; например к сердцу,[2] легкие[3] & печень.[4] Токсичность обусловлена частичный агонист эффект на M1 и М3 мускариновые рецепторы, что приводит к Фрагментация ДНК и гибель нейронов апоптоз.[5]
AEME также используется в научных исследованиях для производства фенилтропан аналоги такие как тропарил, дихлорпан, иометопан, и CFT. Метилэкгонидин также теоретически можно использовать для производства кокаин и так может быть контролируемое вещество в некоторых странах.
Синтез
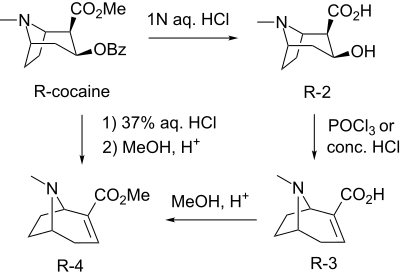
Метилэкгонидин может быть синтезирован без пиролитически от кокаина через гидролиз /обезвоживание[6] с последующим этерификация с метанолом.[7][8]

Схема Клайна[9] основан на реакции 2,4,6-циклогептатриен-7-карбоновой кислоты с метиламином. Это модифицированная версия Патент США 2783235 Грундманн и Оттманн. В сопроводительном патенте Патент США 2783236 эти же авторы реагируют на свой метилэкгонидин с двумя эквивалентами PhLi образовывать третичный спирт путем "твердого" добавления к сложному эфиру, а не "мягкого" Майкл дополнение. Однако эффективность продукта составляет всего одну десятую от атропин. Метил 2,4,6-циклогептатриен-1-карбоксилат может быть получен синтетически.[10][11]

Дэвис и другие. синтезированный (р/S) -метилэкгонидин тандемным циклопропанированием /Справиться перестановкой.[13][14] Таким образом, реакция метилдиазобутеноата (2) с 5 экв. N- ((2- (ТМС) этокси) карбонил) пиррол (1) в присутствии гексаноата родия (II) / гексана дает [3.2.1] -азабициклическую систему (р/S)-8 с доходностью 62%. Незамещенную двойную связь селективно восстанавливали с использованием Катализатор Уилкинсона для получения N-защищенного метилового эфира ангидроэкгонина ((р/S)-4). После снятия защиты азота N8 с помощью TBAF и восстановительное метилирование формальдегидом и цианоборгидрид натрия, (р/S)-5 был получен в целом с хорошим урожаем.
Смотрите также
использованная литература
- ^ Scheidweiler KB, Plessinger MA, Shojaie J, Wood RW, Kwong TC (декабрь 2003 г.). «Фармакокинетика и фармакодинамика метилэкгонидина, пиролизата крэк-кокаина». Журнал фармакологии и экспериментальной терапии. 307 (3): 1179–87. Дои:10.1124 / jpet.103.055434. PMID 14561847. S2CID 15619796.
- ^ Фармакокинетика и фармакодинамика метилэкгонидина, пиролизата кокаинового крема - Scheidweiler et al. 307 (3): 1179 Рисунок IG6 - Журнал фармакологии и экспериментальной терапии.
- ^ Ян Й, Ке Q, Цай Дж, Сяо Ю. Ф., Морган Дж. П. (январь 2001 г.). «Доказательства стимуляции кокаином и метилэкгонидином мускариновых рецепторов M (2) в культивируемых эмбриональных клетках легких человека». Британский журнал фармакологии. 132 (2): 451–60. Дои:10.1038 / sj.bjp.0703819. ЧВК 1572570. PMID 11159694.
- ^ Fandiño AS, Toennes SW, Kauert GF (декабрь 2002 г.). «Исследования гидролитических и окислительных метаболических путей метилового эфира ангидроэкгонина (метилэкгонидина) с использованием микросомальных препаратов из органов крысы». Химические исследования в токсикологии. 15 (12): 1543–8. Дои:10.1021 / tx0255828. PMID 12482236.
- ^ Гарсия Р.К., Дати Л.М., Торрес Л.Х., да Силва М.А., Удо М.С., Абдалла FM и др. (Декабрь 2015 г.). «Мускариновые рецепторы M1 и M3 могут играть роль в нейротоксичности метилового эфира ангидроэкгонина, продукта пиролиза кокаина». Научные отчеты. 5: 17555. Bibcode:2015НатСР ... 517555Г. Дои:10.1038 / srep17555. ЧВК 4667193. PMID 26626425.
- ^ Басмаджян Г.П., Сингх С., Састродджоджо Б., Смит Б.Т., Авор К.С., Чанг Ф. и др. (Ноябрь 1995 г.). «Создание поликлональных каталитических антител против кокаина с использованием аналогов кокаина, конъюгированных с дифтерийным анатоксином». Химико-фармацевтический бюллетень. 43 (11): 1902–11. Дои:10.1021 / ja01502a049. PMID 8575031.
- ^ Де Йонг А.В. (1937). «Некоторые свойства экгонинов и их сложных эфиров II. Структурные формулы экгонинов и экгонидина». Recueil des Travaux Chimiques des Pays-Bas. 56 (2): 186–97, 198–201. Дои:10.1002 / recl.19370560215.
- ^ Матчетт Дж. Р., Левин Дж. (1941). «Выделение метилового эфира экгонидина из семян коки 1». Варенье. Chem. Soc. 63 (9): 2444–2446. Дои:10.1021 / ja01854a038.
- ^ Клайн Р. Х., Райт Дж., Фокс К. М., Эльдефрави МЭ (июль 1990 г.). «Синтез аналогов 3-арилэкгонина как ингибиторов связывания кокаина и захвата дофамина». Журнал медицинской химии. 33 (7): 2024–7. Дои:10.1021 / jm00169a036. PMID 2362282.
- ^ http://www.chemsynthesis.com/base/chemical-structure-15475.html
- ^ Anciaux AJ, Demonceau A, Noels AF, Hubert AJ, Warin R, Teyssie P (1981). «Катализируемые переходными металлами реакции диазосоединений. 2. Присоединение к ароматическим молекулам: Катализ Бюхнеровского синтеза циклогептатриенов». Журнал органической химии. 46 (5): 873–876. Дои:10.1021 / jo00318a010.
- ^ Дэвис Х.М., Хьюби, штат Нью-Джерси (1992). «Энантиоселективный синтез тропанов реакцией винилкарбеноидов, стабилизированных родием, с пирролами». Буквы Тетраэдра. 33 (46): 6935–6938. Дои:10.1016 / S0040-4039 (00) 60899-7. ISSN 0040-4039.
- ^ Дэвис, Х. М. Л .; Saikali, E .; Янг, В. Б. (1991). «Синтез (. + -.) - ферругинина и (. + -.) - метилового эфира ангидроэкгонина тандемным циклопропанированием / перегруппировкой Копе». J. Org. Chem. 56 (19): 5696–5700. Дои:10.1021 / jo00019a044.
- ^ Дэвис Х.М., Янг В.Б., Смит HD (январь 1989 г.). «Новое вхождение в тропановую систему путем реакции винилкарбеноидов, стабилизированных ацетатом родия (II), с пирролами». Буквы Тетраэдра. 30 (35): 4653–6. Дои:10.1016 / S0040-4039 (01) 80766-8.
