Белок, инактивирующий рибосомы - Ribosome-inactivating protein
| Белок, инактивирующий рибосомы | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
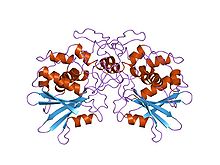 Структура противовирусного белка лука.[1] | |||||||||||
| Идентификаторы | |||||||||||
| Символ | ПОКОЙСЯ С МИРОМ | ||||||||||
| Pfam | PF00161 | ||||||||||
| ИнтерПро | IPR001574 | ||||||||||
| PROSITE | PDOC00248 | ||||||||||
| SCOP2 | 1paf / Объем / СУПФАМ | ||||||||||
| |||||||||||
А белок, инактивирующий рибосомы (ПОКОЙСЯ С МИРОМ) это ингибитор синтеза белка что действует в рибосома.[2]
Ряд бактериальных и растительных токсинов действует, подавляя синтез белка в эукариотический клетки. Токсины Шига и рицин семейство инактивирует 60S рибосомные субъединицы посредством N-гликозидного расщепления, которое высвобождает специфический аденин основа из сахарно-фосфатного остова 28S рРНК.[3][4][5] Члены семейства включают токсины шига и шига-подобные токсины, а также тип I (например, трихосантин и лаффин ) и тип II (например, рицин, агглютинин, и абрин ) белки, инактивирующие рибосомы (RIP). Все эти токсины структурно связаны. RIP представляют значительный интерес из-за их потенциального использования, конъюгированного с моноклональными антителами, в качестве иммунотоксины лечить раки. В дальнейшем, трихосантин было показано, что он обладает сильной активностью против ВИЧ-1 -зараженный Т-клетки и макрофаги.[6] Таким образом, выяснение структурно-функциональных взаимосвязей RIP стало серьезным исследовательским усилием. Теперь известно, что RIP структурно связаны. Консервативный глутаминовый остаток участвует в каталитическом механизме;[7] это находится рядом с консервированным аргинином, который также играет роль в катализе.[8]
Примеры включают:
- Абрин
- Beetin
- Рицин
- Сапорин
- Шига токсин
- Спироплазма белки[9]
- Трихосантин
- Вискумин (Европейская омела )
- Противовирусный протеин из семян марихуаны (Phytolacca americana)[10]
Белки, инактивирующие рибосомы (RIP), делятся на три типа в зависимости от состава белковых доменов:
- Тип I: RIP-I представляют собой полипептиды, состоящие из домена A. Это сайт активности N-гликозидазы.
- Тип II: RIP-II состоят из домена A с каталитической активностью, аналогичной RIP типа I, и домена B со свойствами связывания лектина. Эти свойства облегчают проникновение в клетку, что делает тип II особенно цитотоксичным. Домены A и B соединены дисульфидными связями.[11]
- RIP-II считаются сильнодействующими токсинами. Домен В способен связывать галактозильные фрагменты на поверхности клетки, что облегчает проникновение в клетку, где домен А может выполнять свою каталитическую активность на 28S рРНК в цитозоле.[12]
- Тип III: RIP-III разделены на две подгруппы. Одна подгруппа содержит тот же исходный домен RIP (A) и C-терминал с неизвестными функциями. Другая подгруппа аналогична Типу I, но содержит сайт для инактивации.[11]
Они существуют в бактериях и растениях.[13]
Лишь небольшая часть RIP токсична для человека при употреблении, и белки этого семейства обнаружены в подавляющем большинстве растений, используемых для потребления человеком, таких как рис, кукуруза и ячмень.
использованная литература
- ^ Монзинго А.Ф., Коллинз Э.Д., Эрнст С.Р., Ирвин Д.Д., Робертус Д.Д. (октябрь 1993 г.). «Структура 2.5A противовирусного белка из семян лука». Журнал молекулярной биологии. 233 (4): 705–15. Дои:10.1006 / jmbi.1993.1547. PMID 8411176.
- ^ Рибосома + инактивация + белки в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- ^ Эндо Ю., Цуруги К., Юцудо Т., Такеда Ю., Огасавара Т., Игараси К. (январь 1988 г.). «Сайт действия токсина Vero (VT2) из Escherichia coli O157: H7 и токсина Shiga на рибосомы эукариот. РНК N-гликозидазная активность токсинов». Европейский журнал биохимии. 171 (1–2): 45–50. Дои:10.1111 / j.1432-1033.1988.tb13756.x. PMID 3276522.
- ^ May MJ, Hartley MR, Roberts LM, Krieg PA, Osborn RW, Lord JM (январь 1989 г.). «Инактивация рибосом цепью рицина А: чувствительный метод оценки активности полипептидов дикого типа и мутантных полипептидов». Журнал EMBO. 8 (1): 301–8. Дои:10.1002 / j.1460-2075.1989.tb03377.x. ЧВК 400803. PMID 2714255.
- ^ Фунацу Г., Ислам MR, Минами Й, Сунг-Сил К., Кимура М. (1991). «Консервативные аминокислотные остатки в инактивирующих рибосомы белках растений». Биохимия. 73 (7–8): 1157–61. Дои:10.1016/0300-9084(91)90160-3. PMID 1742358.
- ^ Чжоу К., Фу З., Чен М., Линь И, Пан К. (май 1994 г.). «Структура трихосантина при разрешении 1,88 А». Белки. 19 (1): 4–13. Дои:10.1002 / prot.340190103. PMID 8066085.
- ^ Hovde CJ, Calderwood SB, Mekalanos JJ, Collier RJ (апрель 1988 г.). «Доказательства того, что глутаминовая кислота 167 является остатком активного центра шига-подобного токсина I». Труды Национальной академии наук Соединенных Штатов Америки. 85 (8): 2568–72. Bibcode:1988PNAS ... 85.2568H. Дои:10.1073 / пнас.85.8.2568. ЧВК 280038. PMID 3357883.
- ^ Монзинго А.Ф., Коллинз Э.Д., Эрнст С.Р., Ирвин Д.Д., Робертус Д.Д. (октябрь 1993 г.). «Структура 2.5 A противовирусного белка из семян лука». Журнал молекулярной биологии. 233 (4): 705–15. Дои:10.1006 / jmbi.1993.1547. PMID 8411176.
- ^ Hamilton PT, Peng F, Boulanger MJ, Perlman SJ (январь 2016 г.). "Белок, инактивирующий рибосомы в защитном симбионте дрозофилы". Труды Национальной академии наук Соединенных Штатов Америки. 113 (2): 350–5. Bibcode:2016ПНАС..113..350Н. Дои:10.1073 / pnas.1518648113. ЧВК 4720295. PMID 26712000.
- ^ Домашевский А.В., Goss DJ (январь 2015). «Противовирусный белок из семян семян марихуаны, белок, инактивирующий рибосомы: активность, ингибирование и перспективы». Токсины. 7 (2): 274–98. Дои:10.3390 / токсины7020274. ЧВК 4344624. PMID 25635465.
- ^ а б Лападула WJ, Аюб MJ (сентябрь 2017 г.). «Рибосомы, инактивирующие белки с эволюционной точки зрения». Токсикон. 136: 6–14. Дои:10.1016 / j.toxicon.2017.06.012. PMID 28651991. S2CID 9814488.
- ^ Фредрикссон, Стен-Оке; Артурссон, Элизабет; Бергстрём, Томас; Остин, Андерс; Нильссон, Калле; Остот, Кристер (декабрь 2014 г.). «Идентификация токсинов RIP-II с помощью аффинного обогащения, ферментативного расщепления и ЖХ-МС». Аналитическая химия. 87 (2): 967–974. Дои:10.1021 / ac5032918. ISSN 0003-2700. PMID 25496503.
- ^ Мак А.Н., Вонг Ю.Т., Ан Ю.Дж., Ча С.С., Сзе К.Х., Ау С.В. и др. (2007). «Исследование структуры-функции белка, инактивирующего рибосомы кукурузы: последствия для области внутренней инактивации и единственного глутамата в активном центре». Исследования нуклеиновых кислот. 35 (18): 6259–67. Дои:10.1093 / нар / гкм687. ЧВК 2094058. PMID 17855394.
| Этот биохимия статья - это заглушка. Вы можете помочь Википедии расширяя это. |
