Альфа-глюкозидаза - Alpha-glucosidase
| Альфа-глюкозидаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Гексамер альфа-глюкозидазы, Sulfolobus solfataricus | |||||||||
| Идентификаторы | |||||||||
| Номер ЕС | 3.2.1.20 | ||||||||
| Количество CAS | 9001-42-7 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| БРЕНДА | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| |||||||||
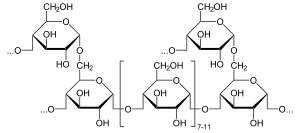
Альфа-глюкозидаза (EC 3.2.1.20, мальтаза, глюкоинвертаза, глюкозидосахараза, мальтаза-глюкоамилаза, альфа-глюкопиранозидаза, глюкозидоинвертаза, альфа-D-глюкозидаза, альфа-глюкозид гидролаза, альфа-1,4-глюкозидаза, альфа-D-глюкозид глюкогидролаза) это глюкозидаза расположен в кисть границы тонкой кишки, которая действует на связи α (1 → 4).[1][2][3][4][5][6] Это в отличие от бета-глюкозидаза. Альфа-глюкозидаза расщепляет крахмал и дисахариды до глюкозы. Мальтаза, аналогичный фермент, который расщепляет мальтоза, почти функционально эквивалентен.
Другие глюкозидазы включают:
Механизм
Альфа-глюкозидаза гидролизует концевые невосстанавливающие (1 → 4) -связанные остатки альфа-глюкозы с высвобождением одной молекулы альфа-глюкозы.[7] Альфа-глюкозидаза - это углевод-гидролаза, которая выделяет альфа-глюкозу в отличие от бета-глюкозы. Остатки бета-глюкозы могут высвобождаться глюкоамилазой, функционально подобным ферментом. Селективность альфа-глюкозидазы к субстрату обусловлена сродством активного сайта фермента.[8] Два предложенных механизма включают нуклеофильное замещение и промежуточный ион оксокарбения.[8]

- Родниус проликсус, кровососущее насекомое, образует гемозоин (Hz) при переваривании гемоглобина хозяина. Синтез гемозоина зависит от сайта связывания субстрата альфа-глюкозидазы.[9]
- Выделены и охарактеризованы альфа-глюкозидазы печени форели. Было показано, что для одной из альфа-глюкозидаз печени форели максимальная активность фермента увеличивалась на 80% во время физических упражнений по сравнению с отдыхающей форелью. Было показано, что это изменение коррелирует с увеличением активности гликогенфосфорилазы печени. Предполагается, что альфа-глюкозидаза в глюкозидном пути играет важную роль в дополнении фосфоролитического пути метаболической реакции печени на энергетические потребности в упражнениях.[10]
- Было показано, что альфа-глюкозидазы тонкого кишечника дрожжей и крыс ингибируются несколькими группами флавоноидов.[11]
Структура

Альфа-глюкозидазы можно разделить по первичной структуре на два семейства.[8]Ген, кодирующий лизосомальную альфа-глюкозидазу человека, имеет длину около 20 т.п.н., и его структура была клонирована и подтверждена.[12]
- Лизосомальная альфа-глюкозидаза человека была изучена на предмет значимости Asp-518 и других остатков в непосредственной близости от активного сайта фермента. Было обнаружено, что замена Asp-513 на Glu-513 препятствует посттрансляционной модификации и внутриклеточному транспорту предшественника альфа-глюкозидазы. Кроме того, остатки Trp-516 и Asp-518 считаются критическими для каталитической функциональности фермента.[13]
- Было показано, что кинетические изменения альфа-глюкозидазы вызываются денатурантами, такими как хлорид гуанидиния (GdmCl) и растворы SDS. Эти денатуранты вызывают потерю активности и конформационные изменения. Утрата активности фермента происходит при гораздо более низких концентрациях денатуранта, чем требуется для конформационных изменений. Это приводит к заключению, что конформация активного центра фермента менее стабильна, чем конформация фермента в целом, в ответ на два денатуранта.[14]
Актуальность болезни
- Болезнь накопления гликогена типа II, также называется Болезнь Помпе: заболевание с дефицитом альфа-глюкозидазы. В 2006 году препарат альглюкозидаза альфа стал первым выпущенным лекарством от болезни Помпе и действует как аналог альфа-глюкозидазы.[15] Дальнейшие исследования альглюкозидаза альфа показал, что иминосахары проявляют ингибирование фермента. Было обнаружено, что одна молекула соединения связывается с одной молекулой фермента. Было показано, что 1-дезоксиноджиримицин (DNJ) будет связывать самый сильный из тестируемых сахаров и почти полностью блокирует активный центр фермента. Исследования расширили знания о механизме связывания альфа-глюкозидазы с иминосахарами.[16]
- Сахарный диабет: Акарбоза, ингибитор альфа-глюкозидазы, конкурентно и обратимо ингибирует альфа-глюкозидазу в кишечнике. Это ингибирование снижает скорость всасывания глюкозы из-за замедленного переваривания углеводов и увеличения времени переваривания. Акарбоза может предотвратить развитие диабетических симптомов.[17] Следовательно, ингибиторы альфа-глюкозидазы (например, акарбоза) используются в качестве антидиабетических препаратов в сочетании с другими антидиабетическими препаратами. Лютеолин Было обнаружено, что он является сильным ингибитором альфа-глюкозидазы. Соединение может ингибировать фермент до 36% при концентрации 0,5 мг / мл.[18] С 2016 года это вещество проходит испытания на крысах, мышах и культура клеток. Аналоги флавоноидов обладают ингибирующей активностью.[19]
- Азооспермия: В диагностике азооспермии может помочь измерение активности альфа-глюкозидазы в семенной плазме. Активность семенной плазмы соответствует функциональности придатка яичка.[20]
- Противовирусные средства: Многие вирусы животных имеют внешнюю оболочку, состоящую из вирусных гликопротеинов. Они часто необходимы для жизненного цикла вируса и используют клеточные механизмы для синтеза. Ингибиторы альфа-глюкозидазы показывают, что этот фермент участвует в пути образования N-гликанов вирусов, таких как ВИЧ и вирус гепатита В человека (HBV). Ингибирование альфа-глюкозидазы может предотвратить слияние ВИЧ и секрецию HBV.[21]
Смотрите также
использованная литература
- ^ альфа-глюкозидазы в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- ^ Bruni, C.B .; Sica, V .; Auricchio, F .; Ковелли, И. (1970). «Дальнейшая кинетическая и структурная характеристика лизосомальной α-D-глюкозид глюкогидролазы из печени крупного рогатого скота». Биохим. Биофиз. Acta. 212 (3): 470–477. Дои:10.1016/0005-2744(70)90253-6. PMID 5466143.
- ^ Flanagan, P.R .; Форстнер, Г. (1978). «Очистка кишечной мальтазы / глюкоамилазы крыс и ее аномальная диссоциация при нагревании или при низком pH». Biochem. J. 173 (2): 553–563. Дои:10.1042 / bj1730553. ЧВК 1185809. PMID 29602.
- ^ Ларнер, Дж .; Lardy, H .; Мирбэк, К. (1960). «Другие глюкозидазы». В Boyer, P.D. (ред.). Ферменты. 4 (2-е изд.). Нью-Йорк: Academic Press. С. 369–378.
- ^ Сивиками, С .; Радхакришнан, А. (1973). «Очистка кишечной глюкоамилазы кролика с помощью аффинной хроматографии на сефадексе G-200». Индийский J. Biochem. Биофизы. 10 (4): 283–284. PMID 4792946.
- ^ Sørensen, S.H .; Norén, O .; Sjöström, H .; Даниэльсен, Э.М. (1982). «Амфифильные микроворсинки кишечника свиней, мальтаза / глюкоамилаза. Структура и специфичность». Евро. J. Biochem. 126 (3): 559–568. Дои:10.1111 / j.1432-1033.1982.tb06817.x. PMID 6814909.
- ^ «EC 3.2.1.20». ExPASy. Получено 1 марта 2012.
- ^ а б c Чиба С. (август 1997 г.). «Молекулярный механизм в альфа-глюкозидазе и глюкоамилазе». Biosci. Biotechnol. Биохим. 61 (8): 1233–9. Дои:10.1271 / bbb.61.1233. PMID 9301101.
- ^ Мури Ф. Б., да Силва-младший, Феррейра Л. С. и др. (2009). «Альфа-глюкозидаза способствует образованию гемозоина у кровососущих насекомых: история эволюции». PLoS ONE. 4 (9): e6966. Дои:10.1371 / journal.pone.0006966. ЧВК 2734994. PMID 19742319.
- ^ Мехрани Х., Стори К.Б. (октябрь 1993 г.). «Характеристика альфа-глюкозидаз из печени радужной форели». Arch. Biochem. Биофизы. 306 (1): 188–94. Дои:10.1006 / abbi.1993.1499. PMID 8215402.
- ^ Тадера К., Минами Й., Такамацу К., Мацуока Т. (апрель 2006 г.). «Ингибирование альфа-глюкозидазы и альфа-амилазы флавоноидами». J. Nutr. Sci. Витаминол. 52 (2): 149–53. Дои:10.3177 / jnsv.52.149. PMID 16802696.
- ^ Hoefsloot L; М. Хогевен-Вестервельд; А. Дж. Рейзер; Б. А. Остра (1 декабря 1990 г.). «Характеристика гена лизосомальной альфа-глюкозидазы человека». Biochem. J. 272 (2): 493–497. Дои:10.1042 / bj2720493. ЧВК 1149727. PMID 2268276.
- ^ Германс, Моник; Мариан Кроос; Джос Ван Бьюмен; Бен Остра; Арнольд Рейзер (25 июля 1991 г.). "Характеристика каталитического сайта лизосомальной α-глюкозидазой человека". Журнал биологической химии. 21. 266 (21): 13507–13512. Получено 1 марта 2012.
- ^ У XQ, Xu H, Yue H, Liu KQ, Wang XY (декабрь 2009 г.). «Кинетика ингибирования и агрегация альфа-глюкозидазы различными денатурантами». Белок J. 28 (9–10): 448–56. Дои:10.1007 / s10930-009-9213-0. PMID 19921411.
- ^ «FDA одобрило первое лечение болезни Помпе». Выпуск новостей FDA. FDA. Получено 1 марта 2012.
- ^ Yoshimizu, M .; Таджима, Y; Matsuzawa, F; Айкава, S; Ивамото, К. Кобаяши, Т; Эдмундс, Т; Fujishima, K; Цудзи, Д; Ито, К; Икекита, М; Кавасима, I; Sugawara, K; Охьянаги, N; Сузуки, Т; Togawa, T; Оно, К; Сакураба, Х (май 2008 г.). «Параметры связывания и термодинамика взаимодействия иминосахаров с рекомбинантной кислотной альфа-глюкозидазой человека (альглюкозидаза альфа): понимание механизма образования комплекса». Clin Chim Acta: 68–73.
- ^ Бишофф Х (август 1995 г.). «Механизм ингибирования альфа-глюкозидазы при лечении диабета». Clin Invest Med. 18 (4): 303–11. PMID 8549017.
- ^ Ким Дж. С., Квон К. С., Сон К. Х. (ноябрь 2000 г.). «Ингибирование альфа-глюкозидазы и амилазы лютеолином, флавоноидом». Biosci. Biotechnol. Биохим. 64 (11): 2458–61. Дои:10.1271 / bbb.64.2458. PMID 11193416.
- ^ Жен и др. (Ноябрь 2017 г.). «Синтез новых флавоноидных алкалоидов в качестве ингибиторов α-глюкозидазы». Биоорганическая и медицинская химия. 25 (20): 5355–64. Дои:10.1016 / j.bmc.2017.07.055. PMID 28797772.
- ^ Махмуд А.М., Геслевич Дж., Кинт Дж. И др. (Март 1998 г.). «Активность семенной альфа-глюкозидазы плазмы и мужское бесплодие». Гм. Репрод. 13 (3): 591–5. Дои:10.1093 / humrep / 13.3.591. PMID 9572418.
- ^ Мехта, Ананд; Зицманн, Николь; Радд, Полина М; Блок, Тимоти М; Двек, Раймонд А. (23 июня 1998 г.). «Ингибиторы α-глюкозидазы как потенциальные противовирусные средства широкого спектра действия». Письма FEBS. 430 (1–2): 17–22. Дои:10.1016 / S0014-5793 (98) 00525-0. PMID 9678587.

