Тетраметилсилан - Википедия - Tetramethylsilane
 | |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Тетраметилсилан | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| Сокращения | ТМС | ||
| 1696908 | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.000.818 | ||
| Номер ЕС |
| ||
| MeSH | Тетраметилсилан | ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 2749 | ||
| |||
| |||
| Характеристики | |||
| C4ЧАС12Si | |||
| Молярная масса | 88.225 г · моль−1 | ||
| Внешность | Бесцветная жидкость | ||
| Плотность | 0,648 г см−3 | ||
| Температура плавления | -99 ° С (-146 ° F, 174 К) | ||
| Точка кипения | От 26 до 28 ° C (от 79 до 82 ° F, от 299 до 301 K) | ||
| Растворимость | органические растворители | ||
| Структура | |||
| Тетраэдр на углероде и кремнии | |||
| 0 Д | |||
| Опасности | |||
Классификация ЕС (DSD) (устарело) | |||
| R-фразы (устарело) | R12 | ||
| S-фразы (устарело) | S16, S3 / 7, S33, S45 | ||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | −28 - −27 ° С | ||
| Родственные соединения | |||
Родственные силаны | Силан Тетрабромид кремния | ||
Родственные соединения | Неопентан | ||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
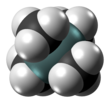
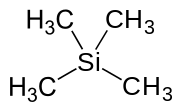
Тетраметилсилан (сокращенно ТМС) это кремнийорганическое соединение с формула Si (CH3)4. Это простейший тетраорганосилан. Как все силаны каркас ТМС тетраэдрический. TMS - это строительный блок в металлоорганическая химия но также находит применение в различных нишевых приложениях.
Синтез и реакция
ТМС является побочным продуктом производства метилхлорсиланов, SiCl.Икс(CH3)4−Икс, через прямой процесс реагирования метилхлорид с кремнием. Наиболее полезными продуктами этой реакции являются продукты для Икс = 1 (триметилсилилхлорид ), 2 (диметилдихлорсилан ) и 3 (метилтрихлорсилан ).[1]
ТМС подвергается депротонированию при лечении бутиллитий дать (H3C)3SiCH2Ли. Последний, триметилсилилметиллитий, является относительно распространенным алкилирующий агент.
В химическое осаждение из паровой фазы, ТМС является предшественником диоксид кремния или же Карбид кремния в зависимости от условий нанесения.
Использование в ЯМР-спектроскопии
Тетраметилсилан - принятый внутренний стандарт для калибровки химический сдвиг за 1ЧАС, 13C и 29Si ЯМР-спектроскопия в органических растворителях (где ТМС растворим). В воде, где он не растворим, натриевые соли DSS, 2,2-диметил-2-силапентан-5-сульфонат, используются вместо них. Из-за его высокой летучести ТМС легко испаряется, что удобно для извлечения образцов, проанализированных с помощью ЯМР-спектроскопии.[2]
Поскольку все двенадцать атомов водорода в молекуле тетраметилсилана эквивалентны, ее 1Спектр ЯМР 1Н состоит из синглета.[3]Химический сдвиг этого синглета обозначается как δ 0, а все остальные химические сдвиги определяются относительно него. Большинство соединений, изученных 1Спектроскопия ЯМР 1Н поглощает слабое поле сигнала ТМС, поэтому обычно нет интерференции между стандартом и образцом. Точно так же все четыре атома углерода в молекуле тетраметилсилана эквивалентны.[3]В полностью развязанном 13В спектре ЯМР 13С углерод в тетраметилсилане выглядит как синглет, что позволяет легко идентифицировать. Химический сдвиг этого синглета также должен быть равен δ 0 в 13Спектр C и все остальные химические сдвиги определяются относительно него.
Коммерческие растворители для ЯМР часто поставляются без ТМС. 1Спектры ЯМР 1Н могут быть откалиброваны по остаточному проирорастворителю (например, оставшимся примерно 0,1% недейтерированного хлороформа в промышленных CDCl3 ). Поскольку дейтерий не наблюдается в 1H ЯМР, можно отчетливо наблюдать остаточные сигналы про-растворителя. За 13При работе с ЯМР 13С спектры обычно калибруются по пику дейтерированного растворителя. Например, дейтерированный хлороформ показывает тройку одинаковой высоты на δ 77.0.[4]Триплет объясняется применением 2nI +1 правило; в случае дейтерия я = 1. Таблицы и диаграммы химических сдвигов для различных типов ЯМР-спектроскопии часто предоставляются поставщиками растворителей для ЯМР. Также была проведена работа по составлению подробных таблиц химических сдвигов растворителей и примесей.[5][6]
Рекомендации
- ^ Эльшенбройх, К. (2006). Металлоорганические соединения. Вайнхайм: Wiley-VCH. ISBN 978-3-527-29390-2.
- ^ Mohrig, Jerry R .; Норинг Хаммонд, Кристина; Шац, Пол Ф. (январь 2006 г.). Методы органической химии (Google Книги выдержка). С. 273–274. ISBN 978-0-7167-6935-4.
- ^ а б Теория ЯМР - химический сдвиг
- ^ Теория ЯМР - Растворители для ЯМР спектроскопии
- ^ Gottlieb, Hugo E .; Котляр, Вадим; Нудельман, Авраам (1997). «Химические сдвиги ЯМР обычных лабораторных растворителей как следовые примеси». Журнал органической химии. 62 (21): 7512–7515. Дои:10.1021 / jo971176v. PMID 11671879.
- ^ Фулмер, Грегори Р .; Миллер, Александр Дж. М .; Шерден, Натаниэль Х .; Gottlieb, Hugo E .; Нудельман, Авраам; Штольц, Брайан М .; Bercaw, John E .; Гольдберг, Карен И. (2010). «Химические сдвиги ЯМР следов примесей: обычные лабораторные растворители, органические вещества и газы в дейтерированных растворителях, имеющие отношение к химик-металлоорганикам» (PDF). Металлоорганические соединения. 29 (9): 2176–2179. Дои:10.1021 / om100106e.