Вспомогательное устройство для желудочков - Ventricular assist device
| Вспомогательное устройство для желудочков | |
|---|---|
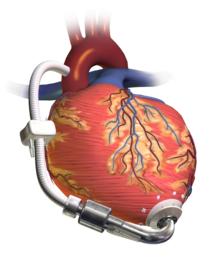
 Вспомогательное устройство для левого желудочка (LVAD), перекачивающее кровь из левого желудочка в аорту, подключенное к выносному блоку управления и аккумуляторной батарее. | |
| MedlinePlus | 007268 |
А желудочковое вспомогательное устройство (VAD) является электромеханический устройство для поддержки сердечного кровообращения, которое используется для частичной или полной замены функции вышедшего из строя сердце. Функция VAD отличается от функции искусственные кардиостимуляторы; некоторые предназначены для краткосрочного использования, как правило, для пациентов, восстанавливающихся после инфаркт миокарда (сердечный приступ) и для пациентов, восстанавливающихся после операция на сердце; некоторые предназначены для длительного использования (от месяцев до лет до бесконечности), как правило, для пациентов, страдающих продвинутыми сердечная недостаточность.
VAD предназначены для оказания помощи правым желудочек (RVAD) или левый желудочек (LVAD), или для поддержки обоих желудочков (BiVAD). Тип применяемого желудочкового вспомогательного устройства зависит от типа основного сердечное заболевание, и от сопротивления легочной артерии, которое определяет рабочую нагрузку правого желудочка. Устройство помощи левому желудочку (LVAD) является наиболее распространенным устройством, применяемым к дефектному сердцу (в большинстве случаев этого достаточно; тогда правая сторона сердца часто может использовать сильно увеличенный кровоток), но когда Сопротивление легочной артерии высокое, тогда может потребоваться (дополнительное) вспомогательное устройство для правого желудочка (RVAD) для решения проблемы сердечного кровообращения. Если требуются и LVAD, и RVAD, обычно используется BiVAD, а не отдельные LVAD и RVAD.
Обычно долгосрочный VAD используется в качестве мост к трансплантации (BTT) - поддержание пациента живым, в достаточно хорошем состоянии и способностью ждать трансплантации сердца за пределами больницы. Другие «мосты» включают мост к кандидатуре, мост к решению и мост к выздоровлению. В некоторых случаях VAD являются также используется как назначенная терапия (DT). В этом случае пациенту не следует проводить трансплантацию сердца, а VAD - это то, что пациент будет использовать до конца своей жизни.[1][2]
VAD отличаются от искусственные сердца, которые предназначены для выполнения функции сердца и обычно требуют удаления сердца пациента.
Дизайн
Насосы
В насосы используемые в VADs можно разделить на две основные категории - пульсирующие насосы,[3] которые имитируют естественную пульсацию сердца, и насосы непрерывного потока.[4] Пульсирующие VAD используют поршневые насосы.[5][6][7] В некоторых пульсирующих насосах (которые используют сжатый воздух в качестве источника энергии)[8]) объем, занимаемый кровью, изменяется во время цикла откачки. Если насос находится внутри корпуса, необходима вентиляционная трубка для наружного воздуха.
VAD с непрерывным потоком меньше и более долговечны, чем с пульсирующим VAD.[9] Обычно они используют либо центробежный насос или осевой насос. Оба типа имеют центральный ротор с постоянными магнитами. Управляемые электрические токи, проходящие через катушки, содержащиеся в корпусе насоса, прикладывают силы к магнитам, которые, в свою очередь, вызывают вращение роторов. В центробежных насосах роторы имеют такую форму, чтобы ускорять кровь по окружности и тем самым заставлять ее двигаться к внешнему ободу насоса, тогда как в насосах с осевым потоком роторы имеют более или менее цилиндрическую форму с лопастями, которые имеют спиралевидную форму, вызывая кровь ускоряться в направлении оси ротора.[10]
Важной проблемой, связанной с насосами с непрерывным потоком, является способ подвески ротора. В ранних версиях использовались твердые подшипники; однако более новые насосы, некоторые из которых одобрены для использования в ЕС, используют либо Магнитная левитация ("маглев")[11][12][13] или гидродинамическая подвеска. Эти насосы содержат только одну движущуюся часть (ротор).
История

Первая система вспомогательного устройства левого желудочка (LVAD) была создана Доминго Лиотта в Медицинском колледже Бейлора в Хьюстоне в 1962 году. Первое вспомогательное устройство для левого желудочка (LVAD) было имплантировано в 1963 году Лиоттой и Э. Стэнли Кроуфорд. Первая успешная имплантация вспомогательного устройства для левого желудочка была завершена в 1966 году Лиоттой вместе с доктором . Майкл Э. Дебейки 37-летней женщине. Паракорпоральный (внешний) контур обеспечивал механическую поддержку в течение 10 дней после операции.[15] Первая успешная долгосрочная имплантация искусственного LVAD была проведена в 1988 г. Уильям Ф. Бернхард из Бостонская детская больница Медицинский центр и Thermedics, Inc. из Вобурна, Массачусетс, в рамках исследовательского контракта Национального института здравоохранения (NIH), который разработал HeartMate, вспомогательное устройство с электронным управлением. Это было профинансировано трехлетним контрактом на сумму 6,2 миллиона долларов США с больницей Thermedics and Children's Hospital, Бостон, Массачусетс, с Национальным институтом сердца, легких и крови, программой NIH.[16] Ранние VAD имитировали работу сердца, используя «пульсирующее» действие, при котором кровь поочередно всасывалась в насос из левого желудочка, а затем вытеснялась в аорту. К устройствам этого типа относится HeartMate IP LVAS, который был одобрен для использования в США Управление по контролю за продуктами и лекарствами (FDA) в октябре 1994 г. Эти устройства начали получать признание в конце 1990-х годов у кардиохирургов, включая Эрик Роуз, О. Х. Фрейзер и Мехмет Оз начали популяризировать идею о том, что пациенты могут жить вне больницы. Освещение в средствах массовой информации амбулаторных больных с VAD подчеркивает эти аргументы.[17]
Более поздние работы были сосредоточены на насосах непрерывного действия, которые можно условно разделить на центробежные насосы или насосы. осевой поток крыльчатка приводные насосы. Эти насосы имеют преимущество большей простоты, что приводит к меньшим размерам и большей надежности. Эти устройства называются VAD второго поколения. Побочным эффектом является то, что у пользователя не будет пульс,[18]или что интенсивность пульса будет серьезно снижена.[19]
VAD третьего поколения подвешивают рабочее колесо в насосе с помощью гидродинамической или электромагнитной подвески, что устраняет необходимость в подшипниках и сокращает количество движущихся частей до одной.[нужна цитата ]
Другая технология, проходящая клинические испытания, - это использование чрескожной индукции для питания и управления устройством, а не чрескожные кабели. Помимо очевидного косметического преимущества, это снижает риск заражения и, как следствие, необходимость принятия профилактических мер. Пульсирующий насос, использующий эту технологию, имеет одобрение CE Mark и проходит клинические испытания для одобрения FDA США.[нужна цитата ]
Совершенно другой подход на ранних стадиях развития - использование надувной манжеты вокруг аорты. Раздувание манжеты сжимает аорту, а сдувание манжеты позволяет аорте расширяться - по сути, аорта становится вторым левым желудочком. Предлагаемое усовершенствование заключается в использовании скелетных мышц пациента, приводимых в движение кардиостимулятор, чтобы привести это устройство в действие, что сделало бы его по-настоящему автономным. Однако аналогичная операция (кардиомиопластика ) был опробован в 1990-х годах с неутешительными результатами. В любом случае, он имеет существенные потенциальные преимущества, так как позволяет избежать необходимости оперировать само сердце и избежать любого контакта между кровью и устройством. Этот подход предполагает возврат к пульсирующему потоку.[нужна цитата ]
Питер Хоутон был самым долго выжившим получателем VAD для постоянного использования. В июне 2000 года он получил экспериментальный LVAD Jarvik 2000. С тех пор он совершил благотворительную прогулку длиной 91 милю, опубликовал две книги, много читал лекции, совершал пешие прогулки по швейцарским Альпам и американскому западу, летал на сверхлегком самолете и путешествовал. широко по всему миру. Он умер от острая травма почек в 2007 году в возрасте 69 лет.[20][21]
Исследования и результаты
Недавние улучшения
- В июле 2009 года в Англии хирурги удалили донорское сердце, которое было имплантировано ребенку рядом с ее родным сердцем после того, как ее родное сердце восстановилось. Этот метод предполагает, что механическое вспомогательное устройство, такое как LVAD, может отнять часть или всю работу от собственного сердца и дать ему время на заживление.[22]
- В июле 2009 года результаты 18-месячного наблюдения в рамках клинического исследования HeartMate II показали, что непрерывный LVAD обеспечивает эффективную гемодинамическую поддержку в течение как минимум 18 месяцев у пациентов, ожидающих трансплантации, с улучшенным функциональным статусом и качеством жизни.[23]
- В июле 2009 года университетская больница Гейдельберга сообщила, что туда был имплантирован первый HeartAssist5, известный как современная версия DeBakey VAD. HeartAssist5 весит 92 грамма, изготовлен из титана и пластика и служит для перекачивания крови из левого желудочка в аорту.[24]
- В настоящее время проходит фаза 1 клинических испытаний (по состоянию на август 2009 г.), в которой участвуют пациенты с шунтированием коронарной артерии и пациенты с сердечной недостаточностью в терминальной стадии, у которых есть вспомогательное устройство для левого желудочка. Испытание включает тестирование пластыря под названием Anginera, который содержит клетки, выделяющие гормоноподобные факторы роста, стимулирующие рост других клеток. В пластырь засевают клетки сердечной мышцы, а затем имплантируют в сердце с целью заставить мышечные клетки начать общаться с естественными тканями таким образом, чтобы обеспечить регулярные сокращения.[25][26]
- В сентябре 2009 года новозеландское новостное издание Stuff сообщило, что еще через 18 месяцев-два года новое беспроводное устройство будет готово к клиническим испытаниям, которое будет обеспечивать питание VAD без прямого контакта. В случае успеха это может снизить вероятность заражения в результате прохождения кабеля питания через кожу.[27]
- В Национальные институты здоровья (NIH) выделил грант в размере 2,8 миллиона долларов на разработку полного искусственного сердца без пульса с использованием двух VAD. Микромед, изначально созданный Майкл Дебейки и Джордж Нун. Грант был продлен на второй год исследований в августе 2009 года. Полное искусственное сердце было создано с использованием двух HeartAssist5 VAD, при этом один VAD качает кровь по всему телу, а другой - в легкие и из легких.[28]
- HeartWare International в августе 2009 года объявила, что она превзошла 50 имплантатов своей системы помощи желудочков HeartWare в своем клиническом испытании ADVANCE, одобренном FDA исследовании IDE. Цель исследования - оценить систему как мост к трансплантации для пациентов с терминальной сердечной недостаточностью. Исследование «Оценка системы HeartWare LVAD для лечения тяжелой сердечной недостаточности» - это многоцентровое исследование, которое началось в мае 2009 года.[29][30]
- 27 июня 2014 года Ганноверская медицинская школа в Ганновере, Германия, под руководством профессора Axel Haverich, доктора медицины, профессора Акселя Хавериха, руководителя отделения кардиоторакальной, трансплантационной и сосудистой хирургии, и хирурга Яна Шмитто, доктора медицины, доктора философии, установила первый человеческий имплант HeartMate III.[31]
- 21 января 2015 года в журнале American College of Cardiology было опубликовано исследование, в котором предполагается, что длительное использование LVAD может вызвать регенерацию сердца.[32] Это может объяснить феномен «моста к восстановлению», впервые описанный группой Якуба в NEJM в 2009 г. (см. Выше).[нужна цитата ]
- Бейсболист Рода Кэрью, занесенный в Зал славы, имел застойную сердечную недостаточность, и ему был установлен HeartMate II. Он боролся с ношением оборудования, поэтому он объединил усилия, чтобы предоставить наиболее полезную одежду для HeartMate II и HeartMate III.[33]
- В декабре 2018 года два клинических случая были выполнены в Казахстане, и полностью беспроводная система LVAD Jarvik 2000 в сочетании с Левит Кардио FiVAD (полностью имплантируемое желудочковое вспомогательное устройство) имплантировали людям. В Беспроводная передача энергии технология, основанная на технике, называемой копланарной передачей энергии (CET), которая способна передавать энергию от внешней передающей катушки к маленькой приемной катушке, которая имплантирована в человеческое тело. В ранней послеоперационной фазе операция CET была выполнена, как и ожидалось, у обоих пациентов, при которой была запитана помпа и поддерживалась зарядка аккумулятора для выполнения медицинских и медсестринских процедур. В Левит Кардио Система FiVAD с беспроводной технологией копланарной передачи энергии, которая снижает риск заражения за счет устранения трансмиссии, обеспечивая при этом успешную передачу энергии, позволяющую обеспечить существенную (примерно 6 часов) поддержку LVAD без обивки.[34]
Большинство VAD на рынке сегодня несколько громоздки. Самое маленькое устройство, одобренное FDA, HeartMate II, весит около 1 фунта (0,45 кг) и имеет размеры 3 дюйма (7,6 см). Это оказалось особенно важным для женщин и детей, для которых альтернативы были бы слишком большими.[35] По состоянию на 2017 год HeartMate III был одобрен FDA. Он меньше, чем его предшественник HeartMate II, и использует полное рабочее колесо на магнитной подвеске вместо подшипниковой системы с чашкой и шариком, как в HeartMate II.[36]
Одно устройство, VentrAssist, получило одобрение CE Mark для использования в ЕС и начало клинические испытания в США. По состоянию на июнь 2007 года эти насосы были имплантированы более чем 100 пациентам. В 2009 году Ventracor был передан в руки администраторов из-за финансовых проблем, а позже в том же году был ликвидирован. Никакие другие компании не покупали эту технологию, поэтому устройство VentrAssist практически перестало функционировать. По состоянию на январь 2010 года около 30–50 пациентов во всем мире продолжают получать поддержку с помощью устройств VentrAssist.[нужна цитата ]
HeartWare HVAD работает аналогично VentrAssist, но намного меньше по размеру и не требует имплантации брюшного кармана. Устройство получило знак CE в Европе и одобрение FDA в США. Недавно было показано, что HeartWare HVAD можно имплантировать через ограниченный доступ без стернотомия.[37]
В небольшом количестве случаев вспомогательные устройства для левого желудочка в сочетании с лекарственной терапией позволили сердцу восстановиться в достаточной степени для того, чтобы устройство можно было удалить (эксплантированный).[1][2]
Основное исследование HeartMate II LVAD
Серия исследований с использованием HeartMate II LVAD оказалась полезной для определения жизнеспособности и рисков использования LVAD для промежуточной трансплантации и целевой терапии.
- Пилотное испытание HeartMate II LVAD началось в ноябре 2003 г. и включало 46 пациентов в 15 центрах. Результаты включали 11 пациентов, которым оказывали поддержку более одного года, и трех пациентов, которых поддерживали более двух лет.
- Сердцеед II основное испытание началось в 2005 году и включало оценку HeartMate II по двум показаниям: мост к трансплантации (BTT) и целевое лечение (DT), или долгосрочная, постоянная поддержка. Thoratec Corp. объявила, что это был первый раз, когда FDA одобрило клиническое испытание, чтобы включить оба показания в один протокол.[38][39][40]
- Многоцентровое исследование, проведенное в США с 2005 по 2007 год с участием 113 пациентов (из которых 100 сообщили об основных исходах), показало, что значительное улучшение функции было преобладающим через три месяца, а выживаемость составила 68% через двенадцать месяцев.[41]
- Основываясь на данных наблюдения за одним годом первых 194 пациентов, включенных в исследование, FDA одобрило HeartMate II для промежуточной трансплантации. Исследование предоставило клинические доказательства улучшения показателей выживаемости и качества жизни для широкого круга пациентов.[42][43]
- Данные восемнадцатимесячного наблюдения за 281 пациентом, которые либо достигли конечной точки исследования, либо завершили 18 месяцев послеоперационного наблюдения, показали улучшенную выживаемость, менее частые побочные эффекты и большую надежность с LVADS с непрерывным потоком по сравнению с устройствами с пульсирующим потоком. Из 281 пациента 157 пациентов перенесли трансплантацию, 58 пациентов продолжили лечение LVAD в своем теле, а 7 пациентов удалили LVAD, потому что их сердце восстановилось; остальные 56 погибли. Результаты показали, что пациенты Класс NYHA сердечной недостаточности значительно улучшилось после шести месяцев поддержки LVAD по сравнению с исходным уровнем до LVAD. Несмотря на то, что это испытание включало индикацию перехода от моста к трансплантату, результаты дают первые доказательства того, что LVAD с непрерывным потоком имеют преимущества с точки зрения долговечности и надежности для пациентов, получающих механическую поддержку для целевой терапии.[44]
- После одобрения FDA HeartMate II LVAD для перехода к трансплантации было проведено исследование после одобрения («реестр») для оценки эффективности устройства в коммерческих условиях. Исследование показало, что устройство улучшило результаты как по сравнению с другими видами лечения LVAD, так и с исходными пациентами. В частности, пациенты HeartMate II показали более низкий уровень креатинина, 30-дневная выживаемость была значительно выше и составила 96%, а 93% достигли успешных результатов (трансплантация, восстановление сердца или долгосрочное LVAD).[45]
HARPS
Исследование протокола восстановления Harefield (HARPS) - это клиническое испытание для оценки того, могут ли пациенты с тяжелой сердечной недостаточностью, которым требуется поддержка VAD, восстановить достаточную функцию миокарда, чтобы можно было удалить устройство (известное как эксплантация). HARPS сочетает LVAD (HeartMate XVE) с обычными пероральными лекарствами от сердечной недостаточности, за которыми следует новый агонист β2 кленбутерол. Это открывает возможность того, что некоторые пациенты с тяжелой сердечной недостаточностью могут отказаться от трансплантации сердца.[46]
На сегодняшний день 73% (11 из 15) пациентов, которые прошли режим комбинированной терапии, продемонстрировали достаточное выздоровление, чтобы позволить эксплантацию и избежать трансплантации сердца; отсутствие рецидива сердечной недостаточности у выживших пациентов составило 100% и 89% через один и четыре года после эксплантации, соответственно; средняя фракция выброса составила 64% через 59 месяцев после эксплантации; все пациенты относились к классу I по NYHA, при терапии кленбутеролом не сообщалось о значительных побочных эффектах.
ПОВТОР
Клиническое испытание REMATCH (рандомизированная оценка механической помощи при лечении застойной сердечной недостаточности) началось в мае 1998 г. и проводилось до июля 2001 г. в 20 центрах трансплантации сердца в США. Исследование было разработано для сравнения долгосрочной имплантации вспомогательных устройств для левого желудочка с оптимальным медицинским лечением пациентов с сердечной недостаточностью в терминальной стадии, которым требуется, но не соответствует требованиям, для трансплантации сердца. В результате клинических результатов устройство получило одобрение FDA по обоим показаниям в 2001 и 2003 годах соответственно.[47]
Испытание продемонстрировало улучшение двухлетней выживаемости на 81% среди пациентов, получавших HeartMate XVE, по сравнению с оптимальным медицинским лечением. Кроме того, исследование целевой терапии после исследования REMATCH продемонстрировало дополнительное улучшение на 17% (61% против 52%) годичной выживаемости пациентов, которым имплантировали VAD (HeartMate XVE), что повлияло на соответствующий выбор. кандидатов и сроков имплантации VAD.
Испытание, проведенное в 2001 г. Д-р Эрик А. Роуз и группа исследования REMATCH с пациентами с застойной сердечной недостаточностью, которые не подходили для трансплантации, показала выживаемость через два года в 23% для тех, кому имплантировали LVAD, по сравнению с 8% для тех, кто лечился лекарствами. Двумя основными осложнениями имплантации VAD были инфекция и механический отказ (см. Ниже).
Согласно ретроспективному когортному исследованию, сравнивающему пациентов, получавших вспомогательное устройство для левого желудочка, и инотропную терапию в ожидании трансплантации сердца, у группы, получавшей LVAD, улучшились клинические и метаболические функции во время трансплантации с лучшим кровяным давлением, натрием, азотом мочевины крови, и креатинин. После трансплантации 57,7% группы инотропа имели почечная недостаточность против 16,6% в группе LVAD; 31,6% группы инотропов имели правожелудочковую недостаточность по сравнению с 5,6% в группе LVAD; а выживаемость без событий составила 15,8% в группе инотропа по сравнению с 55,6% в группе LVAD.[48]
Осложнения и побочные эффекты
Кровотечение является наиболее частым ранним послеоперационным осложнением после имплантации или эксплантации LVAD, требуя повторной операции почти у 60% реципиентов.[49][50] Последствия массивных переливаний крови огромны и включают инфекцию, легочную недостаточность, увеличение затрат, правожелудочковую недостаточность, аллосенсибилизацию и передачу вируса, некоторые из которых могут оказаться фатальными или помешать трансплантации.[50] Когда происходит кровотечение, оно влияет на годовую смертность по Каплан-Мейеру.[49] Помимо сложности популяции пациентов и сложности этих процедур, способствующих кровотечению, сами устройства могут способствовать тяжелой коагулопатии, которая может возникнуть при имплантации этих устройств.[51]
Поскольку использование устройств обычно приводит к тому, что кровь течет по небиологической поверхности, кровь предрасполагается к свертывание, есть потребность в антикоагулянт меры. Одно устройство, HeartMate XVE, имеет биологическую поверхность, полученную из фибрин и не требует длительной антикоагуляции (кроме аспирина); К сожалению, эта биологическая поверхность может также предрасполагать пациента к инфекции из-за избирательного сокращения определенных типов лейкоцитов.[52]
Новые конструкции VAD, которые сейчас одобрены для использования в Европейском сообществе и проходят испытания для утверждения FDA, почти устранили механические поломки.[нужна цитата ]
Сложно измерить артериальное давление у пациентов с LVAD, используя стандартный мониторинг артериального давления, и в настоящее время его измеряют с помощью Допплерография в амбулаторные больные и инвазивный артериальное давление мониторинг в стационарные пациенты.[53]
Инфекция, связанная с VAD, может быть вызвана большим количеством различных организмов:[54]
- Грамположительные бактерии (Стафилококки, особенно Staph. aureus, Энтерококки )
- Грамотрицательные бактерии (Синегнойная палочка, Энтеробактер виды Клебсиелла виды)
- Грибы, особенно Candida разновидность
Лечение инфекции, связанной с VAD, чрезвычайно сложно, и многие пациенты умирают от инфекции, несмотря на оптимальное лечение. Первоначальное лечение должно проводиться антибиотиками широкого спектра действия, но необходимо приложить все усилия для получения подходящих образцов для посева. Окончательное решение относительно лечения антибиотиками должно быть основано на результатах микробиологических культур.[нужна цитата ]
Другие проблемы включают иммуносупрессия, свертывание крови в результате инсульта и кровотечение, вызванное антикоагулянтной терапией. Некоторые из полиуретан компоненты, используемые в устройствах, вызывают удаление части иммунные клетки при контакте с ними крови. Это предрасполагает пациента к грибковый и немного вирусный инфекции, требующие соответствующих профилактическая терапия.[55]
Учитывая множество рисков и изменений образа жизни, связанных с имплантатами вспомогательного желудочкового устройства,[56] Важно, чтобы потенциальные пациенты были проинформированы до принятия решения.[57] В дополнение к консультациям врача доступны различные интернет-ресурсы, ориентированные на пациентов, которые помогают в обучении пациентов.[58][59]
Список имплантируемых устройств VAD
Этот раздел должен быть обновлено. (Апрель 2015 г.) |
Это неполный список, который может никогда не быть полным.
Упомянутые дополнения приветствуются
| Устройство | Производитель | Тип | Статус утверждения по состоянию на июль 2010 г. |
|---|---|---|---|
| HeartAssist5 | ReliantHeart | Непрерывный поток приводится в движение ротором с осевым потоком. | Разрешено к применению в Европейском Союзе. Детская версия одобрена FDA для использования детьми в США. Проходит клинические испытания в США на одобрение FDA. |
| Новакор | Мировое Сердце | Пульсирующий. | Был одобрен для использования в Северной Америке, Европейском Союзе и Японии. Сейчас не существует и больше не поддерживается производителем. (Приобретение HeartWare завершено в августе 2012 г.) |
| HeartMate XVE | Thoratec | Пульсирующий | Одобрение FDA для BTT в 2001 г. и DT в 2003 г. Обозначение CE. Сейчас редко используется из-за проблем с надежностью. |
| HeartMate II | Торатек | Постоянный осевой поток с приводом от ротора, шариковые и чашки подшипников | Одобрено для использования в Северной Америке и ЕС. Знак CE авторизован. Одобрение FDA для BTT в апреле 2008 г. Недавно одобрено FDA в США для целевой терапии (по состоянию на январь 2010 г.). |
| HeartMate III | Thoratec | Непрерывный поток приводится в движение осевым ротором с магнитной подвеской. | Основные испытания HeartMate III начались в 2014 г. и поддерживаются CarewMedicalWear. Одобрение FDA для BTT в 2017 г. |
| Incor | Берлинское сердце | Непрерывный поток приводится в движение осевым ротором с магнитной подвеской. | Разрешено использовать в Европейском Союзе. Используется для получения разрешений на гуманитарные нужды в индивидуальном порядке в США. Начал клинические испытания в США в 2009 году. |
| Excor Pediatric | Берлинское сердце | Внешнее мембранное насосное устройство предназначено для детей. | Разрешено к использованию в Европейском Союзе. FDA предоставило США исключение по использованию гуманитарных устройств в декабре 2011 года. |
| Ярвик 2000 | Ярвик Сердце | Осевой ротор непрерывного действия на керамических подшипниках. | В настоящее время используется в США в качестве моста к пересадке сердца в рамках клинических исследований, одобренных FDA. В Европе Jarvik 2000 получил сертификат CE Mark как для мостовидных протезов, так и для пожизненного использования. В настоящее время разрабатывается дочерняя версия. |
| MicroMed DeBakey VAD | MicroMed | Непрерывный поток приводится в действие осевым ротором на керамических подшипниках. | Разрешено к применению в Европейском Союзе. Детская версия одобрена FDA для использования детьми в США. Проходит клинические испытания в США на одобрение FDA. |
| VentrAssist | Вентракор[60] | Непрерывный поток приводится в движение центробежным ротором с гидродинамической подвеской. | Одобрено для использования в Европейском Союзе и Австралии. Компания объявила о банкротстве, в то время как клинические испытания для утверждения FDA продолжались в 2009 году. В настоящее время компания распущена, а интеллектуальная собственность продана Thoratec. |
| MTIHeartLVAD | www.mitiheart.com | Непрерывный поток приводится в движение центробежным ротором с магнитной подвеской. | В настоящее время проходит испытания на животных, недавно успешно завершенный 60-дневный имплантат теленка. |
| C-Pulse (теперь «Аквадекс») | Солнечное сердце (теперь «Решения CHF») | Пульсирующий, приводится в действие надувной манжетой вокруг аорты. | В настоящее время имеется в продаже |
| HVAD | HeartWare | Миниатюрный аппарат «третьего поколения» с центробежным кровотоком и ротором с гидромагнитной подвеской, который может быть размещен в перикардиальном пространстве. | Получен знак CE для распространения в Европе, январь 2009 г. Получено одобрение FDA в США, ноябрь 2012 г. Начато исследование BTT в США в октябре 2008 г. (завершено в феврале 2010 г.) и исследование DT в США в августе 2010 г. (регистрация завершена в мае 2012 г.). Одобрение FDA для BTT в 2012 г. и DT в 2017 г. |
| МВАД | HeartWare | Помпа HeartWare MVAD - это миниатюрное желудочковое вспомогательное устройство, находящееся на стадии разработки, примерно треть размера помпы HeartWare HVAD. | HeartWare завершила исследования GLP (сентябрь 2011 г.). |
| DuraHeart | Терумо | Центробежный насос с магнитной подвеской. | Сертификат CE одобрен, испытания FDA США продолжаются по состоянию на январь 2010 г. |
| Thoratec PVAD (Паракорпоральное желудочковое вспомогательное устройство) | Thoratec | Пульсирующая система включает три основных компонента: насос крови, канюли и пневматический привод (консоль с двойным приводом или портативный драйвер VAD). | Знак CE авторизован. Получил одобрение FDA для BTT в 1995 году и для восстановления после кардиотомии (операции на открытом сердце) в 1998 году. |
| IVAD - имплантируемое желудочковое вспомогательное устройство | Торатек | Пульсирующая система включает три основных компонента: насос крови, канюли и пневматический привод (консоль с двойным приводом или портативный драйвер VAD). | Знак CE авторизован. Получено одобрение FDA для BTT в 2004 году. Разрешено только для внутреннего имплантата, но не для паракорпорального имплантата из-за проблем с надежностью. |
| FiVAD | Левит Кардио | Универсальная беспроводная система для LVAD. Дайте пациентам 6 часов свободы | Устройство для исследования, испытание 2 пациентов в декабре 2018 г. Ярвик 2000 LVAD в Астане от проф. Пя.[34] |
Смотрите также
Рекомендации
- ^ а б Биркс, EJ; Тэнсли, PD; Харди, Дж; и другие. (2006). "Вспомогательное устройство левого желудочка и лекарственная терапия для лечения сердечной недостаточности". Медицинский журнал Новой Англии. 355 (18): 1873–1884. Дои:10.1056 / NEJMoa053063. PMID 17079761.
- ^ а б "Первая программа VentrAssist Heart Recovery показана на национальном телевидении". Ventracor.com. 19 октября 2006 г.
- ^ Файдек, Б; Krzysztof, J (2–5 сентября 2014 г.). «Система автоматического управления желудочковым вспомогательным устройством». 19-я Международная конференция по методам и моделям в автоматизации и робототехнике (MMAR): 874–879. Дои:10.1109 / MMAR.2014.6957472. ISBN 978-1-4799-5081-2. S2CID 13070912.
- ^ Шульман, АР; Мартенс, Т.П .; Christos, PJ; и другие. (2007). «Сравнение инфекционных осложнений между вспомогательными устройствами левого желудочка с непрерывным и пульсирующим потоком». Журнал торакальной и сердечно-сосудистой хирургии. 133 (3): 841–842. Дои:10.1016 / j.jtcvs.2006.09.083. PMID 17320612.
- ^ "Панель A показывает пульсирующий поток первого поколения слева ve - Open-i". openi.nlm.nih.gov. Получено 23 апреля 2018.
- ^ "404 Страница не найдена". ResearchGate. Получено 23 апреля 2018. Cite использует общий заголовок (Помогите)
- ^ «Компоненты пульсирующего насоса SynCardia TAH» (PDF). syncardia.com. Получено 23 апреля 2018.
- ^ «У HeartMate XVE тоже есть вентиляционная линия, несмотря на то, что он работает от батареи» (PDF). aldmd.com. Получено 23 апреля 2018.
- ^ Убой, MS; Pagani, FD; Роджерс, JG; и другие. (2010). «Клиническое управление вспомогательными устройствами для левого желудочка с непрерывным потоком при тяжелой сердечной недостаточности». Журнал трансплантации сердца и легких. 29 (4): S1–39. Дои:10.1016 / j.healun.2010.01.011. PMID 20181499.
- ^ Фукамачи, Кийо; Смедира, Николай (август 2005 г.). «Меньшие, безопасные, полностью имплантируемые LVAD: факт или фантазия?». Обзор текущего журнала Американского колледжа кардиологии. 14 (8): 40–42. Дои:10.1016 / j.accreview.2005.06.001.
- ^ Умно, Фрэнк. «Сердечный насос с магнитной левитацией, имплантированный первому пациенту в США». «Кардиология сегодня». Октябрь 2008 г.
- ^ Пай, CN; Шинши, Т; Асама, Дж; и другие. (2008). «Разработка компактного центробежного перфузионного насоса Maglev, заключенного в титановый корпус». Журнал усовершенствованного механического проектирования, систем и производства. 2 (3): 343–355. Дои:10.1299 / jamdsm.2.343.
- ^ Хоши, Н; Шинши, Т; Такатани, S (2006). «Кровяные насосы третьего поколения с механическими бесконтактными магнитными подшипниками». Искусственные органы. 30 (5): 324–338. Дои:10.1111 / j.1525-1594.2006.00222.x. PMID 16683949.
- ^ «Доктор Дентон Кули и доктор Майкл Э. Дебейки: рок-звезды хьюстонской медицины». Хьюстон Хроникл. 3 апреля 2014 г.
- ^ Кирклин, JK; Нафтел, округ Колумбия (сентябрь 2008 г.). «Механическая поддержка кровообращения: эволюция терапии». Циркуляция: сердечная недостаточность. 1 (3): 200–5. Дои:10.1161 / circheartfailure.108.782599. ЧВК 3437761. PMID 19808290.
- ^ «Объявлен прогресс Heart Pump - многообещающий шаг в технологии искусственного сердца». Детский сегодня (Март): 1,5. 19 марта 1988 г.
- ^ Электрическое сердце. PBS.
- ^ Дэн Баум."Нет пульса: как врачи заново изобрели человеческое сердце" Популярная наука, 2012.
- ^ "Часто задаваемые вопросы по VAD". Медицинский центр Колумбийского университета. Цитата: «У пациента, которому имплантирован HeartMate II, обычно снижен пульс». Просмотрено 27 августа 2016 г.
- ^ "Первый пожизненный пациент". Ярвик Сердце. Архивировано из оригинал 21 ноября 2010 г.
- ^ Пациент установил мировой рекорд по продолжительности жизни с помощью устройства для кардиологической помощи. Техасский институт сердца. 6 июля 2007 г.
- ^ Мо, Томас (14 июля 2009 г.). «Трансплантат показывает репаративные возможности сердца». Лос-Анджелес Таймс.
- ^ Pagani, FD; Миллер, LW; Рассел, SD; и другие. (2009). «Расширенная механическая поддержка кровообращения с роторным вспомогательным устройством левого желудочка с непрерывным потоком». Журнал Американского колледжа кардиологии. 54 (4): 312–321. Дои:10.1016 / j.jacc.2009.03.055. PMID 19608028.
- ^ «Кардиохирурги Гейдельберга впервые в мире имплантируют новое устройство для сердечной помощи Дебейки». Науки. 17 августа 2009 г. Архивировано с оригинал 18 июля 2011 г.
- ^ Куинн, Дейл (4 августа 2009 г.). «Исследование VA: пластырь для лечения сердца». Аризона Дейли Стар. Архивировано из оригинал 7 августа 2009 г.
- ^ «Исследование ангины у пациентов, перенесших операцию по шунтированию коронарной артерии (АКШ)». ClinicalTrials.gov. Национальные институты здравоохранения США. 27 марта 2009 г.. Получено 15 сентября 2009.
- ^ Хантер, Тим (13 сентября 2009 г.). "Познакомьтесь с бионическим мужчиной киви". Стандарт Манавату.
- ^ «Грант в размере 2,8 миллиона долларов возобновлен на разработку искусственного сердца без пульса». BusinessWire. 6 августа 2009 г.
- ^ «Оценка системы HeartWare LVAD для лечения тяжелой сердечной недостаточности». Медицинский центр Джона Хопкинса. Май 2009 г.
- ^ «HeartWare International превосходит 50 имплантатов в США». Биомедицина. 20 августа 2009 г.
- ^ «Thoratec объявляет о первом человеческом имплантате HeartMate III и начале испытаний с маркировкой CE». Корпорация Торатек. 20 августа 2009 г. Архивировано с оригинал 7 октября 2014 г.
- ^ Canseco, Diana C .; Кимура, Ватару; Гарг, Соня; Мукерджи, Шибани; Бхаттачарья, Супарно; Абдисалаам, Салим; Дас, Сандип; Асайтамби, Арумугаме; Mammen, Pradeep P.A .; Садек, Хешам А. (2015). "Разгрузка желудочков человека вызывает пролиферацию кардиомиоцитов". Журнал Американского колледжа кардиологии. 65 (9): 892–900. Дои:10.1016 / j.jacc.2014.12.027. ЧВК 4488905. PMID 25618530.
- ^ "LVAD Wear". www.carewmedicalwear.com.
- ^ а б «Первое использование человеком беспроводной копланарной передачи энергии в сочетании с вспомогательным устройством для левого желудочка с непрерывным потоком». Трансплантация сердца и легких. 4 февраля 2019.
- ^ Богаев, Р; Чен, L; Рассел, SD; и другие. (2007). «Медицинские аспекты терминальной сердечной недостаточности: трансплантация и аппаратная терапия I, реферат 1762: новый вариант для женщин с тяжелой сердечной недостаточностью: результаты испытания моста HeartMate II с вспомогательным вспомогательным устройством для левого желудочка с непрерывным потоком к трансплантации». Тираж. II. Американская Ассоциация Сердца. 116: 372. Архивировано с оригинал 8 июня 2011 г.
- ^ https://www.thoratec.com/medical-professionals/vad-product-information/heartmate3/HeartMate3_PressKit-UK.pdf
- ^ Попов, А.Ф .; Хоссейни, MT; Зыч, Б; и другие. (2012). "Имплантация вспомогательного устройства левого желудочка HeartWare посредством двусторонней передней торакотомии". Летопись торакальной хирургии. 93 (2): 674–676. Дои:10.1016 / j.athoracsur.2011.09.055. PMID 22269746.
- ^ Бентон, Сьюзен (19 августа 2008 г.). «Информационный бюллетень по основным клиническим испытаниям HeartMate II» (PDF). Корпорация Торатек. Получено 10 сентября 2009.
- ^ Дьюи, Тодд (19 августа 2008 г.). "Основное испытание HeartMate II LVAS". Сердечно-легочный научно-исследовательский институт. Архивировано из оригинал 13 июля 2007 г.
- ^ Магер, Белинда (25 апреля 2008 г.). «FDA одобрило механический сердечный насос HeartMate II для пациентов с сердечной недостаточностью, ожидающих трансплантации органов». Нью-Йорк – пресвитерианская больница. Архивировано из оригинал 8 мая 2008 г.
- ^ Миллер, LW; Pagani, FD; Рассел, SD; и другие. (2007). «Использование устройства непрерывного потока у пациентов, ожидающих трансплантации сердца». Медицинский журнал Новой Англии. 357 (9): 885–896. Дои:10.1056 / NEJMoa067758. PMID 17761592.
- ^ Гэвин, Кара (23 апреля 2008 г.). «Волнующие времена для сердечных устройств в U-M». Система здравоохранения Мичиганского университета. Архивировано из оригинал 10 мая 2008 г.
- ^ «Thoratec HeartMate II LVAS - P060040». Управление по контролю за продуктами и лекарствами. 23 апреля 2008 г.. Получено 28 августа 2009.
- ^ Эйзен, HJ; Ханкинс, SR (2009). «Роторное вспомогательное устройство левого желудочка с непрерывным потоком». Журнал Американского колледжа кардиологии. 54 (4): 322–324. Дои:10.1016 / j.jacc.2009.04.028. PMID 19608029.
- ^ Starling, RC; Naka, Y; Бойл, AJ; и другие. (Август 2009 г.). «Результаты первичного исследования FDA после одобрения INTERMACS с вспомогательным устройством для левого желудочка с непрерывным потоком в качестве моста к трансплантации сердца». Журнал сердечной недостаточности. 15 (6): S46. Дои:10.1016 / j.cardfail.2009.06.252.
- ^ Миллер, Лесли; Ааронсон и Пагани (2008). «Исследование протокола восстановления Harefield для пациентов с рефрактерной хронической сердечной недостаточностью (HARPS)». ClinicalTrials.gov. Получено 3 августа 2009.
- ^ Роза, EA; Московиц, AJ; Пакер, М; и другие. (1999). «Исследование REMATCH: обоснование, дизайн и конечные точки. Рандомизированная оценка механической помощи для лечения застойной сердечной недостаточности». Летопись торакальной хирургии. 67 (3): 723–730. Дои:10.1016 / S0003-4975 (99) 00042-9. PMID 10215217.
- ^ Роджерс, JG; Батлер, Дж; Lansman, SL; и другие. (2007). «Хроническая механическая поддержка кровообращения у пациентов с инотропно-зависимой сердечной недостаточностью, которые не являются кандидатами на трансплантацию». Журнал Американского колледжа кардиологии. 50 (8): 741–747. Дои:10.1016 / j.jacc.2007.03.063. PMID 17707178.
- ^ а б Шаффер, Дж. М.; Arnaoutakis, GJ; Allen, JG; и другие. (2011). «Осложнения кровотечений и использование продуктов крови с имплантацией вспомогательного устройства левого желудочка». Летопись торакальной хирургии. 91 (3): 740–749. Дои:10.1016 / j.athoracsur.2010.11.007. PMID 21352991.
- ^ а б Goldstein, Daniel J .; Роберт Б. Бофорд (2003). «Вспомогательные устройства для левого желудочка и кровотечение: добавление оскорбления к травме». Летопись торакальной хирургии. 75 (6): S42–7. Дои:10.1016 / с0003-4975 (03) 00478-8. PMID 12820734.
- ^ Спаниер, Талия; Оз, М; Левин, H; и другие. (1996). «Активация коагуляции и фибринолитических путей с помощью вспомогательных устройств левого желудочка». Журнал торакальной и сердечно-сосудистой хирургии. 112 (4): 1090–1097. Дои:10.1016 / s0022-5223 (96) 70111-3. PMID 8873737.
- ^ Samuels, LE; Kohout, J; Казанова-Гош, Э; и другие. (2008). «Аргатробан как первичный или вторичный послеоперационный антикоагулянт у пациентов, которым имплантированы вспомогательные желудочковые устройства». Летопись торакальной хирургии. 85 (5): 1651–1655. Дои:10.1016 / j.athoracsur.2008.01.100. PMID 18442558.
- ^ Кастанья, Франческо; Stöhr, Эрик Дж .; Пинсино, Альберто; Кокрофт, Джон Р.; Уилли, Джошуа; Решад Гаран, А .; Топкара, Вели К .; Коломбо, Паоло К.; Юзефпольская, Мелана; Макдоннелл, Барри Дж. (2017). «Уникальное артериальное давление и пульсация пациентов с LVAD: текущие проблемы и будущие возможности». Текущие отчеты о гипертонии. 19 (10): 85. Дои:10.1007 / s11906-017-0782-6. ISSN 1522-6417. ЧВК 5645430. PMID 29043581.
- ^ Гордон, Р.Дж.; Quagliarello, B; Лоуи, ФД (2006). «Инфекции, связанные с вспомогательными желудочковыми устройствами». Ланцетные инфекционные болезни. 6 (7): 426–37. Дои:10.1016 / S1473-3099 (06) 70522-9. PMID 16790383.
- ^ Холман, WL; Rayburn, BK; Макгиффин, округ Колумбия; и другие. (2003). «Инфекция в желудочковых вспомогательных устройствах: профилактика и лечение». Летопись торакальной хирургии. 75 (6 Прил.): S48 – S57. Дои:10.1016 / S0003-4975 (03) 00479-X. PMID 12820735.
- ^ Marcuccilli, L; Касида, Дж; Питерс, РМ (2013). «Модификация самооценки у пациентов с вспомогательным устройством левого желудочка: начальное исследование» (PDF). Журнал клинического сестринского дела. 22 (2456–64): 2456–64. Дои:10.1111 / j.1365-2702.2012.04332.x. HDL:2027.42/99069. PMID 23506318.
- ^ Mcillvennan, CK; Аллен, Луизиана; Nowels, C; Брике, А; Кливленд, JC; Мэтлок, ДД (2014). «Принятие решения о назначении терапии вспомогательными устройствами для левого желудочка:« не было выбора »против« Я очень много думал об этом »"". Циркуляция: качество и результаты сердечно-сосудистой системы. 7 (3): 374–80. Дои:10.1161 / CIRCOUTCOMES.113.000729. ЧВК 4081474. PMID 24823949.
- ^ Яковетто, MC; Мэтлок, DD; Mcillvennan, CK; и другие. (2014). «Образовательные ресурсы для пациентов, рассматривающих возможность использования вспомогательного устройства для левого желудочка: перекрестный обзор Интернет-материалов, печатных и мультимедийных материалов». Циркуляция: качество и результаты сердечно-сосудистой системы. 7 (6): 905–11. Дои:10.1161 / CIRCOUTCOMES.114.000892. PMID 25316772.
- ^ Мэтлок, DD; Аллен, Луизиана; Томпсон, Дж. С.; Макилвеннан, СК (31 июля 2014 г.). «Устройство помощи при принятии решения для вспомогательного устройства левого желудочка (LVAD) для целевой терапии Устройство для пациентов с тяжелой сердечной недостаточностью» (PDF). Медицинский факультет Университета Колорадо.
- ^ Компания Ventracor была ликвидирована 3 июля 2009 года, в результате чего активы компании, включая ее интеллектуальную собственность, данные клинических испытаний, установки и оборудование, а также остаточные активы, будут выставлены на продажу.Бойд, Тони (13 июля 2009 г.). "Бессердечный". Деловой зритель. Получено 15 сентября 2009.
внешняя ссылка
- MyLVAD.com - небрендовый сайт с информацией о различных LVAD.
