Активатор (генетика) - Activator (genetics)
Транскрипционный активатор это белок (фактор транскрипции ) что увеличивает транскрипция гена или набора генов.[1] Активаторы считаются имеющими положительный контроль над экспрессией генов, поскольку они функционируют для обеспечения транскрипции генов и, в некоторых случаях, необходимы для того, чтобы транскрипция генов происходила.[1][2][3][4] Большинство активаторов ДНК-связывающие белки это привязано к усилители или же промотор-проксимальные элементы.[1] Сайт ДНК, связанный с активатором, называется «сайтом связывания активатора».[3] Часть активатора, которая осуществляет белок-белковые взаимодействия с общим аппаратом транскрипции, называется «активирующей областью» или «доменом активации».[1]
Большинство активаторов действуют путем связывания специфической последовательности с регуляторным участком ДНК, расположенным рядом с промоутер и осуществление белок-белковых взаимодействий с общим аппаратом транскрипции (РНК-полимераза и общие факторы транскрипции ), тем самым облегчая связывание общего аппарата транскрипции с промотором.[1][2][3][4] Другие активаторы способствуют транскрипции генов, заставляя РНК-полимеразу высвобождаться из промотора и двигаться вдоль ДНК.[2] Иногда РНК-полимераза может приостановиться вскоре после выхода из промотора; Активаторы также функционируют, позволяя этим «остановленным» РНК-полимеразам продолжать транскрипцию.[1][2]
Активность активаторов можно регулировать. У некоторых активаторов есть аллостерический сайт, и они могут функционировать только тогда, когда определенная молекула связывается с этим сайтом, что по существу включает активатор.[4] Посттрансляционные модификации активаторов также могут регулировать активность, увеличивая или уменьшая активность в зависимости от типа модификации и модифицируемого активатора.[1]
В некоторых клетках, обычно эукариотических, несколько активаторов могут связываться с сайтом связывания; эти активаторы имеют тенденцию к кооперативному связыванию и синергетическому взаимодействию.[1][2]
Структура
Белки-активаторы состоят из двух основных домены: а ДНК-связывающий домен который связывается с последовательностью ДНК, специфичной для активатора, и домен активации это функционирует, чтобы увеличить транскрипцию гена, взаимодействуя с другими молекулами.[1] ДНК-связывающие домены активатора бывают разных форм, включая спираль-поворот-спираль, цинковый палец, и лейциновая молния среди прочего.[1][2][3] Эти ДНК-связывающие домены специфичны для определенной последовательности ДНК, что позволяет активаторам включать только определенные гены.[1][2][3] Домены активации также бывают различных типов, которые классифицируются на основе аминокислотной последовательности домена, включая аланин -богатые, глутамин -богатые и кислые домены.[1] Эти домены не столь специфичны и имеют тенденцию взаимодействовать с множеством целевых молекул.[1]
Активаторы также могут иметь аллостерические сайты которые отвечают за включение и выключение самих активаторов.[4]
Механизм действия
Связывание активатора с регуляторными последовательностями
Внутри бороздок двойной спирали ДНК, функциональные группы пары оснований обнажены.[2] Последовательность ДНК, таким образом, создает уникальный образец поверхностных особенностей, включая области возможных водородная связь, ионная связь, а также гидрофобные взаимодействия.[2] Активаторы также имеют уникальные последовательности аминокислот с боковыми цепями, которые способны взаимодействовать с функциональными группами ДНК.[2][3] Таким образом, структура боковых цепей аминокислот, составляющих активаторный белок, будет комплементарна поверхностным особенностям конкретной регуляторной последовательности ДНК, с которой он был разработан, для связывания.[1][2][3] Комплементарные взаимодействия между аминокислотами белка-активатора и функциональными группами ДНК создают «точную» специфичность между активатором и его регуляторной последовательностью ДНК.[2]
Большинство активаторов связываются с большими канавками двойной спирали, так как эти области имеют тенденцию быть более широкими, но есть некоторые, которые будут связываться с малыми канавками.[1][2][3]
Сайты связывания активатора могут быть расположены очень близко к промотору или на расстоянии множества пар оснований.[2][3] Если регуляторная последовательность расположена далеко, ДНК будет зацикливаться (петля ДНК), чтобы связанный активатор взаимодействовал с аппаратом транскрипции в промоторном сайте.[2][3]
У прокариот несколько генов могут транскрибироваться вместе (оперон ), и, таким образом, контролируются одной и той же регуляторной последовательностью.[2] У эукариот гены обычно транскрибируются индивидуально, и каждый ген контролируется своими собственными регуляторными последовательностями.[2] Регуляторные последовательности, в которых связываются активаторы, обычно находятся выше промотора, но их также можно найти ниже по течению или даже внутри интроны у эукариот.[1][2][3]
Функции увеличения транскрипции генов
Связывание активатора с его регуляторной последовательностью способствует транскрипции гена за счет активации активности РНК-полимеразы.[1][2][3][4] Это осуществляется с помощью различных механизмов, таких как привлечение аппарата транскрипции к промотору и запуск РНК-полимеразы для продолжения элонгации.[1][2][3][4]
Набор персонала
Гены, контролируемые активаторами, требуют связывания активаторов с регуляторными сайтами, чтобы задействовать необходимый аппарат транскрипции в промоторной области.[1][2][3]
Активаторные взаимодействия с РНК-полимеразой в основном прямые у прокариот и непрямые у эукариот.[2] У прокариот активаторы имеют тенденцию вступать в контакт с РНК-полимеразой напрямую, чтобы помочь связать ее с промотором.[2] У эукариот активаторы в основном взаимодействуют с другими белками, и именно эти белки будут взаимодействовать с РНК-полимеразой.[2]
Прокариоты
У прокариот гены, контролируемые активаторами, имеют промоторы, которые сами по себе не могут прочно связываться с РНК-полимеразой.[2][3] Таким образом, белки-активаторы способствуют связыванию РНК-полимеразы с промотором.[2][3] Это делается с помощью различных механизмов. Активаторы могут изгибать ДНК, чтобы лучше экспонировать промотор, чтобы РНК-полимераза могла связываться более эффективно.[3] Активаторы могут вступать в прямой контакт с РНК-полимеразой и прикреплять ее к промотору.[2][3][4]
Эукариоты
У эукариот активаторы имеют множество различных молекул-мишеней, которые они могут рекрутировать, чтобы способствовать транскрипции генов.[1][2] Они могут задействовать другие факторы транскрипции и кофакторы которые необходимы для инициации транскрипции.[1][2]
Активаторы могут привлекать молекулы, известные как коактиваторы.[1][2] Эти молекулы-коактиваторы могут затем выполнять функции, необходимые для начала транскрипции, вместо самих активаторов, такие как модификации хроматина.[1][2]
ДНК у эукариот гораздо более конденсирована; таким образом, активаторы имеют тенденцию привлекать белки, которые способны реструктурировать хроматин, так что промотор становится более доступным для механизмов транскрипции.[1][2] Некоторые белки изменят расположение нуклеосомы вдоль ДНК, чтобы обнажить промоторный сайт (АТФ-зависимые комплексы ремоделирования хроматина ).[1][2] Другие белки влияют на связывание гистонов с ДНК через посттрансляционные модификации гистонов, позволяя ДНК, плотно заключенной в нуклеосомы, расшататься.[1][2]
Все эти привлеченные молекулы работают вместе, чтобы в конечном итоге привлечь РНК-полимеразу к промоторному сайту.[1][2]
Высвобождение РНК-полимеразы
Активаторы могут способствовать транскрипции генов, сигнализируя РНК-полимеразе о выходе за пределы промотора и продвижении вдоль ДНК, инициируя начало транскрипции.[2] Иногда РНК-полимераза может остановиться вскоре после начала транскрипции, и для высвобождения РНК-полимеразы из этого «остановленного» состояния требуются активаторы.[1][2] Существует множество механизмов высвобождения этих «остановившихся» РНК-полимераз. Активаторы могут действовать просто как сигнал для запуска непрерывного движения РНК-полимеразы.[2] Если ДНК слишком конденсирована, чтобы позволить РНК-полимеразе продолжать транскрипцию, активаторы могут привлекать белки, которые могут реструктурировать ДНК, чтобы удалить любые блоки.[1][2] Активаторы могут также способствовать привлечению факторов элонгации, которые необходимы РНК-полимеразе для продолжения транскрипции.[1][2]
Регулирование активаторов
Существуют различные способы регулирования активности самих активаторов, чтобы гарантировать, что активаторы стимулируют транскрипцию генов в соответствующее время и на соответствующих уровнях.[1] Активность активатора может увеличиваться или уменьшаться в ответ на стимулы окружающей среды или другие внутриклеточные сигналы.[1]
Активация белков-активаторов
Активаторы часто необходимо «включить», прежде чем они смогут способствовать транскрипции генов.[2][3][4] Активность активаторов контролируется способностью активатора связываться со своим регуляторным участком вдоль ДНК.[2][3][4] ДНК-связывающий домен активатора имеет активную и неактивную формы, которые контролируются связыванием молекул, известных как аллостерические эффекторы к аллостерическому сайту возбудителя.[4]
Активаторы в неактивной форме не связаны ни с какими аллостерическими эффекторами.[4] В неактивном состоянии активатор не может связываться со своей специфической регуляторной последовательностью в ДНК и, таким образом, не оказывает регулирующего воздействия на транскрипцию генов.[4]
Когда аллостерический эффектор связывается с аллостерическим сайтом активатора, происходит конформационное изменение ДНК-связывающего домена, которое позволяет белку связываться с ДНК и увеличивать транскрипцию гена.[2][4]
Посттрансляционные модификации
Некоторые активаторы способны подвергаться посттрансляционные модификации которые влияют на их активность в клетке.[1] Такие процессы как фосфорилирование, ацетилирование, и убиквитинирование среди прочего, было замечено, что они регулируют активность активаторов.[1] В зависимости от добавляемой химической группы, а также от природы самого активатора посттрансляционные модификации могут либо увеличивать, либо уменьшать активность активатора.[1] Например, было замечено, что ацетилирование увеличивает активность некоторых активаторов за счет таких механизмов, как увеличение аффинности связывания ДНК.[1] С другой стороны, убиквитинирование снижает активность активаторов, поскольку убиквитин маркирует белки для деградации после того, как они выполнили свои соответствующие функции.[1]
Синергия
У прокариот единственный белок-активатор способен способствовать транскрипции.[2][3] У эукариот обычно более одного активатора собирается в сайте связывания, образуя комплекс, который способствует транскрипции.[1][2] Эти активаторы связывают совместно на сайте связывания, что означает, что связывание одного активатора увеличивает сродство сайта к связыванию другого активатора (или в некоторых случаях другого регулятора транскрипции), что облегчает связывание нескольких активаторов на этом сайте.[1][2] В этих случаях активаторы взаимодействуют друг с другом. синергетически, что означает, что скорость транскрипции, достигаемая при совместной работе нескольких активаторов, намного выше, чем аддитивные эффекты активаторов, если бы они работали индивидуально.[1][2]
Примеры
Регулирование мальтозного катаболизма
Распад мальтоза в кишечная палочка контролируется активацией гена.[3] Гены, кодирующие ферменты, ответственные за катаболизм мальтозы, могут быть расшифрованы только в присутствии активатора.[3]
Активатор, контролирующий транскрипцию ферментов мальтозы, отключен в отсутствие мальтозы.[3] В неактивной форме активатор не может связываться с ДНК и способствовать транскрипции генов мальтозы.[3][4]
Когда мальтоза присутствует в клетке, она связывается с аллостерическим сайтом белка-активатора, вызывая конформационные изменения в ДНК-связывающем домене активатора.[3][4] Это конформационное изменение «включает» активатор, позволяя ему связываться со своей специфической регуляторной последовательностью ДНК.[3][4] Связывание активатора с его регуляторным сайтом способствует связыванию РНК-полимеразы с промотором и, таким образом, транскрипции, производя ферменты, необходимые для расщепления мальтозы, попавшей в клетку.[3]
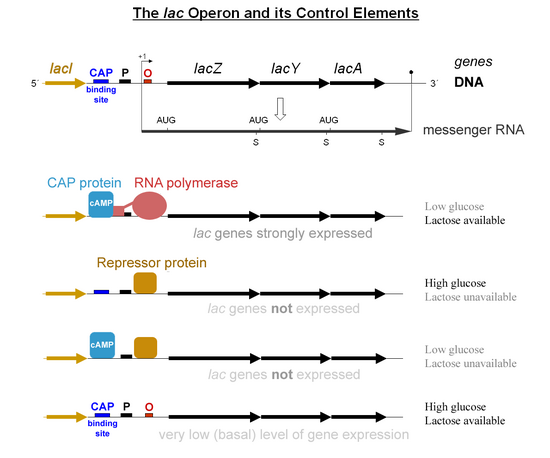
Регулирование Lac Operon
В протеин-активатор катаболита (CAP), иначе известный как белок рецептора цАМФ (CRP), активирует транскрипцию в лак оперон бактерии кишечная палочка.[5] Циклический аденозинмонофосфат (цАМФ) вырабатывается при голодании по глюкозе; эта молекула действует как аллостерический эффектор, который связывается с CAP и вызывает конформационные изменения, которые позволяют CAP связываться с участком ДНК, расположенным рядом с промотором lac.[5] Затем CAP осуществляет прямое межбелковое взаимодействие с РНК-полимеразой, которая привлекает РНК-полимеразу к промотору lac.[5]
Смотрите также
- Коактиватор (генетика)
- Глоссарий терминов экспрессии генов
- Оперон
- Промоутер (биология)
- Регулирование экспрессии генов
- Репрессор
- Фактор транскрипции
- Бактериальная транскрипция
- Эукариотическая транскрипция
Рекомендации
- ^ а б c d е ж грамм час я j k л м п о п q р s т ты v ш Икс у z аа ab ac объявление ае аф аг ах ай эй ак аль являюсь ан Ма, июнь (2011). «Активаторы транскрипции и механизмы активации». Белки и клетки. 2 (11): 879–888. Дои:10.1007 / s13238-011-1101-7. ISSN 1674-8018. ЧВК 4712173. PMID 22180087 - через PubMed.
- ^ а б c d е ж грамм час я j k л м п о п q р s т ты v ш Икс у z аа ab ac объявление ае аф аг ах ай эй ак аль являюсь ан ао ap водный ар в качестве в au Альбертс, Брюс; Джонсон, Александр; Льюис, Джулиан; Морган, Дэвид; Рафф, Мартин; Робертс, Кейт; Уолтер, Питер (2015). Молекулярная биология клетки (Шестое изд.). Нью-Йорк, Нью-Йорк: Наука о гирляндах. С. 373–392. ISBN 978-0-8153-4432-2. OCLC 887605755.
- ^ а б c d е ж грамм час я j k л м п о п q р s т ты v ш Икс у z аа ab Мэдиган, Майкл Т; Бендер, Келли С; Бакли, Дэниел Х; Саттли, Мэтью В.; Шталь, Дэвид А (2018). Биология микроорганизмов Брока (Пятнадцатое изд.). Нью-Йорк, Нью-Йорк: Пирсон. С. 174–179. ISBN 978-0-13-426192-8. OCLC 958205447.
- ^ а б c d е ж грамм час я j k л м п о п Гриффитс, Энтони Дж. Ф.; Гелбарт, Уильям М .; Миллер, Джеффри Х .; Левонтин, Ричард С. (1999). «Основы прокариотической регуляции транскрипции». Современный генетический анализ - через NCBI.
- ^ а б c Басби, Стив; Эбрайт, Ричард Х (1999-10-22). «Активация транскрипции белком-активатором катаболита (CAP)». Журнал молекулярной биологии. 293 (2): 199–213. Дои:10.1006 / jmbi.1999.3161. ISSN 0022-2836. PMID 10550204.
