Фосфат аммония - Ammonium phosphate
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК фосфат аммония | |
| Другие имена фосфат триаммония | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.030.709 |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
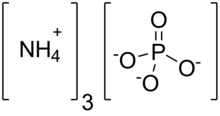
| (NH4)3PO4 | |
| Молярная масса | 149,09 г / моль |
| Внешность | Белый, четырехгранный кристаллы |
| 58,0 г / 100 мл (25 ° С) | |
| Опасности | |
| Пиктограммы GHS |  |
| Сигнальное слово GHS | Предупреждение |
| H302, H319 | |
| P264, P270, P280, P301 + 312, P305 + 351 + 338, P330, P337 + 313, P501 | |
| NFPA 704 (огненный алмаз) | |
| Термохимия | |
Станд. Энтальпия формирование (ΔжЧАС⦵298) | −1671,9 кДж / моль |
| Родственные соединения | |
Другой катионы | Тринатрийфосфат Фосфат калия |
Родственные соединения | Диаммоний фосфат Моноаммоний фосфат |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Фосфат аммония это аммоний соль ортофосфорной кислоты. Это очень нестабильное соединение с формула (NH4)3PO4. Из-за своей нестабильности он неуловим и не имеет коммерческой ценности. Родственная «двойная соль» (NH4)3PO4.(NH4)2HPO4 также признан, но слишком нестабилен для практического использования. Обе соли триаммония выделяют аммиак. В отличие от нестабильной природы солей триаммония, диаммонийфосфат (NH4)2HPO4 и моноаммониевая соль (NH4)ЧАС2PO4 представляют собой стабильные материалы, которые обычно используются в качестве удобрений для обеспечения растений фиксированным азотом и фосфором.[2]
Приготовление триаммонийфосфата
Фосфат триаммония можно получить в лаборатории путем обработки 85% фосфорной кислоты 30% раствором аммиака:[нужна цитата ]
- ЧАС3PO4 + 3 NH3 → (NH4)3PO4
(NH4)3PO4 бесцветное кристаллическое твердое вещество. Твердое вещество, имеющее запах аммиака, легко растворяется в воде. Соль превращается в гидрофосфат диаммония (NH4)2HPO4.
Смотрите также
Рекомендации
- ^ Лиде, Дэвид Р. (1998). Справочник по химии и физике (87 изд.). Бока-Ратон, Флорида: CRC Press. С. 4–42, 5–19. ISBN 978-0-8493-0594-8.
- ^ Шредтер, Клаус; Беттерманн, Герхард; Стаффель, Томас; Валь, Фридрих; Кляйн, Томас; Хофманн, Томас (2008). «Фосфорная кислота и фосфаты». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a19_465.pub3.
| Этот неорганический сложный –Связанная статья является заглушка. Вы можете помочь Википедии расширяя это. |

