Соединение интеркалирования графита - Graphite intercalation compound
Соединения интеркалирования графита (GIC) - сложные материалы, имеющие формулу CXм где ион Xп + или Xn− вставлен (вставленный ) между противоположно заряженными слоями углерода. Обычно m намного меньше 1.[1][2] Эти материалы представляют собой глубоко окрашенные твердые частицы, которые демонстрируют ряд электрических и окислительно-восстановительных свойств для потенциальных применений.
Подготовка и состав
Эти материалы получают путем обработки графита сильным окислителем или сильным восстановителем:
- С + м Х → СХм
Реакция обратимая.
Хост (графит) и гость X взаимодействуют посредством перенос заряда. Аналогичный процесс лежит в основе коммерческого литий-ионные батареи.
В смеси с прослоями графита не каждый слой обязательно занят гостями. В так называемом соединения стадии 1, графитовые слои и интеркалированные слои чередуются и в соединения стадии 2два графитовых слоя без промежуточного материала чередуются с прослоем. Фактический состав может варьироваться, и поэтому эти соединения являются примером нестехиометрический соединения. Принято указывать композицию вместе со сценой. Слои раздвигаются при включении гостевых ионов.
Примеры
Производные щелочных и щелочноземельных металлов

Одно из наиболее изученных соединений интеркаляции графита, KC8, готовится плавлением калий поверх графитового порошка. Калий поглощается графитом, и материал меняет цвет с черного на бронзовый.[3] Полученное твердое тело пирофорный.[4] Состав объясняется предположением, что расстояние от калия до калия в два раза больше расстояния между шестиугольниками в углеродном каркасе. Связь между слоями анионного графита и катионами калия ионная. Электропроводность материала больше, чем у α-графита.[4][5] KC8 это сверхпроводник с очень низкой критической температурой Tc = 0,14 К.[6] Отопление KC8 приводит к образованию ряда продуктов разложения по мере удаления атомов K:[нужна цитата ]
- 3 KC8 → KC24 + 2 тыс.
Через промежуточные звенья KC24 (синего цвета),[3] KC36, KC48, в конечном итоге соединение KC60 полученные результаты.
Стехиометрия MC8 наблюдается для M = K, Rb и Cs. Для более мелких ионов M = Li+, Sr2+, Ba2+, Европа2+, Yb3+, а Са2+, предельная стехиометрия - MC6.[6] Графит кальция CaC
6 получается путем погружения в высоко ориентированный пиролитический графит в жидком сплаве Li – Ca в течение 10 суток при 350 ° С. Кристаллическая структура CaC
6 принадлежит R3м космическая группа. Расстояние между слоями графита увеличивается при интеркалировании Са с 3,35 до 4,524 Å, а расстояние углерод-углерод увеличивается с 1,42 до 1,444 Å.
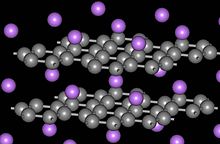
6
С барий и аммиак, катионы сольватируются, давая стехиометрию (Ba (NH3)2.5C10.9(этап 1)) или с цезий, водород и калий (CsC8· K2ЧАС4/3C8(этап 1)).
В отличие от других щелочных металлов, количество интеркаляции Na очень мало. Квантово-механические расчеты показывают, что это происходит из довольно общего явления: среди щелочных и щелочноземельных металлов Na и Mg обычно имеют самую слабую химическую связь с данным субстратом по сравнению с другими элементами той же группы периодической таблицы.[7] Это явление возникает из-за конкуренции между трендами энергии ионизации и взаимодействием иона с подложкой по столбцам периодической таблицы.[7] Однако значительная интеркаляция Na в графит может происходить в тех случаях, когда ион заключен в оболочку растворителя в процессе совместной интеркаляции. Сложная разновидность магния (I) также внедрилась в графит.[8]
Бисульфат графита, перхлорат, гексафторарсенат: окисленные атомы углерода
Соединения интеркалирования бисульфат графита и перхлорат графита могут быть получены обработкой графита сильными окислителями в присутствии сильных кислот. В отличие от графитов калия и кальция, в этом процессе окисляются углеродные слои: 48 C + 0,25 O2 + 3 часа2ТАК4 → [C24]+[HSO4]−· 2H2ТАК4 + 0,5 часов2О
В перхлорате графита количество плоских слоев атомов углерода составляет 794 пикометры отдельно, разделенные ClO4− ионы. Катодное восстановление перхлората графита аналогично нагреванию KC.8, что приводит к последовательному удалению HClO4.
Как бисульфат графита, так и перхлорат графита являются лучшими проводниками по сравнению с графитом, как и было предсказано с использованием механизма положительных отверстий.[4]Реакция графита с [O2]+[AsF6]− дает соль [C8]+[AsF6]−.[4]
Производные галогенидов металлов
Ряд галогенидов металлов интеркалирует в графит. Наиболее изучены хлоридные производные. Примеры включают MCl2 (M = Zn, Ni, Cu, Mn), MCl3 (M = Al, Fe, Ga), MCl4 (M = Zr, Pt) и т. Д.[1] Материал состоит из слоев плотноупакованных слоев галогенидов металлов между листами углерода. Производная C~8FeCl3 экспонаты спин-стекло поведение.[9] Эта система оказалась особенно плодородной для изучения фазовых переходов.[нужна цитата ] Ступень n магнитного GIC имеет n слоев графита, разделяющих последовательные магнитные слои. По мере увеличения номера стадии взаимодействие между спинами в последовательных магнитных слоях становится слабее, и может возникнуть двумерное магнитное поведение.
Галоген- и оксид-графитовые соединения
Хлор и бром обратимо интеркалируют в графит. Йода нет. Фтор реагирует необратимо. В случае брома известны следующие стехиометрии: CпBr для n = 8, 12, 14, 16, 20 и 28.
Потому что образуется необратимо, монофторид углерода часто не классифицируется как соединение интеркаляции. Имеет формулу (CF)Икс. Его получают реакцией газообразного фтор с графитом при 215–230 ° C. Цвет сероватый, белый или желтый. Связь между атомами углерода и фтора ковалентная. Монофторид тетракарбона (C4F) получают обработкой графита смесью фтора и фтороводород при комнатной температуре. Состав имеет черновато-синий цвет. Монофторид углерода не является электропроводным. Он был изучен как катод материал в одном типе первичной (неперезаряжаемой) литиевые батареи.
Оксид графита представляет собой неустойчивое твердое вещество желтого цвета.
Свойства и приложения
Соединения интеркалирования графита на протяжении многих лет очаровывали материаловедов благодаря своим разнообразным электронным и электрическим свойствам.
Сверхпроводимость
Среди сверхпроводящих соединений интеркалирования графита CaC
6 имеет самую высокую критическую температуру Tc = 11,5 К, которое далее увеличивается под действием приложенного давления (15,1 К при 8 ГПа).[6] Считается, что сверхпроводимость в этих соединениях связана с ролью межслоевого состояния - свободной электронной зоны, расположенной примерно на 2 эВ (0,32 аДж) выше Уровень Ферми; сверхпроводимость возникает только при заполнении межслоевого состояния.[10] Анализ чистых CaC
6 используя высокое качество ультрафиолетовый свет показал проводить фотоэмиссионная спектроскопия с угловым разрешением измерения. Открытие сверхпроводящей щели в π * -зоне выявило существенный вклад в общую силу электрон-фононной связи от π * -межслойного межзонного взаимодействия.[10]
Реагенты в химическом синтезе: KC8
Материал бронзового цвета KC8 один из самых сильных восстановители известен. Он также использовался как катализатор в полимеризация и как связывающий реагент за арилгалогениды к бифенилы.[11] В одном исследовании свежеприготовленный KC8 обрабатывали 1-йодододеканом, доставляя модификацию (микрометр чешуйчатые углеродные пластинки с длинными выступающими алкильными цепями, обеспечивающими растворимость), который растворим в хлороформ.[11] Еще одно соединение графита калия, KC24, был использован в качестве монохроматора нейтронов. Новое важное применение графита калия было представлено изобретением калиево-ионный аккумулятор. Словно литий-ионный аккумулятор, то калиево-ионный аккумулятор следует использовать анод на углеродной основе вместо металлического анода. В этом случае важным преимуществом является стабильная структура графита калия.
Смотрите также
- Бакминстерфуллерен интеркалаты
- Ковалентные сверхпроводники
- Диборид магния, в котором используются шестиугольные плоские бор листы вместо карбона
- Пиролитический графит
Рекомендации
- ^ а б Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- ^ H-P Boehm; Setton, R .; Stumpp, E .; и другие. (1994). «Номенклатура и терминология интеркаляционных соединений графита» (PDF). Чистая и прикладная химия (PDF). 66 (9): 1893. Дои:10.1351 / pac199466091893. Архивировано из оригинал (PDF) на 2012-04-06.
- ^ а б Ottmers, D.M .; Расе, Х.Ф. (1966). «Графиты калия, полученные методом смешанной реакции». Углерод. 4 (1): 125–127. Дои:10.1016/0008-6223(66)90017-0. ISSN 0008-6223.
- ^ а б c d Кэтрин Э. Хаукрофт; Алан Г. Шарп (2008). «Глава 14: Группа 14 элементов». Неорганическая химия, 3-е издание. Пирсон. п. 386. ISBN 978-0-13-175553-6.
- ^ NIST Ionizing Radiation Division 2001 - Основные технические достижения. Physics.nist.gov
- ^ а б c Emery, N .; Херольд, Клэр; Марише, Жан-Франсуа; Лагранж, Филипп; и другие. (2008). «Обзор: Синтез и сверхпроводящие свойства CaC.6". Наука и технология перспективных материалов (PDF). 9 (4): 044102. Bibcode:2008STAdM ... 9d4102E. Дои:10.1088/1468-6996/9/4/044102. ЧВК 5099629. PMID 27878015.
- ^ а б Лю, Юаньюэ; Меринов, Борис В .; Годдард, Уильям А. (5 апреля 2016 г.). «Происхождение низкой емкости по натрию в графите и, как правило, слабого связывания Na и Mg с субстратом среди щелочных и щелочноземельных металлов». Труды Национальной академии наук. 113 (14): 3735–3739. arXiv:1604.03602. Bibcode:2016ПНАС..113.3735Л. Дои:10.1073 / pnas.1602473113. ЧВК 4833228. PMID 27001855.
- ^ Сюй, Вэй; Чжан, Ханьян; Лернер, Майкл М. (25.06.2018). «Интеркаляция графита комплексами диамина магния». Неорганическая химия. Американское химическое общество (ACS). 57 (14): 8042–8045. Дои:10.1021 / acs.inorgchem.8b01250. ISSN 0020-1669.
- ^ Миллман, С. Э .; Циммерман Г.О. (1983). «Наблюдение за состоянием спинового стекла в FeCl.3: графит интеркалированный ». Журнал физики C: Физика твердого тела. 16 (4): L89. Bibcode:1983JPhC ... 16L..89M. Дои:10.1088/0022-3719/16/4/001.
- ^ а б Csányi; Littlewood, P. B .; Невидомский, Андрей Х .; Пикард, Крис Дж .; Simons, B.D .; и другие. (2005). «Роль межслоевого состояния в электронной структуре сверхпроводящих соединений с интеркалированным графитом». Природа Физика. 1 (1): 42–45. arXiv:cond-mat / 0503569. Bibcode:2005НатФ ... 1 ... 42С. Дои:10.1038 / nphys119.
- ^ а б Чакраборти, С .; Чаттопадхьяй, Джаянта; Го, Вэньхуа; Биллапс, У. Эдвард; и другие. (2007). «Функционализация графита калия». Angewandte Chemie International Edition. 46 (24): 4486–8. Дои:10.1002 / anie.200605175. PMID 17477336.
дальнейшее чтение
- Т. Еноки, М. Судзуки и М. Эндо (2003). Соединения интеркалирования графита и их применение. Издательство Оксфордского университета. ISBN 978-0-19-512827-7.
- РС. Dresselhaus и G. Dresselhaus Review (1981). «Интеркаляционные соединения графита». Успехи в физике. 30 (2): 139–326. Bibcode:1981AdPhy..30..139D. Дои:10.1080/00018738100101367. (187 страниц), также перепечатывается как Dresselhaus, M. S .; Дрессельхаус, Г. (2002). «Интеркаляционные соединения графита». Успехи в физике. 51 (1): 1–186. Bibcode:2002AdPhy..51 .... 1D. CiteSeerX 10.1.1.170.2655. Дои:10.1080/00018730110113644.
- Д. Савойя; Тромбини, К .; Умани-Рончи, А .; и другие. (1985). «Применение калий-графита и металлов, диспергированных на графите, в органическом синтезе» (PDF). Чистая и прикладная химия (PDF). 57 (12): 1887. Дои:10.1351 / pac198557121887.
- Suzuki, Itsuko S .; Тинг-Ю Хуанг; Масацугу Сузуки (13 июня 2002 г.). «Магнитная фазовая диаграмма CoCl-1 ступени.2 соединение интеркаляции графита: наличие метамагнитного перехода и спин-флоп переходов ». Физический обзор B. 65 (22): 224432. Bibcode:2002PhRvB..65v4432S. Дои:10.1103 / PhysRevB.65.224432.
- Rancourt, DG; C Meschi; С. Фландруа (1986). "S = 1/2 антиферромагнитные конечные цепочки, эффективно изолированные фрустрацией: CuCl2-интеркалированный графит ». Физический обзор B. 33 (1): 347–355. Bibcode:1986ПхРвБ..33..347Р. Дои:10.1103 / PhysRevB.33.347. PMID 9937917.


