Срединное преоптическое ядро - Median preoptic nucleus
| Срединное преоптическое ядро | |
|---|---|
| Идентификаторы | |
| NeuroNames | 378 |
| НейроЛекс Я БЫ | birnlex_1208 |
| TA98 | A14.1.08.908 |
| TA2 | 5711 |
| FMA | 62323 |
| Анатомические термины нейроанатомии | |

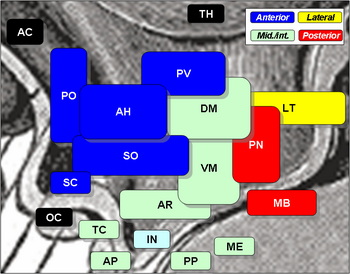
В срединное преоптическое ядро расположен дорсальнее трех других ядер преоптическая область из передний гипоталамус. Гипоталамус расположен прямо под таламус, главная сенсорная релейная станция нервная система, и считается частью лимбическая система, который также включает такие структуры, как гиппокамп и миндалина. Гипоталамус принимает активное участие в поддержании гомеостаз тела, и срединное преоптическое ядро не является исключением, способствуя регуляции состава крови, температура тела, и медленный сон.
Срединное преоптическое ядро активно участвует в трех основных областях. К ним относятся осморегуляция, терморегуляция, и спать гомеостаз. Внутри каждой области есть множество функций. Роль, которую играет медианное преоптическое ядро в осморегуляция в состав крови и объем, включая баланс жидкости и соли, и вызывает реакцию, варьирующуюся от поведенческой до эндокринный. Терморегуляция включает оба ответа на инфекционное заболевание и к понижению внутренней температуры при кожный воздействие холода, оба из которых вовлекают срединное преоптическое ядро как важный медиатор сенсорного ввода и нормативный выпуск. Гомеостаз сна участвует как в возникновении, так и в поддержании спать.
Срединное преоптическое ядро имеет возбуждающий и тормозящий проекции на многие области мозг. Он оказывает тормозящее влияние через ГАМКергический проекции на области мозга, участвующие в стимуляция из термогенез, а также на активные области мозга, чтобы вызвать сон. Микроинъекция этанола, триазолам, и пропофол в этой области вызывает сон у грызунов, предполагая, что он участвует в их фармакологическом воздействии на сон. Глутаматергический и норадренергический, а также другие нейротрансмиттеры, имеют возбуждающий влияет на другие области мозга. Срединное преоптическое ядро активно участвует в сердечно-сосудистый регулирование, включая выпуск предсердный натрийуретический пептид посредством сердце в ответ на высокий объем крови. Он также участвует в управлении фебрильный ответ на инфекционное заболевание и стимулирование жажда, среди других функций. Связность и анатомическое положение медианного преоптического ядра позволяют ему быть одновременно ретрансляционной станцией и посредником для сенсорной и регуляторной информации, а также производить нервный, эндокринный и поведенческий ответы на поддержание гомеостаз.
Расположение
Срединное преоптическое ядро расположено в преоптическая область из гипоталамус. Формирует критическую часть антеровентрального третий желудочек и средняя линия lamina terminalis, медианное преоптическое ядро занимает анатомическое положение, что позволяет ему играть важную роль во многих аспектах гомеостатический регулирование. Этот регион важен в сердечно-сосудистый, артериальное давление, и состав крови регулирования, и получает входы от подформенный орган (SFO) и сосудистый орган lamina terminalis (VOLT), которые лежат вне гематоэнцефалический барьер и передавать информацию о осмоляльность крови и уровни эндокринный сигналы, такие как предсердный натрийуретический пептид (ANP).[1]
Связь
Связь с другими регионами гипоталамус, такой как вентролатеральная преоптическая область (VLPO) и с областями ствола головного мозга также позволяют среднему преоптическому ядру участвовать в других аспектах гомеостаз. К ним относятся поведение во сне и бодрствовании, а также жажда пьянство, а также терморегуляция. Параллельные пути в преоптическая область участвуют в регуляции температуры тела и высокая температура отклик. Один путь берет начало в срединном преоптическом ядре, а другой - в дорсолатеральной преоптической области (DLPO). Оба тормозящий в районы мозговой ствол которые активируют не дрожащий термогенез через коричневая жировая ткань (BAT) в ответ на кожный холод или простагландин E2.[2]
Роль в терморегуляции
Известно, что у млекопитающих существует циркадный ритм температуры тела (Tb), который зависит от целостности супрахиазматического ядра (SCN), однако голодание также влияет на Tb в период покоя, и присутствие SCN важно для этого процесса. Хотя не только SCN, но и дугообразное ядро (ARC), участвуют в настройке Tb через афференты к терморегулирующему срединному преоптическому ядру (MnPO). После исследований, проведенных Guzmán-Ruiz et al. Известно, что высвобождение вазопрессина из SCN снижает температуру непосредственно перед началом светового дня, тогда как высвобождение гормона, стимулирующего выработку а-меланоцитов, особенно в конце темного периода, поддерживает высокую температуру. Оба пептида оказывают противоположное влияние на активность коричневой жировой ткани через терморегуляторные ядра, такие как дорсомедиальное ядро гипоталамуса и ядро дорсального шва. Координация циркадных и метаболических сигналов в гипоталамусе необходима для адекватного контроля температуры. Баланс между высвобождением нейропептидов, производимых биологическими часами и метаболическим сенсорным органом, таким как дугообразное ядро, необходим для адекватного контроля температуры. Эти наблюдения показывают, что области мозга, участвующие в циркадных и метаболических функциях организма, должны взаимодействовать, чтобы обеспечить согласованную организацию физиологических процессов, связанных с контролем температуры [11].
Механизмы нервной активации, участвующие в регуляции температура тела в основном не определены. Известно, что симпатические пути участвуют в увеличении производства тепла и сокращении потерь тепла и активируются нейроны в ростальном мозговом шве (RMR).[2] Было установлено, что эти нейроны играют важную роль в повышении температуры тела как при воздействии холода, так и при индуцированной лихорадке, по наблюдениям, что гиперполяризация до воздействия этих условий подавляет подъем температура тела в ответ.
Лихорадочный ответ
Входы в RMR от медианного преоптического ядра: ГАМКергический, а потому тормозящий характер. Поражения среднего преоптического ядра вызывают уменьшение высокая температура ответов, так как прогнозы от MnPn до RMR содержат простагландин Рецепторы EP3, которые необходимы для ответа на лихорадку. Простагландин E2 связывается с рецепторами E3 в среднем преоптическом ядре, чтобы ингибировать их активность и вызывать высокая температура. Это означает, что медианное преоптическое ядро отвечает за механизмы торможения, которые повышают температура тела. Это не единственная область гипоталамус вовлечение, и устранение активности срединного преоптического ядра само по себе не вызовет повышения температуры тела. В сочетании с поражениями на других преоптический ядра гипоталамуса, однако, повреждение среднего преоптического ядра вызывает повышенное исходная температура тела.[2]
Менопауза
Другие рецепторы, нейрокинин 3 рецепторы, которые экспрессируются в срединном преоптическом ядре, также участвуют в терморегуляция. Активация этих рецепторов у крыс вызывает снижение температура ядра. Эти рецепторы сильно экспрессируются в средней преоптической области в ответ на снижение эстроген уровни в менопаузальный женщин, и считается, что они играют роль в формировании приливы в течение менопауза.[3]
Воздействие холода в окружающей среде
Реакция на холод вызывается кожными чувствительными к холоду путями через Парабрахиальная область. Терморецепторы в коже определяют температуру окружающей среды относительно температуры тела. Эти афферентные нейроны проецируются вверх по спинному мозгу к парабрахиальной области, которая иннервирует несколько областей преоптической зоны, включая медианное преоптическое ядро. Воздействие холода приводит к растормаживание RMR и других регионов, что приводит к термогенезу коричневого жира. Это также известно как термогенез без дрожи, который метаболизирует жир, но рассеивается тепло от движущая сила протона в митохондриях, а не с использованием окислительного фосфорилирования производить АТФ.[4]
Роль в осморегуляции
Область мозга, которая включает вентральную часть среднего преоптического ядра, передне-вентральный третий желудочек (AV3V), сильно участвует в поддержании жидкости, электролитов и сердечно-сосудистой системы. гомеостаз.[5] Срединное преоптическое ядро вместе с сосудистый орган lamina terminalis (VOLT) и подформенный орган (SFO) реагируют на изменения в составе крови, а также на нервные импульсы от рецепторов в кровеносных сосудах.Рецепторы растяжения в аорта и другие суда отправляют сенсорного ввода в этот регион, передавая информацию о объем крови и артериальное давление.
Реакция на изменение осмоляльности крови
Важность среднего преоптического ядра в составе жидкости и гомеостазе можно увидеть анатомически, поскольку оно содержит связи между несколькими областями, которые сильно участвуют в балансе жидкости в организме и сердечно-сосудистой функцией, такими как паравентрикулярный ядро и супраоптический ядро. Эти области лежат за пределами гематоэнцефалический барьер и имеют рецепторы, которые определяют осмоляльность крови и передают информацию через среднее преоптическое ядро.
Функционально его важность можно понять, потому что поражения к срединному преоптическому ядру обычно вызывают несоответствующий состав жидкости, потребление воды и высвобождение предсердный натрийуретический пептид (ANP).[5] Ответы на изменения в составе жидкости, опосредованные средним преоптическим ядром, являются результатом норадренергический иннервация из областей каудального вентролатерального мозгового вещества. Ответы могут быть эндокринный, автономный или поведенческий и ответы на скачки уровня натрия в крови включают высвобождение предсердного натрийуретического пептида и окситоцина. Предсердный натрийуретический пептид высвобождается сердцем в ответ на высокое артериальное давление и высокая соленость крови. Это важный и мощный вазодилататор, а также снижает обратный захват натрия почками. Кроме того, он подавляет такие пути, как ренин-альдострон-ангиотензин путь, который поднимает артериальное давление.[5]
Активация срединного преоптического ядра приводит к стимуляция из паравентрикулярное ядро (PVN). Афференты к этой области глутаматергический, или используют глутамат в качестве основного нейромедиатора, хотя ангиотензин II производит аналогичный ответ и приводит к симпатическому возбуждению PVN.[6] Это было подтверждено использованием глутамат антагонист рецептора в PVN, который ингибировал этот ответ в результате активации MnPn. Таким образом, глутамат, связанный с рецепторами, необходим для активация этих нейронов в срединном преоптическом ядре и активация паравентрикулярного ядра. Активация PVN через этот глутаматергический механизм приводит к увеличению активности почечный симпатический нерв пути, а также частота сердцебиения и среднее артериальное давление.[7]
Роль в гомеостатической регуляции сна
Анатомические и электрофизиологический Эксперименты на взрослых крысах показывают, что медиана преоптического ядра играет важную роль в производстве сна. Первым свидетельством этого было наблюдение, что ущерб этой области нанес бессонница у пациентов-людей.[8] Текущие эксперименты с использованием c-Fos экспрессия в качестве маркера активации нейронов во время сна показывает дихотомия функции по продвижению и поддержанию сна между вентролатеральное преоптическое ядро и срединное преоптическое ядро. Данные свидетельствуют о том, что ГАМКергический нейроны в среднем преоптическом ядре играют роль в стимулировании наступления сна, в то время как нейроны в вентролатеральное преоптическое ядро играют роль в поддержании сна.[9] Хотя идея полного разделения функций между этими двумя ядрами является привлекательной, это, скорее, вопрос степени участия этих двух ядер в возникновении и поддержании сна, а не играющих совершенно разные роли. Вероятно, что MnPn играет важную, но не исключительную роль в наступлении сна, тогда как VLPO играет более важную роль в поддержании сна. Обе области проецируются на активные области мозга. Существует также плотная двунаправленная проекция нейронов между средним преоптическим ядром и вентролатеральное преоптическое ядро. Это существование тормозных выступов между вентролатернальным преоптическим ядром и средним преоптическим ядром предполагает общую функцию и регуляторные отношения между двумя ядрами.[9]
Медленный сон
Поощрение сна ГАМКергическими нейронами в средней преоптической области наиболее тесно связано с NREM, или спокойный сон.[10] Время, проведенное в медленном сне, увеличивается с количеством активированных ГАМК рецепторов в средней преоптической области, что демонстрируется увеличением времени медленного сна в ответ на микроинъекции агонистов ГАМК в среднюю преоптическую зону кошек. Время, проведенное в фазе быстрого сна, не увеличилось, а контрольные инъекции уменьшили время, проведенное как в медленном, так и в быстром сне.[10]
Отношения с VLPO
Вентролатеральное (VLPO) и медианное преоптическое (MnPn) ядра способствуют засыпанию. ГАМКергический проекции нейронов в активные области мозга. Активация нейронов в VLPO и MnPn приводит к увеличению концентрации первичного тормозного нейромедиатора, ГАМК, в областях бодрствования мозга, таких как туберомаммиллярное ядро и голубое пятно. Это приводит к торможению холинергический, норадренергический и серотонинергический деятельность в этих областях. Норадренергические проекции из областей, способствующих бодрствованию, подавляют области, способствующие засыпанию, устанавливая «взаимное тормозящее взаимодействие» между областями сна и бодрствования, которое приводит к регуляции сон. Механизм активации нейронов, способствующих сну, в VLPO и MnPn не был четко определен, однако было высказано предположение, что супрахиазмическое ядро может играть роль, а также просто уменьшать сенсорного ввода в начале сонливости.[8]
Рекомендации
- ^ Колай, М., и Рено, Л. П. (2010). Метаботропные рецепторы глутамата в срединных преоптических нейронах модулируют возбудимость нейронов и глутаматергические и ГАГАергические входы из субфорного органа (том 103, стр. 1104, 2010). Журнал нейрофизиологии, 104 (1), 579-579
- ^ а б c Йошида, К., Ли, X. Д., Кано, Г., Лазарус, М., и Сапер, К. Б. (2009). Параллельные преоптические пути терморегуляции. Журнал неврологии, 29 (38)
- ^ Дакс, П. А., Краевский, С. Дж., И Ранс, Н. Е. (2011). Активация рецепторов нейрокинина 3 в среднем преоптическом ядре снижает внутреннюю температуру у крысы. Эндокринология, 152 (12), 4894-4905.
- ^ Накамура, К. (2011). Центральные схемы регулирования температуры тела и повышения температуры тела. Американский журнал физиологии. Регуляторная интегративная и сравнительная физиология, 301 (5), R1207-R1228.
- ^ а б c Педрино, Г. Р., Монако, Л. Р., и Краво, С. Л. (2009). Вазодилатация почек, вызванная гипернатриемией. Роль альфа-адренорецепторов в среднем преоптическом ядре. Клиническая и экспериментальная фармакология и физиология, 36 (12)
- ^ Генри М., Гроб М. и Мужино Д. (2009). Эндогенный ангиотензин II способствует ГАМКергической нейротрансмиссии, афферентной к Na + -чувствительным нейронам среднего преоптического ядра крысы. Американский журнал физиологии. Регуляторная интегративная и сравнительная физиология, 297 (3), R783-R792.
- ^ Ллевеллин, Т., Чжэн, Х., Лю, X. Ф., Сюй, Б., и Патель, К. П. (2012). Срединное преоптическое ядро и субфорный орган управляют почечной симпатической нервной активностью посредством глутаматергического механизма в паравентрикулярном ядре. Американский журнал физиологии. Регуляторная интегративная и сравнительная физиология, 302 (4), R424-R432.
- ^ а б Луппи, П. Х., и Форт, П. (2011). Какие механизмы активируют спящие нейроны, расположенные в преоптической области? Сон и биологические ритмы, 9, 59-64.
- ^ а б Гвилия, И., Сунцова, Н., Ангара, Б., МакГинти, Д., и Шимусиак, Р. (2011). Созревание гомеостаза сна у развивающихся крыс: роль нейронов преоптической области. Американский журнал физиологии. Регуляторная интегративная и сравнительная физиология, 300 (4), R885-R894
- ^ а б Бенедетто Л., Чейз М. Х. и Тортероло П. (2012). ГАМКергические процессы в среднем преоптическом ядре способствуют медленному сну. Поведенческие исследования мозга, 232 (1), 60-65.
[11] Гусман-Руис, М.А., Рамирес-Корона, А., Герреро-Варгас, Н.Н., Сабат, Э., Рамирес-Пласенсиа, О.Д., Фуэнтес-Ромеро, Р., ... и Буйс, Р.М. (2015) . Роль супрахиазматического и дугообразного ядер в регуляции суточной температуры у крыс. Журнал неврологии, 35 (46), 15419-15429.
