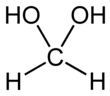
Метандиол - Methanediol
| |||
 | |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Метандиол[1] | |||
Другие имена
| |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| Сокращения | МАДОЛ | ||
| 1730798 | |||
| ЧЭБИ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.006.673 | ||
| Номер ЕС |
| ||
PubChem CID | |||
| UNII | |||
| |||
| |||
| Характеристики | |||
| CЧАС4О2 | |||
| Молярная масса | 48.041 г · моль−1 | ||
| Внешность | Бесцветная жидкость | ||
| Плотность | 1,199 г см−3 | ||
| Точка кипения | 194 ° C (381 ° F, 467 K) при 101 кПа | ||
| Давление газа | 16,1 Па | ||
| Кислотность (пKа) | 13.29[2] | ||
| 1.401 | |||
| Опасности | |||
| точка возгорания | 99,753 ° С (211,555 ° F, 372,903 К) | ||
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Метандиол, также известный как моногидрат формальдегида или же метиленгликоль, является органическое соединение с химическая формула CH2(ОЙ)2. Это самый простой геминальный диол. Он встречается не в чистом виде, а в виде водных растворов, где он сосуществует с олигомерами (короткими полимерами). Состав хорошо охарактеризован, но имеет меньшее технологическое значение, чем родственные параформальдегид ((CH2O)п), формальдегид (ЧАС2C = O) и 1,3,5-триоксан ((CH2O)3).[3]
Метандиол является продуктом гидратация формальдегида. В константа равновесия для гидратации оценивается в 103,[4] CH2(ОЙ)2 преобладает в разбавленном (<0,1%) растворе. В более концентрированных растворах олигомеризуется до HO (CH2O)пЧАС.[3]
Вхождение
Дианион, метандиолат, считается промежуточным звеном в скрещенных Канниццаро реакция.
Состав имеет некоторое отношение к астрохимия.[5]
Безопасность
Метандиол, а не формальдегид, указан как один из основных ингредиентов "Бразильский выброс ", формула для выпрямления волос, продаваемая в США. Равновесие с формальдегидом вызывает беспокойство, поскольку формальдегид в выпрямителях для волос представляет опасность для здоровья,[6][7] но риск оспаривается.[8]
Смотрите также
- Ортоформиновая кислота (метантриол)
- Ортокарбоновая кислота (метантетрол)
Рекомендации
- ^ «Метандиол - Резюме соединения». PubChem Compound. США: Национальный центр биотехнологической информации. 26 марта 2005 г. Идентификационные и связанные записи. Получено 20 октября 2011.
- ^ Bell, R.P .; Мактиг, П. Т. (1960). «603. Кинетика альдольной конденсации ацетальдегида». Журнал химического общества (возобновлено): 2983. Дои:10.1039 / JR9600002983.
- ^ а б Ройсс, Гюнтер; Дистелдорф, Вальтер; Геймер Армин Отто; Эфес, Альбрехт (2000). «Формальдегид». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a11_619.
- ^ Эрик В. Анслин, Деннис А. Догерти (2006), Современная физическая органическая химия. Книги университетских наук. ISBN 1-891389-31-9. 1095 страниц
- ^ Гаррод, Робин Т .; Уивер, Сюзанна Л. Видикус; Хербст, Эрик (2008). «Сложная химия в областях звездообразования: расширенная химическая модель разогрева газовых зерен». Астрофизический журнал. 682 (1): 283–302. arXiv:0803.1214. Bibcode:2008ApJ ... 682..283G. Дои:10.1086/588035.
- ^ «Продукты для разглаживания волос, которые могут выделять формальдегид». www.osha.gov. Управление по охране труда.
- ^ SpecialChem. "Новости индустрии".
- ^ Golden, R .; Валентини, М. (июль 2014 г.). «Эквивалентность формальдегида и метиленгликоля: критическая оценка химических и токсикологических аспектов». Нормативная токсикология и фармакология. 69 (2): 178–186. Дои:10.1016 / j.yrtph.2014.03.007. PMID 24709515.