Паннексин - Pannexin
| Часть серия на |
| Пуринергическая сигнализация |
|---|
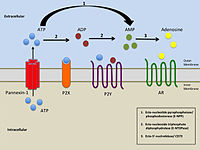 Упрощенная иллюстрация внеклеточной пуринергической передачи сигналов |
| Концепции |
| Мембранные транспортеры |
| Паннексин | |
|---|---|
| Идентификаторы | |
| Символ | Паннексин |
| ИнтерПро | IPR039099 |
| TCDB | 1.A.25 |
| паннексин 1 | |||||||
|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||
| Символ | PANX1 | ||||||
| Ген NCBI | 24145 | ||||||
| HGNC | 8599 | ||||||
| OMIM | 608420 | ||||||
| RefSeq | NM_015368 | ||||||
| UniProt | Q96RD7 | ||||||
| Прочие данные | |||||||
| Locus | Chr. 11 q14-q21 | ||||||
| |||||||
| паннексин 2 | |||||||
|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||
| Символ | PANX2 | ||||||
| Ген NCBI | 56666 | ||||||
| HGNC | 8600 | ||||||
| OMIM | 608421 | ||||||
| RefSeq | NM_052839 | ||||||
| UniProt | Q96RD6 | ||||||
| Прочие данные | |||||||
| Locus | Chr. 22 q13 | ||||||
| |||||||
| паннексин 3 | |||||||
|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||
| Символ | PANX3 | ||||||
| Ген NCBI | 116337 | ||||||
| HGNC | 20573 | ||||||
| OMIM | 608422 | ||||||
| RefSeq | NM_052959 | ||||||
| UniProt | Q96QZ0 | ||||||
| Прочие данные | |||||||
| Locus | Chr. 11 q24.2 | ||||||
| |||||||
Паннексины (от греческого παν - все и от латинского nexus - соединение) - это семейство белков позвоночных, идентифицированных по их гомологии с беспозвоночными. иннексины.[1] Хотя иннексины отвечают за формирование щелевые соединения у беспозвоночных было показано, что паннексины преимущественно существуют в виде больших трансмембранных каналы соединяя внутриклеточное и внеклеточное пространство, обеспечивая прохождение ионов и небольших молекул между этими компартментами (такими как АТФ и сульфородамин B ).
Три паннексина описаны в Хордовые: Panx1, Panx2 и Panx3.[2]
Функция
Паннексины могут образовывать межклеточные трансмембранные «полуканалы» для транспорта молекул размером менее 1000 Да или межклеточные щелевые соединения. Эти гемиканалы могут присутствовать в плазме, мембранах ER и Гольджи. Они транспортируют Ca2+, АТФ, инозитолтрифосфат и другие небольшие молекулы и могут образовывать полуканалы с большей легкостью, чем субъединицы коннексина.[3] Паннексин 1 представляет собой катионный канал с большой проводимостью сердечных миоцитов.[4] Паннексин 1 и паннексин 2 лежат в основе функции каналов в нейронах и способствуют ишемическому повреждению мозга.[5]
Было показано, что паннексин 1 участвует в ранних стадиях врожденного иммунитета через взаимодействие с P2X7 пуринергический рецептор. Активация канала паннексина путем связывания АТФ с рецептором P2X7 приводит к высвобождению интерлейкин-1β.[6]
Гипотетические роли паннексинов в нервной системе включают участие в сенсорной обработке, синхронизацию между гиппокамп и кора, пластичность гиппокампа и распространение кальциевых волн. Волны кальция поддерживаются глиальными клетками, которые помогают поддерживать и модулировать нейроны. метаболизм. Согласно одной из гипотез, паннексины также могут участвовать в патологических реакциях, в том числе в повреждении нервной системы после ишемии и последующей гибели клеток.[7]
Каналы паннексина 1 - это пути высвобождения АТФ из клеток.[8]
Отношение к коннексинам
Межклеточный щелевые соединения у позвоночных, включая человека, образуются коннексин семейство белков.[9] Структурно паннексины и коннексины очень похожи и состоят из 4 трансмембранных доменов, 2 внеклеточных и 1 внутриклеточной петли, а также внутриклеточных N- и C-концевых хвостов. Несмотря на эту общую топологию, белковые семейства не обладают достаточным сходством последовательностей, чтобы с уверенностью сделать вывод об общем происхождении.
N-концевой участок (Pfam PF12534 ) из VRAC -формирование белков LRRC8, таких как LRRC8A также могут быть связаны с паннексинами.[10]
Структура Xenopus tropicalis (западная когтистая лягушка) паннексин (PDB: 6VD7) Была решена. Он образует гептамерный диск. Человеческая версия (PDB: 6М02) Аналогично.[11][12]
Клиническое значение
Усекающие мутации в паннексине 1 способствуют метастазированию рака груди и толстой кишки в легкие, позволяя раковым клеткам выжить при механическом растяжении в микроциркуляции за счет высвобождения АТФ.[13]
Паннексины могут участвовать в процессе развития опухоли. В частности, уровни экспрессии PANX2 предсказывают выживаемость после постановки диагноза для пациентов с глиальными опухолями.
Пробенецид, хорошо зарекомендовавший себя препарат для лечения подагра, позволяет различать каналы, образованные коннексины и паннексины. Пробенецид не влияет на каналы, образованные коннексинами, но ингибирует каналы паннексина-1.[14]
Рекомендации
- ^ Панчин Ю., Кельмансон И., Мац М., Лукьянов К., Усман Н., Лукьянов С. (июнь 2000 г.). «Вездесущее семейство предполагаемых молекул щелевых контактов». Текущая биология. 10 (13): R473-4. Дои:10.1016 / S0960-9822 (00) 00576-5. PMID 10898987. S2CID 20001454.
- ^ Литвин О., Тиунова А., Коннелл-Альбертс Ю., Панчин Ю., Баранова А. (2006). «Что спрятано в сокровищнице паннексина: взгляды и догадки». Журнал клеточной и молекулярной медицины. 10 (3): 613–34. Дои:10.1111 / j.1582-4934.2006.tb00424.x. ЧВК 3933146. PMID 16989724.
- ^ Шестопалов В.И., Панчин Ю. (февраль 2008 г.). «Паннексины и разнообразие белков щелевых контактов». Клеточные и молекулярные науки о жизни. 65 (3): 376–94. Дои:10.1007 / s00018-007-7200-1. PMID 17982731. S2CID 23181471.
- ^ Лимай С.Р., Махмуд М.А. (октябрь 1987 г.). «Микроангиопатия сетчатки при пигментной паравенозной хориоретинальной атрофии». Британский журнал офтальмологии. 71 (10): 757–61. Дои:10.1136 / bjo.71.10.757. ЧВК 1041301. PMID 3676145.
- ^ Барджотас П., Кренц А., Хормузди С.Г., Риддер Д.А., Херб А., Баракат В. и др. (Декабрь 2011 г.). «Паннексины при нейродегенерации, вызванной ишемией». Труды Национальной академии наук Соединенных Штатов Америки. 108 (51): 20772–7. Bibcode:2011PNAS..10820772B. Дои:10.1073 / pnas.1018262108. ЧВК 3251101. PMID 22147915.
- ^ Пелегрин П., Surprenant A (ноябрь 2006 г.). «Паннексин-1 опосредует образование крупных пор и высвобождение интерлейкина-1бета АТФ-зависимым рецептором P2X7». Журнал EMBO. 25 (21): 5071–82. Дои:10.1038 / sj.emboj.7601378. ЧВК 1630421. PMID 17036048.
- ^ Барджотас П., Кренц А., Хормузди С.Г., Риддер Д.А., Херб А., Баракат В. и др. (Декабрь 2011 г.). «Паннексины при нейродегенерации, вызванной ишемией». Труды Национальной академии наук Соединенных Штатов Америки. 108 (51): 20772–7. Bibcode:2011PNAS..10820772B. Дои:10.1073 / pnas.1018262108. ЧВК 3251101. PMID 22147915.
- ^ Бао Л., Локовей С., Даль Г. (август 2004 г.). «Мембранные каналы паннексина являются механочувствительными проводниками для АТФ». Письма FEBS. 572 (1–3): 65–8. Дои:10.1016 / j.febslet.2004.07.009. PMID 15304325. S2CID 43459258.
- ^ Даль Г., Локовей С. (июль 2006 г.). «Паннексин: пробивать или не пробивать - это вопрос?». IUBMB Life. 58 (7): 409–19. Дои:10.1080/15216540600794526. PMID 16801216. S2CID 24038607.
- ^ Abascal F, Zardoya R (июль 2012 г.). «Белки LRRC8 имеют общего предка с паннексинами и могут образовывать гексамерные каналы, участвующие в межклеточной коммуникации». BioEssays. 34 (7): 551–60. Дои:10.1002 / bies.201100173. HDL:10261/124027. PMID 22532330. S2CID 24648128.
- ^ Михальски К., Сирянен Дж. Л., Хенце Э, Кумпф Дж., Фурукава Х., Кавате Т. (февраль 2020 г.). «Крио-ЭМ-структура паннексина 1 раскрывает уникальные мотивы отбора и ингибирования ионов». eLife. 9: e54670. Дои:10.7554 / eLife.54670. ЧВК 7108861. PMID 32048993.
- ^ Цюй Р., Донг Л., Чжан Дж., Ю Икс, Ван Л., Чжу С. (март 2020 г.). «Крио-ЭМ структура канала человеческого гептамерного паннексина 1». Клеточные исследования. 30 (5): 446–448. Дои:10.1038 / s41422-020-0298-5. ЧВК 7196123. PMID 32203128.
- ^ Ферлоу П.В., Чжан С., Сунг Т.Д., Халберг Н., Гударзи Х., Мангрум С. и др. (Июль 2015 г.). «Механочувствительные каналы паннексина-1 опосредуют выживание метастатических клеток микрососудов». Природа клеточной биологии. 17 (7): 943–52. Дои:10.1038 / ncb3194. ЧВК 5310712. PMID 26098574.
- ^ Сильверман В., Локовей С., Даль Г. (сентябрь 2008 г.). «Пробенецид, средство от подагры, подавляет каналы паннексина 1». Американский журнал физиологии. Клеточная физиология. 295 (3): C761-7. Дои:10.1152 / ajpcell.00227.2008. ЧВК 2544448. PMID 18596212.
дальнейшее чтение
- Эндрю Л. Харрис и Даррен Лок (2009). Коннексины, Путеводитель. Нью-Йорк: Спрингер. п. 574. ISBN 978-1-934115-46-6.
