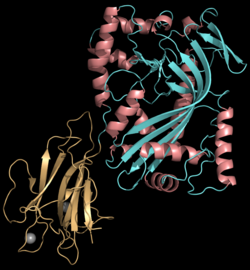
Перфорин - Википедия - Perforin
Перфорин-1 это белок что у людей кодируется PRF1 ген и Прф1 ген у мышей.[5][6][7]
Функция
Перфорин - порообразующий цитолитический белок содержится в гранулах цитотоксические Т-лимфоциты (CTL) и естественные клетки-киллеры (NK-клетки). На дегрануляция перфорин связывается с клетками-мишенями плазматическая мембрана, и олигомеризуется Ca2 + -зависимым образом с образованием пор на клетке-мишени. Образовавшаяся пора делает возможным пассивную диффузию семейства проапоптотических протеаз, известных как гранзимы, в целевую ячейку.[8] Литическая часть перфорина, внедряющая мембрану, является MACPF домен.[9] Этот регион имеет гомологию с холестерин-зависимым цитолизины от грамположительных бактерий.[10]
Перфорин имеет структурное и функциональное сходство с дополнительный компонент 9 (С9). Как и C9, этот белок создает трансмембранный трубочки и способен неспецифически лизировать множество клеток-мишеней. Этот белок является одним из основных цитолитических белков цитолитических гранул и, как известно, является ключевой эффекторной молекулой для цитолиза, опосредованного Т-клетками и естественными клетками-киллерами.[7] Считается, что перфорин действует путем создания отверстий в плазматической мембране, что вызывает приток кальция и запускает механизмы восстановления мембраны. Эти механизмы восстановления переносят перфорин и гранзимы в ранние эндосомы.[11]
Клиническое значение
Гомозиготное наследование дефектных PRF1 аллели приводят к развитию семейный гемофагоцитарный лимфогистиоцитоз тип 2 (FHL2), редкое и летальное аутосомно-рецессивное заболевание младенчества.[7]
Взаимодействия
Перфорин был показан взаимодействовать с кальретикулин.[12]
Смотрите также
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000180644 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000037202 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Fink TM, Zimmer M, Weitz S, Tschopp J, Jenne DE, Lichter P (сентябрь 1992 г.). «Человеческий перфорин (PRF1) отображается на 10q22, область, которая является синтеничной с хромосомой 10 мыши». Геномика. 13 (4): 1300–2. Дои:10.1016/0888-7543(92)90050-3. PMID 1505959.
- ^ Синкай Й., Йошида М.С., Маэда К., Кобата Т., Маруяма К., Йодой Дж., Ягита Х., Окумура К. (январь 1990 г.). «Молекулярное клонирование и хромосомное отнесение гена перфорина человека (PFP)». Иммуногенетика. 30 (6): 452–7. Дои:10.1007 / BF02421177. PMID 2592021. S2CID 35292868.
- ^ а б c «Ген Entrez: перфорин 1 PRF1 (порообразующий белок)».
- ^ Трапани Дж. А. (1996). «Апоптоз клеток-мишеней, индуцированный цитотоксическими Т-клетками и естественными клетками-киллерами, включает синергию между порообразующим белком, перфорином, и сериновой протеазой, гранзимом В». Австралийский и новозеландский медицинский журнал. 25 (6): 793–9. Дои:10.1111 / j.1445-5994.1995.tb02883.x. PMID 8770355.
- ^ Чопп Дж, Массон Д., Стэнли К.К. (1986). «Структурное / функциональное сходство между белками, участвующими в цитолизе, опосредованном комплементом и цитотоксическими Т-лимфоцитами». Природа. 322 (6082): 831–4. Bibcode:1986Натура.322..831Т. Дои:10.1038 / 322831a0. PMID 2427956. S2CID 4330219.
- ^ Rosado CJ, Buckle AM, Law RH, Butcher RE, Kan WT, Bird CH, Ung K, Browne KA, Baran K, Bashtannyk-Puhalovich TA, Faux NG, Wong W, Porter CJ, Pike RN, Ellisdon AM, Pearce MC, Боттомли С.П., Эмсли Дж., Смит А.И., Россджон Дж., Хартланд Э.Л., Воскобойник И., Трапани Дж. А., Берд П.И., Данстон М.А., Уиссток Дж.С. (2007). «Общая складка опосредует защиту позвоночных и бактериальную атаку». Наука. 317 (5844): 1548–51. Bibcode:2007Научный ... 317.1548R. Дои:10.1126 / science.1144706. PMID 17717151. S2CID 20372720.
- ^ Тиери Дж., Киф Д., Булан С., Букро Э., Уолч М., Мартинвалет Д., Гопинг И.С., Блекли Р.С., Кирххаузен Т., Либерман Дж. (2011). «Поры перфорина в эндосомной мембране запускают высвобождение эндоцитированного гранзима B в цитозоль клеток-мишеней». Nat. Иммунол. 12 (8): 770–7. Дои:10.1038 / ni.2050. ЧВК 3140544. PMID 21685908.
- ^ Андрин С., Пинкоски М.Дж., Бернс К. и др. (Июль 1998 г.). «Взаимодействие между Ca2 +-связывающим белком кальретикулином и перфорином, компонентом цитотоксических Т-клеточных гранул». Биохимия. 37 (29): 10386–94. Дои:10.1021 / bi980595z. PMID 9671507.
дальнейшее чтение
- Трапани Дж. А. (1996). «Апоптоз клеток-мишеней, индуцированный цитотоксическими Т-клетками и естественными клетками-киллерами, включает синергию между порообразующим белком, перфорином, и сериновой протеазой, гранзимом В». Австралийский и новозеландский медицинский журнал. 25 (6): 793–9. Дои:10.1111 / j.1445-5994.1995.tb02883.x. PMID 8770355.
- Peitsch MC, Amiguet P, Guy R et al. (1990). «Локализация и молекулярное моделирование встроенного в мембрану домена девятого компонента человеческого комплемента и перфорина». Мол. Иммунол. 27 (7): 589–602. Дои:10.1016 / 0161-5890 (90) 90001-Г. PMID 2395434.
- Молодой JD, Хенгартнер H, Podack ER, Cohn ZA (1986). «Очистка и характеристика цитолитического порообразующего белка из гранул клонированных лимфоцитов с природной киллерной активностью». Клетка. 44 (6): 849–59. Дои:10.1016/0092-8674(86)90007-3. PMID 2420467. S2CID 30182487.
- Янг JD, Кон З.А., Podack ER (1986). «Девятый компонент комплемента и порообразующий белок (перфорин 1) из цитотоксических Т-клеток: структурное, иммунологическое и функциональное сходство». Наука. 233 (4760): 184–90. Дои:10.1126 / science.2425429. PMID 2425429.
- Лихтенхельд MG, Podack ER (1990). «Структура гена перфорина человека. Простая организация гена с интересными потенциальными регуляторными последовательностями». J. Immunol. 143 (12): 4267–74. PMID 2480391.
- Синкай Ю., Такио К., Окумура К. (1988). «Гомология перфорина девятому компоненту комплемента (C9)». Природа. 334 (6182): 525–7. Bibcode:1988Натура.334..525С. Дои:10.1038 / 334525a0. PMID 3261391. S2CID 4348928.
- Лихтенхельд М.Г., Олсен К.Дж., Лу П. и др. (1988). «Структура и функции перфорина человека». Природа. 335 (6189): 448–51. Bibcode:1988Натура.335..448л. Дои:10.1038 / 335448a0. PMID 3419519. S2CID 4359028.
- Goebel WS, Schloemer RH, Brahmi Z (1996). «Индуцированный клеткой-мишенью оборот мРНК перфорина в клетках NK3.3 опосредуется множеством элементов в кодирующей области мРНК». Мол. Иммунол. 33 (4–5): 341–9. Дои:10.1016/0161-5890(95)00155-7. PMID 8676885.
- Нёске К., Билзер Т., Планц О, Штиц Л. (1998). "Вирус-специфические CD4 + Т-клетки устраняют вирус болезни Борна из мозга посредством индукции цитотоксических CD8 + Т-клеток". Дж. Вирол. 72 (5): 4387–95. Дои:10.1128 / JVI.72.5.4387-4395.1998. ЧВК 109669. PMID 9557729.
- Андрин С., Пинкоски М.Дж., Бернс К. и др. (1998). «Взаимодействие между Ca2 +-связывающим белком кальретикулином и перфорином, компонентом цитотоксических Т-клеточных гранул». Биохимия. 37 (29): 10386–94. Дои:10.1021 / bi980595z. PMID 9671507.
- Ю. ЧР, Ортальдо Дж. Р., Куриэль Р. Э. и др. (1999). «Роль сайта связывания STAT в регуляции промотора перфорина человека». J. Immunol. 162 (5): 2785–90. PMID 10072525.
- Степп С.Е., Дюфурк-Лагелуз Р., Ле Деист Ф. и др. (1999). «Дефекты гена перфорина в семейном гемофагоцитарном лимфогистиоцитозе». Наука. 286 (5446): 1957–9. Дои:10.1126 / science.286.5446.1957. PMID 10583959.
- Такахаши Т., Ниеда М., Коэдзука Ю. и др. (2000). «Анализ человеческих V-альфа 24+ CD4 + NKT-клеток, активированных дендритными клетками, полученными из моноцитов с импульсным воздействием альфа-гликозилцерамида». J. Immunol. 164 (9): 4458–64. Дои:10.4049 / jimmunol.164.9.4458. PMID 10779745.
- Бадовинац В.П., Твиннереим А.Р., Харти Дж. Т. (2000). «Регулирование антиген-специфического гомеостаза CD8 + Т-клеток перфорином и интерфероном-гамма». Наука. 290 (5495): 1354–8. Bibcode:2000Sci ... 290.1354B. Дои:10.1126 / science.290.5495.1354. PMID 11082062.
- Горансдоттер Эриксон К., Фадил Б., Нильссон-Арднор С. и др. (2001). «Спектр мутаций гена перфорина при семейном гемофагоцитарном лимфогистиоцитозе». Являюсь. J. Hum. Genet. 68 (3): 590–7. Дои:10.1086/318796. ЧВК 1274472. PMID 11179007.
- Клементи Р., Цур Штадт Ю., Савольди Г. и др. (2002). «Шесть новых мутаций в гене PRF1 у детей с гемофагоцитарным лимфогистиоцитозом». J. Med. Genet. 38 (9): 643–6. Дои:10.1136 / jmg.38.9.643. ЧВК 1734943. PMID 11565555.
- Амбах А, Боннекох Б., Голльник Х (2001). «Высвобождение гранул перфорина из цитотоксических лимфоцитов ex vivo ингибируется циклоспорином, но не метотрексатом». Skin Pharmacol. Appl. Skin Physiol. 14 (5): 249–60. Дои:10.1159/000056355. PMID 11586066. S2CID 30142804.
внешняя ссылка
- перфорин в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)