Авторецептор - Autoreceptor
An ауторецептор это тип рецептор расположен в мембраны из пресинаптический нервные клетки. Он служит частью негативный отзыв зациклиться преобразование сигнала. Он чувствителен только к нейротрансмиттеры или же гормоны выпускается нейроном, на котором находится ауторецептор. Аналогично гетерорецептор чувствителен к нейротрансмиттерам и гормонам, которые не выделяются клеткой, на которой он сидит. Данный рецептор может действовать как ауторецептор или как гетерорецептор, в зависимости от типа передатчика, выделяемого клеткой, в которую он встроен.
Ауторецепторы могут располагаться в любой части клеточной мембраны: в дендриты, то Тело клетки, то аксон, или терминалы аксонов.[1]
Канонически пресинаптический нейрон выпускает нейротрансмиттер через синаптическая щель быть обнаруженным рецепторами постсинаптического нейрона. Ауторецепторы на пресинаптическом нейроне также обнаруживают этот нейромедиатор и часто функционируют, чтобы контролировать внутренние клеточные процессы, обычно подавляя дальнейшее высвобождение или синтез нейромедиатора. Таким образом, выброс нейротрансмиттера регулируется отрицательной обратной связью. Ауторецепторы обычно G-белковые рецепторы (скорее, чем ионные каналы, управляемые передатчиком ) и действовать через второй посланник.[2]
Примеры
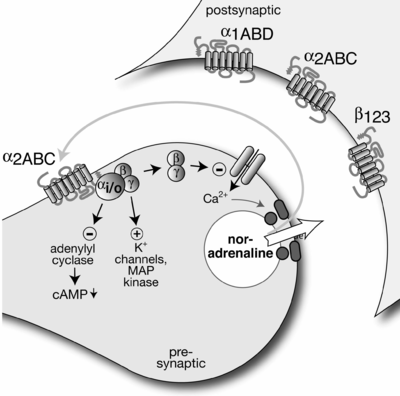
В качестве примера, норэпинефрин выпущенный из сочувствующий нейроны могут взаимодействовать с альфа-2А и альфа-2С-адренорецепторы для подавления дальнейшего высвобождения норадреналина. По аналогии, ацетилхолин выпущенный из парасимпатический нейроны могут взаимодействовать с M2 И м4 рецепторы для подавления дальнейшего высвобождения ацетилхолина. Нетипичный пример - β-адренергический ауторецептор в симпатическая периферическая нервная система, который действует на увеличивать выпуск передатчика.[1]
В D2sh ауторецептор взаимодействует с следовые аминовые рецепторы 1 (TAAR1), недавно обнаруженный GPCR, чтобы регулировать моноаминергические системы в головном мозге.[3] Активный TAAR1 противодействует активности ауторецепторов, инактивируя переносчик дофамина (DAT).[4] В своем обзоре TAAR1 в моноаминергический систем, Се и Миллер предложили эту схему: синаптический дофамин связывается с дофаминовым ауторецептором, который активирует DAT. Дофамин проникает в пресинаптические клетки и связывается с TAAR1, что увеличивает аденилилциклаза Мероприятия. Это в конечном итоге позволяет перевод из следы аминов в цитоплазме и активация циклические нуклеотидные ионные каналы, которые дополнительно активируют TAAR1 и сбрасывают дофамин в синапс. Через серию фосфорилирование события, связанные с PKA и PKC, активный TAAR1 инактивирует DAT, предотвращая захват дофамина из синапсов.[5] Наличие двух постсинаптических рецепторов с противоположными способностями к регулированию транспортер моноаминов функция позволяет регулировать моноаминергическую систему.
Также может снизиться активность ауторецепторов. облегчение парных импульсов (PPF).[нужна цитата ] Клетка обратной связи активируется (частично) деполяризованным постсинаптическим нейроном. Клетка обратной связи высвобождает нейротрансмиттер, к которому восприимчив ауторецептор пресинаптического нейрона. Ауторецептор вызывает ингибирование кальциевых каналов (замедление притока ионов кальция) и открытие калиевых каналов (увеличение оттока ионов калия) в пресинаптической мембране. Эти изменения в концентрации ионов эффективно уменьшают количество исходного нейромедиатора, высвобождаемого пресинаптическим окончанием в синаптическую щель. Это вызывает окончательное угнетение активности постсинаптического нейрона. Таким образом, цикл обратной связи завершен.

Рекомендации
- ^ а б Siegel GJ, Agranoff BW, Albers RW, et al., Eds. (1999). «Катехоламиновые рецепторы». Основы нейрохимии: молекулярные, клеточные и медицинские аспекты (6-е изд.). Липпинкотт-Рэйвен.
- ^ Медведь; Коннорс; Парадизо (2006). Нейробиология: исследование мозга (3-е изд.). п.119.
- ^ Се ц, В. С. (2007). "Сигнал рецептора 1, связанного с амином, следы обезьяны-резуса: усиление переносчиками моноаминов и ослабление ауторецептором D2 in vitro". Журнал фармакологии и экспериментальной терапии. 321 (1): 116–127. Дои:10.1124 / jpet.106.116863. PMID 17234900.
- ^ Се З, Уэстморленд С.В., Миллер Г.М. (2008). «Модуляция переносчиков моноаминов с помощью общих биогенных аминов через следовые амино-ассоциированные рецепторы 1 и ауторецепторы моноаминов в клетках 293 эмбриональной почки человека и синаптосомах мозга». Журнал фармакологии и экспериментальной терапии. 325 (2): 629–640. Дои:10.1124 / jpet.107.135079. PMID 18310473.
- ^ Се З, Миллер GM (2009). «Следы амино-ассоциированного рецептора 1 как моноаминергический модулятор в головном мозге». Биохимическая фармакология. 78 (9): 1095–1104. Дои:10.1016 / j.bcp.2009.05.031. ЧВК 2748138. PMID 19482011.
