Перегруппировка бензиловой кислоты - Benzilic acid rearrangement
В перегруппировка бензиловой кислоты формально 1,2-перегруппировка из 1,2-дикетоны сформировать α-гидрокси –карбоновые кислоты используя основание. Эта реакция получила свое название от реакции бензил с гидроксид калия формировать бензиловая кислота. Впервые в исполнении Юстус фон Либих в 1838 г.,[1] это первый зарегистрированный пример реакция перегруппировки.[2] Она стала классической реакцией в органическом синтезе и уже неоднократно рассматривалась ранее.[3][4][5] Его можно рассматривать как внутримолекулярный непропорциональность реакция, поскольку один углеродный центр окисляется, а другой восстанавливается.

Было показано, что реакция работает в ароматный, полуароматический, алифатический, и гетероциклический субстраты. Реакция лучше всего протекает, когда функциональные группы кетонов не имеют смежных энолизируемый протонов, поскольку это позволяет альдольная конденсация завершить. При использовании циклических дикетонов реакция формально представляет собой сокращение кольца. Было обнаружено, что арильные группы мигрируют легче, чем алкильные группы, и что арильные группы с электроноакцепторный группы мигрируют быстрее всех.
Механизм реакции
Реакция является представителем 1,2-перегруппировки. Давно установившаяся механизм реакции впервые был полностью предложен Кристофер Келк Ингольд, и был обновлен in silico данные[6] как указано ниже. В целом реакция протекает второго порядка по скорости, первого порядка по дикетону и первого порядка по основанию.
А гидроксид анион атакует один из кетон группы в 1 в нуклеофильное присоединение сформировать алкоксид 2. Следующий шаг требует вращения связки, чтобы конформер 3 что помещает мигрирующую группу R в позицию для атаки на вторую карбонильную группу. В согласованный На этапе мигрирующая группа R атакует -карбонильную группу, образуя другой алкоксид, с сопутствующим образованием кето-группы у другого углерода. Этот шаг миграции ставка определения. Эта последовательность напоминает нуклеофильное ацильное замещение. Расчеты показывают, что когда R равно метил накопление заряда на этой группе в переходное состояние может достигать 0,22, и что метильная группа расположена между центральной углеродной углеродной связью!


В карбоновая кислота в среднем 4 является менее основным, чем алкоксид, и поэтому имеет место обратимый перенос протона, благоприятствующий промежуточному 5 который протонируется при кислотной обработке до конечного α-гидрокси –карбоновая кислота 6. Расчеты показывают, что точное описание последовательности реакции возможно с участием 4 молекул воды, отвечающих за стабилизацию накопления заряда. Они также обеспечивают челнок для эффективного переноса одного протона с образованием промежуточных 5.
Вышеупомянутый механизм согласуется со всеми доступными экспериментальными данными.[3] В равновесие между видами 1 и 2 поддерживается 18О Изотопная маркировка эксперименты. В дейтерированная вода карбонильный кислородный обмен происходит намного быстрее, чем перегруппировка, что указывает на то, что первое равновесие не является этапом, определяющим скорость. Дальнейшие эксперименты показали более высокую относительную скорость в дейтерированной системе растворителей по сравнению с недейтерированной системой растворителей идентичного в остальном состава. Это объяснялось большей относительной основностью дейтерированного гидроксид-аниона по сравнению с нормальным гидроксид-анионом и использовалось для указания того, что миграции водорода не происходило на стадии, определяющей скорость реакции. Это исключало согласованный механизм реакции, поскольку перенос водорода мог бы происходить на этапе определения скорости.
Вариации
Перегруппировка бензилового эфира
Эта реакция идентична обычной перегруппировке бензиловой кислоты, за исключением того, что вместо гидроксид-иона используют алкоксид или амид-анион. Используемый алкоксид не должен быть легко окисляемым (например, этоксид калия ), поскольку это способствует Редукция Меервейна – Понндорфа – Верлея путь как побочная реакция. В целом реакция идет второго порядка по скорости, первого порядка по алкоксиду и первого порядка по дикетону. Продукт реакции представляет собой α-гидрокси –сложный эфир или α-гидрокси-амид.
Альфа-кетол перегруппировка
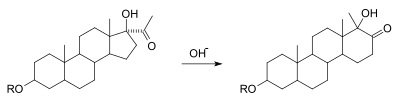
В альфа-кетол перегруппировка представляет собой взаимное превращение гидроксила альфа в карбонил к дополнительным карбонильным и гидроксильным группам с миграцией заместителя. Это механически эквивалентно перегруппировке бензилловой кислоты в точке после того, как нуклеофил атакует 1,2-дикарбонил. Это изменение реакции, как известно, происходит на многих подложках, несущих ацилоин функциональная группа. На рисунке ниже показан расширение кольца из циклопентана в циклогексановое кольцо в качестве примера реакции.[7][8]
Смотрите также
Рекомендации
- ^ Либих, Дж. (1838). "Theorie der organischen Verbindungen Уэбера Лорана". Annalen der Chemie. 25: 1–31. Дои:10.1002 / jlac.18380250102.
- ^ "Прекурсоры нервно-паралитического агента: бензиловая кислота и метилбензилат ", Информационные бюллетени по боевым химическим и биологическим агентам, химическим прекурсорам.
- ^ а б Selman, S .; Истхэм, Дж. (1960). "БЕНЗИЛИНОВАЯ КИСЛОТА И СООТВЕТСТВУЮЩИЕ ИЗМЕНЕНИЯ" Q. Rev. Chem. Soc. 14 (3): 221–235. Дои:10,1039 / qr9601400221.
- ^ Bowden, K .; Фабьен, В. М. Ф. (2001). «Реакции карбонильных соединений в основных растворах. Часть 36: Катализируемые основаниями реакции 1,2-дикарбонильных соединений». J. Phys. Орг. Chem. 14 (11): 794–796. Дои:10.1002 / poc.433.
- ^ Гилл, Г. Б. (1961). «Перегруппировки бензилбензиловой кислоты». Комп. Орг. Синтезатор. 3: 821–838.
- ^ Шиничи Ямабе; Норико Цучида и Шоко Ямазаки (2006). «Путь реакции, контролируемой FMO в перегруппировке бензил-бензиловой кислоты». J. Org. Chem. 71 (5): 1777–1783. Дои:10.1021 / jo051862r. PMID 16496961.
- ^ Убер-стероиды и половой гормон. 48. Mitteilung. Die Überführung von 17-Äthinyl-androsten-Derivaten в прегненон-производном. Herstellung des 17-Oxy-progesterons Helvetica Chimica Acta Том 21, выпуск 1, дата: 1938, Страницы: 1760–1770 Л. Ружичка, Х. Ф. Мельдаль Дои:10.1002 / hlca.193802101214
- ^ Убер-стероиды и половой гормон. (51. Mitteilung). Die Herstellung von Neo-прегненолон aus 5-3, 17-Dioxypregnenon- (20) Helvetica Chimica Acta Том 22, выпуск 1, дата: 1939, Страницы: 421–424 Л. Ружичка, Х. Ф. Мельдаль Дои:10.1002 / hlca.19390220155