Синтез ДНК - DNA synthesis

Синтез ДНК это естественное или искусственное создание дезоксирибонуклеиновая кислота (ДНК) молекулы. ДНК - это макромолекула состоит из нуклеотид единицы, которые связаны ковалентными связями и водородными связями, в повторяющейся структуре. Синтез ДНК происходит, когда эти нуклеотидные единицы соединяются вместе с образованием ДНК; это может происходить искусственно (in vitro) или естественно (in vivo). Нуклеотидные единицы состоят из азотистого основания (цитозин, гуанин, аденин или тимин), пентозного сахара (дезоксирибоза) и фосфатной группы. Каждая единица соединяется, когда между ее фосфатной группой и пентозным сахаром следующего нуклеотида образуется ковалентная связь, образуя сахарно-фосфатный остов. ДНК представляет собой комплементарную двухцепочечную структуру, поскольку специфическое спаривание оснований (аденин и тимин, гуанин и цитозин) происходит естественным образом, когда между нуклеотидными основаниями образуются водородные связи.
Есть несколько разных определений синтеза ДНК: он может относиться к Репликация ДНК - биосинтез ДНК (in vivo Амплификация ДНК), полимеразной цепной реакции - ферментативный синтез ДНК (in vitro Амплификация ДНК) или синтез генов - физически создающий искусственные генные последовательности. Хотя каждый тип синтеза очень отличается, у них действительно есть некоторые общие черты: нуклеотиды, которые были соединены для образования полинуклеотиды может действовать как матрица ДНК для одной формы синтеза ДНК - ПЦР. Репликация ДНК также работает с использованием шаблона ДНК, двойная спираль ДНК раскручивается во время репликации, подвергая неспаренные основания для новых нуклеотидов водородной связи. Однако для синтеза генов не требуется матрица ДНК, и гены собираются. de novo.
Синтез ДНК происходит во всех эукариоты и прокариоты, а также некоторые вирусы. Точный синтез ДНК важен для предотвращения мутаций ДНК. У людей мутации могут приводить к таким заболеваниям, как рак, поэтому синтез ДНК и задействованные механизмы in vivo, широко изучалась на протяжении десятилетий. В будущем эти исследования могут быть использованы для разработки технологий, включающих синтез ДНК, которые будут использоваться для хранения данных.
Репликация ДНК


В природе молекулы ДНК синтезируются всеми живыми клетками в процессе репликации ДНК. Обычно это происходит при делении клеток. Репликация ДНК происходит так, что во время деления клетки каждая дочерняя клетка содержит точную копию генетического материала клетки. В естественных условиях Синтез ДНК (репликация ДНК) зависит от сложного набора ферментов, которые эволюционировали, чтобы действовать во время Фаза S клеточного цикла согласованным образом. И у эукариот, и у прокариот репликация ДНК происходит, когда специфические топоизомеразы, геликазы и гиразы (белки-инициаторы репликации) разматывать двухцепочечная ДНК, обнажающая азотистые основания.[1] Эти ферменты вместе с дополнительными белками образуют макромолекулярную машину, которая обеспечивает точное дублирование последовательностей ДНК. Происходит комплементарное спаривание оснований, образуя новую двухцепочечную молекулу ДНК. Это известно как полуконсервативный репликация, поскольку одна цепь новой молекулы ДНК происходит от «родительской» цепи.
Эукариотические ферменты постоянно сталкиваются с повреждениями ДНК, которые могут нарушить репликацию ДНК. Это повреждение имеет форму повреждений ДНК, которые возникают спонтанно или из-за агентов, повреждающих ДНК. Поэтому механизмы репликации ДНК строго контролируются, чтобы предотвратить коллапс при повреждении.[2] Контроль системы репликации ДНК гарантирует, что геном реплицируется только один раз за цикл; чрезмерная репликация вызывает повреждение ДНК. Нарушение регуляции репликации ДНК является ключевым фактором нестабильности генома во время развития рака.[3]
Это подчеркивает специфику механизма синтеза ДНК. in vivo. Существуют различные способы искусственного стимулирования репликации естественной ДНК или создания искусственных генных последовательностей. Однако синтез ДНК in vitro может быть очень подверженным ошибкам процессом.
Синтез репарации ДНК
Поврежденная ДНК подлежит ремонту несколькими разными ферментативные процессы восстановления, где каждый отдельный процесс специализируется на устранении определенных типов повреждений. ДНК человека может быть повреждена из нескольких природных источников, и недостаточное восстановление связано с болезнями и преждевременное старение.[4] Большинство процессов репарации ДНК формируют одноцепочечные разрывы в ДНК на промежуточной стадии репарации, и эти разрывы заполняются репарационным синтезом.[4] Конкретные процессы репарации, требующие заполнения пробелов путем синтеза ДНК, включают: эксцизионная репарация нуклеотидов, базовая эксцизионная пластика, ремонт несоответствия, гомологичный рекомбинационный ремонт, негомологичное соединение концов и соединение концов, опосредованное микрогомологией.
Обратная транскрипция
Обратная транскрипция является частью цикла репликации определенных семейств вирусов, включая ретровирусы. Он включает копирование РНК в двухцепочечную комплементарную ДНК (кДНК) с использованием обратная транскриптаза ферменты. В ретровирусах вирусная РНК вставляется в ядро клетки-хозяина. Там фермент обратной транскриптазы вируса добавляет нуклеотиды ДНК к последовательности РНК, генерируя кДНК, которая вставляется в геном клетки-хозяина ферментом. интегрировать, кодирующие вирусные белки.[5]
Полимеразной цепной реакции
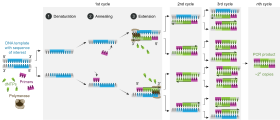
А полимеразной цепной реакции представляет собой форму ферментативного синтеза ДНК в лаборатории с использованием циклов повторного нагрева и охлаждения реакции для Плавление ДНК и ферментативная репликация ДНК.
Синтез ДНК во время ПЦР очень похож на синтез живых клеток, но имеет очень специфические реагенты и условия. Во время ПЦР ДНК химически извлекается из белков-шаперонов хозяина, затем нагревается, вызывая термическую диссоциацию нитей ДНК. Две новые цепи кДНК построены из исходной цепи, эти цепи можно снова разделить, чтобы они действовали как матрица для других продуктов ПЦР. Исходная ДНК размножается с помощью многих раундов ПЦР.[1] Можно сделать более миллиарда копий исходной цепи ДНК.
Случайный мутагенез
Для многих экспериментов, таких как структурные и эволюционные исследования, ученым необходимо создать большую библиотеку вариантов определенной последовательности ДНК. Случайный мутагенез происходит in vitro, когда мутагенная репликация с использованием ДНК-полимеразы низкой точности сочетается с селективной амплификацией ПЦР для получения множества копий мутантной ДНК.[6]
ОТ-ПЦР
ОТ-ПЦР отличается от обычной ПЦР тем, что синтезирует кДНК из мРНК, а не из матричной ДНК. Этот метод сочетает реакцию обратной транскрипции с амплификацией на основе ПЦР, поскольку последовательность РНК действует как матрица для фермента обратной транскриптазы. ОТ-ПЦР часто используется для проверки экспрессии генов в определенных тканях или типах клеток на различных стадиях развития или для проверки генетических нарушений.[7]
Синтез генов
Искусственный синтез генов это процесс синтеза ген in vitro без необходимости в первичных образцах матричной ДНК. в 2010 г. Дж. Крейг Вентер и его команда были первыми, кто использовал полностью синтезированную ДНК для создания самовоспроизводящегося микроба, получившего название Лаборатория микоплазм.[8]
Синтез олигонуклеотидов
Синтез олигонуклеотидов это химический синтез последовательностей нуклеиновых кислот. Большинство биологических исследований и биоинженерии включает синтетическую ДНК, которая может включать олигонуклеотиды, синтетические гены или даже хромосомы. Сегодня вся синтетическая ДНК создается на заказ с использованием фосфорамидитного метода. Марвин Х. Карутерс. Олиго синтезируются из строительных блоков, которые копируют природные основы. Этот процесс автоматизирован с конца 1970-х годов и может использоваться для формирования желаемых генетических последовательностей, а также для других целей в медицине и молекулярной биологии. Однако создание последовательностей химическим путем нецелесообразно за пределами 200–300 оснований и является экологически опасным процессом. Эти олигонуклеотиды, состоящие примерно из 200 оснований, могут быть связаны с использованием методов сборки ДНК, создавая более крупные молекулы ДНК.[9]
Некоторые исследования изучали возможность ферментативного синтеза с использованием терминальная дезоксинуклеотидилтрансфераза (TdT), ДНК-полимераза, не требующая матрицы. Однако этот метод еще не так эффективен, как химический синтез, и коммерчески недоступен.[10]
С развитием искусственного синтеза ДНК изучается возможность хранения данных ДНК. Благодаря сверхвысокой плотности хранения и долговременной стабильности синтетическая ДНК представляет собой интересный вариант для хранения больших объемов данных. Хотя информацию можно очень быстро получить из ДНК с помощью технологий секвенирования нового поколения, синтез ДНК de novo является основным узким местом в этом процессе. За цикл можно добавить только один нуклеотид, причем каждый цикл занимает секунды, поэтому общий синтез занимает очень много времени, а также очень подвержен ошибкам. Однако, если биотехнология улучшится, синтетическая ДНК однажды может быть использована для хранения данных.[11]
Синтез пары оснований
Сообщается, что новые азотистое основание пары могут быть синтезированы, а также A-T (аденин - тимин ) и G-C (гуанин - цитозин ). Синтетические нуклеотиды могут использоваться для расширения генетического алфавита и обеспечения специфической модификации участков ДНК. Даже всего лишь третья пара оснований увеличила бы количество аминокислот, которые могут кодироваться ДНК, с существующих 20 аминокислот до возможных 172.[8] ДНК Хатимодзи состоит из восьми букв нуклеотидов, образующих четыре возможных пары оснований. Таким образом, это вдвое больше плотности информации естественной ДНК. Согласно исследованиям, РНК даже была произведена из ДНК хатимоджи. Эта технология также может использоваться для хранения данных в ДНК.[12]
Рекомендации
- ^ а б Пельт-Веркуил, Эван (2008). «Краткое сравнение между репликацией ДНК in vivo и амплификацией ПЦР in vitro». Принципы и технические аспекты амплификации ПЦР (PDF). Роттердам: Springer, Нидерланды. С. 9–15. Дои:10.1007/978-1-4020-6241-4_2. ISBN 978-1-4020-6240-7. S2CID 215257488.
- ^ Patel, Darshil R .; Вайс, Роберт С. (2018). «Трудная ссора: когда репликационные вилки сталкиваются с повреждением ДНК». Biochem Soc Trans. 46 (6): 1643–1651. Дои:10.1042 / BST20180308. ЧВК 6487187. PMID 30514768.
- ^ Ройссвиг, Карл-Уве; Пфандер, Борис (2019). «Контроль инициации репликации эукариотической ДНК - механизмы обеспечения плавных переходов». Гены (Базель). 10 (2): 99. Дои:10.3390 / гены10020099. ЧВК 6409694. PMID 30700044.
- ^ а б Тивари V, Уилсон DM 3-й. Повреждение ДНК и связанные с ним дефекты репарации ДНК при заболеваниях и преждевременном старении. Am J Hum Genet. 2019 1 августа; 105 (2): 237-257. DOI: 10.1016 / j.ajhg.2019.06.005. Рассмотрение. PMID: 31374202
- ^ Хьюз, Стивен Х (2015). «Обратная транскрипция ретровирусов и ретротранспозонов LTR». Микробиологический спектр. 3 (2): 1051–1077. Дои:10.1128 / microbiolspec.MDNA3-0027-2014. ISBN 9781555819200. ЧВК 6775776. PMID 26104704.
- ^ Форлони, М (2018). «Случайный мутагенез с использованием ДНК-полимераз, подверженных ошибкам». Холодный источник Харб Проток. 2018 (3): pdb.prot097741. Дои:10.1101 / pdb.prot097741. PMID 29496818.
- ^ Бахман, Юлия (2013). «Глава вторая - ПЦР с обратной транскрипцией (ОТ-ПЦР)». Методы в энзимологии. 530: 67–74. Дои:10.1016 / B978-0-12-420037-1.00002-6. PMID 24034314.
- ^ а б Файкс, Брэдли Дж. (8 мая 2014 г.). «Жизнь, созданная с помощью расширенного генетического кода». Сан-Диего Union Tribune. Архивировано из оригинал 9 мая 2014 г.. Получено 8 мая 2014.
- ^ Паллюк, Себастьян; Арлоу, Дэниел Х; и другие. (2018). «Синтез ДНК de novo с использованием конъюгатов полимераза-нуклеотид». Природа Биотехнологии. 36 (7): 645–650. Дои:10.1038 / nbt.4173. OSTI 1461176. PMID 29912208. S2CID 49271982.
- ^ Перкель, Джеффри М. (2019). «Гонка за ферментативный синтез ДНК накаляется». Природа. 566 (7745): 565. Дои:10.1038 / d41586-019-00682-0. PMID 30804572.
- ^ Табатабаи, С. Касра (2020). «Перфокарты ДНК для хранения данных о нативных последовательностях ДНК с помощью ферментативного разрезания». Nature Communications. 11 (1): 1742. Дои:10.1038 / s41467-020-15588-z. ЧВК 7142088. PMID 32269230.
- ^ Хошика, Шуичи (2020). «ДНК и РНК Хатимодзи. Генетическая система с восемью строительными блоками». Наука. 363 (6429): 884–887. Дои:10.1126 / science.aat0971. ЧВК 6413494. PMID 30792304.
