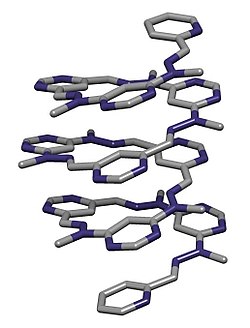
Фолдамер - Foldamer
В химия, а фолдамер представляет собой дискретную цепную молекулу или олигомер который складывается в конформационно упорядоченное состояние в растворе. Это искусственные молекулы, имитирующие способность белки, нуклеиновые кислоты, и полисахариды к складывать в четко определенные конформации, такие как спирали и β-листы. Структура фолдамера стабилизирована нековалентные взаимодействия между несмежными мономеры.[2][3] Фолдамеры изучаются с основной целью конструирования больших молекул с предсказуемой структурой. Изучение фолдамеров связано с темой молекулярная самосборка, молекулярное распознавание и химия хозяин – гость.
Дизайн

Фолдамеры могут различаться по размеру, но они определяются наличием нековалентных несмежных взаимодействий. Это определение исключает такие молекулы, как поли (изоцианаты) (широко известные как (полиуретан )) и поли (пролины) поскольку они надежно складываются в спирали за счет соседний ковалентные взаимодействия.,[4] Фолдамеры имеют динамическую реакцию сворачивания [развернутый → свернутый], в которой крупное макроскопическое сворачивание вызвано сольвофобными эффектами (гидрофобный коллапс), в то время как конечное энергетическое состояние свернутого фолдамера обусловлено нековалентными взаимодействиями. Эти взаимодействия работают совместно, чтобы сформировать наиболее стабильную третичную структуру, поскольку полностью свернутые и развернутые состояния более стабильны, чем любые частично свернутые состояния.[5]
Прогнозирование складывания
Структуру фолдамера часто можно предсказать по его первичная последовательность. Этот процесс включает динамическое моделирование равновесия сворачивания на атомном уровне при различных условиях. Этот тип анализа может быть применен и к небольшим белкам, однако вычислительная технология не может моделировать все последовательности, кроме самых коротких.[6]
Путь сворачивания фолдамера может быть определен путем измерения отклонения от экспериментально определенной предпочтительной структуры при различных термодинамических и кинетический условия. Изменение структуры измеряется путем расчета среднеквадратическое значение отклонение от основного атомного положения предпочтительной структуры. Структура фолдамера в различных условиях может быть определена расчетным путем, а затем подтверждена экспериментально. Изменения температуры, растворителя вязкость, давление, pH, и концентрация соли может дать ценную информацию о структуре фолдамера. Измерение кинетики сворачивания, а также равновесия сворачивания позволяет наблюдать эффекты этих различных условий на структуру фолдамера.[6]
Растворитель часто влияет на сворачивание. Например, путь сворачивания с участием гидрофобный коллапс сложится иначе в неполярный растворитель. Это различие связано с тем, что разные растворители стабилизируют разные промежуточные соединения пути сворачивания, а также разные конечные структуры фолдамеров на основе межмолекулярный нековалентные взаимодействия.[6]
Нековалентные взаимодействия
Нековалентный межмолекулярный взаимодействия, хотя и небольшие по отдельности, их суммирование существенно меняет химические реакции. Ниже перечислены общие межмолекулярные силы, которые химики использовали для создания фолдамеров.
- Водородная связь (особенно с пептидные связи )
- Укладка пи
- Сольвофобный эффекты, которые приводят к гидрофобный коллапс
- Силы Ван-дер-Ваальса
- Электростатическое притяжение
Общие конструкции
Фолдамеры делятся на три разные категории: пептидомиметик фолдамеры, нуклеотидомиметические фолдамеры и абиотические фолдамеры. Пептидомиметические фолдамеры - это синтетические молекулы, имитирующие структуру белков, а нуклеотидомиметические фолдамеры основаны на взаимодействиях в нуклеиновых кислотах. Абиотические фолдамеры стабилизируются ароматическими взаимодействиями и взаимодействиями с переносом заряда, которые обычно не встречаются в природе.[2] Три описанные ниже конструкции отклоняются от схемы Мура.[3] строгое определение фолдамера, которое исключает спиральные фолдамеры.
Пептидомиметик
Пептидомиметические фолдамеры часто нарушают ранее упомянутое определение фолдамеров, поскольку они часто принимают спиральный конструкции. Благодаря своему дизайну и возможностям они представляют собой важную веху в исследованиях фолдамеров.[7][8] Самые большие группы пептидомиметиков состоят из β - пептиды, γ - пептиды и δ - пептиды, а также возможные мономерные комбинации.[8] В аминокислоты Эти пептиды различаются только одним (β), двумя (γ) или тремя (δ) атомами углерода в метилене, но структурные изменения были глубокими. Эти пептидные последовательности хорошо изучены, поскольку контроль последовательности приводит к надежному предсказанию сворачивания. Кроме того, с несколькими метилен атомы углерода между карбоксил и амино- концы фланкирующих пептидных связей, могут быть сконструированы различные боковые цепи группы R. Один из примеров новизны β-пептидов можно увидеть в исследованиях Райзера и его коллег.[9] Используя гетеролигопептид, состоящий из α-аминокислот и цис-β-аминоциклопропанкарбоновых кислот (цис-β-АСС), они обнаружили образование спиральных последовательностей в олигомерах длиной всего семь остатков и определенную конформацию в пяти остатках; уникальное качество пептидов, содержащих циклические β-аминокислоты.[10][11][12][13]
Нуклеотидомиметик
Нуклеотидомиметики обычно не квалифицируются как фолдамеры. Большинство из них предназначены для имитации отдельных оснований ДНК, нуклеозиды, или же нуклеотиды для неспецифического воздействия на ДНК.[14][15][16] Они имеют несколько различных медицинских применений, в том числе противораковый, противовирусное средство, и противогрибковый Приложения.
Абиотический

Абиотические фолдамеры снова представляют собой органические молекулы, предназначенные для динамического сворачивания. Они используют одно или несколько известных ключевых межмолекулярных взаимодействий, оптимизированных их конструкцией. Одним из примеров является олигопирролы которые организуются при связывании анионов, таких как хлорид, посредством водородных связей (см. рисунок). Сворачивание индуцируется в присутствии аниона: в противном случае полипиррольные группы имеют небольшие конформационные ограничения.[17][18]
Другие примеры
- м-Фениленэтиниленовые олигомеры складываются в спиральную конформацию за счет сольвофобные силы и ароматическая укладка взаимодействия.
- β-пептиды состоят из аминокислоты содержащий дополнительный CH
2 единица измерения между амин и карбоновая кислота. Они более устойчивы к ферментативный деградации и продемонстрировали антимикробную активность. - Пептоиды находятся N-замещенные полиглицины, которые используют стерические взаимодействия для сворачивания в спиральные структуры, подобные полипролину I типа.[19]
- Aedamers которые складываются в водных растворах за счет гидрофобных и ароматических взаимодействий.
- Ароматические олигоамидные фолдамеры Эти примеры являются одними из крупнейших и наиболее структурно охарактеризованных фолдамеров.[20]
- Ариламид фолдамеры,[21] например Брилацидин
Рекомендации
- ^ Лен, Жан-Мари; и другие. (2003). «Закодированные спиральностью молекулярные нити: эффективный доступ по гидразоновому маршруту и структурным особенностям». Helv. Чим. Acta. 86 (5): 1598–1624. Дои:10.1002 / hlca.200390137.
- ^ а б «Фолдамеры: структура, свойства и применение» Стефан Хехт, Иван Хук Ред. Wiley-VCH, Weinheim, 2007. ISBN 9783527315635
- ^ а б Hill, D.J .; Mio, M. J .; Prince, R. B .; Hughes, T. S .; Мур, Дж. С. (2001). «Полевой справочник по фолдамеру». Chem. Rev. 101 (12): 3893–4012. Дои:10.1021 / cr990120t. PMID 11740924.
- ^ Грин, М. М .; Park, J .; Сато, Т .; Терамото, А .; Лифсон, С .; Селинджер, Р. Л. Б .; Селинджер, Дж. В. (1999). «Макромолекулярный путь к хиральной амплификации». Энгью. Chem. Int. Эд. 38 (21): 3138–3154. Дои:10.1002 / (SICI) 1521-3773 (19991102) 38:21 <3138 :: AID-ANIE3138> 3.0.CO; 2-C.
- ^ Геллман, С. (1998). «Фолдамеры: манифест». Соотв. Chem. Res. 31 (4): 173–180. Дои:10.1021 / ar960298r.
- ^ а б c ван Гунстерен, Уилфред Ф. (2007). Фолдамеры: структура, свойства и применение; Моделирование складывающихся равновесий.. Wiley-VCH Verlag GmbH & Co. KGaA. С. 173–192. Дои:10.1002 / 9783527611478.ch6.
- ^ Анслин и Догерти, Современная физическая органическая химия, University Science Books, 2006 г., ISBN 978-1-891389-31-3
- ^ а б Martinek, T.A .; Фулоп, Ф. (2012). «Пептидные фолдамеры: увеличение разнообразия». Chem. Soc. Rev. 41 (2): 687–702. Дои:10.1039 / C1CS15097A. PMID 21769415.
- ^ De Pol, S .; Zorn, C .; Klein, C.D .; Зербе, О .; Райзер, О. (2004). «Удивительно стабильные спиральные конформации в альфа / бета-пептидах за счет включения цис-бета-аминоциклопропаткарбоновых кислот». Энгью. Chem. Int. Эд. 43 (4): 511–514. Дои:10.1002 / anie.200352267. PMID 14735548.
- ^ Seebach, D .; Бек, А.К .; Bierbaum, D. J .; Chem. Биодив., 2004, 1, 1111-1239.
- ^ Seebach, D .; Бек, А.К .; Бирбаум, Д.Дж. (2004). «Химические и биологические исследования B-олигоаргининов». Химия и биоразнообразие. 1 (1): 1111–1239. Дои:10.1002 / cbdv.200490014. PMID 17191776.
- ^ Низами, Билал. "FoldamerDB: База данных фолдамеров". foldamerdb.ttk.hu. Получено 2020-07-06.
- ^ Низами, Билал; Берецки-Сакаль, Дороття; Варро, Николетт; эль-Баттиуи, Камаль; Nagaraj, Vignesh U .; Szigyártó, Imola Cs; Мандити, Иштван; Беке-Сомфаи, Тамаш (2020-01-08). «FoldamerDB: база данных пептидных фолдамеров». Исследования нуклеиновых кислот. 48 (D1): D1122 – D1128. Дои:10.1093 / нар / gkz993. ISSN 0305-1048.
- ^ Лонгли, ДБ; Харкин Д.П .; Джонстон PG (май 2003 г.). «5-фторурацил: механизмы действия и клинические стратегии». Nat. Преподобный Рак. 3 (5): 330–338. Дои:10.1038 / nrc1074. PMID 12724731.
- ^ Секрист, Джон (2005). «Нуклеозиды как противоопухолевые средства: от концепции до клиники». Серия симпозиумов по нуклеиновым кислотам. 49 (49): 15–16. Дои:10.1093 / nass / 49.1.15. PMID 17150610.
- ^ Rapaport, E .; Фонтейн Дж (1989). «Противораковая активность адениновых нуклеотидов у мышей опосредуется увеличением пулов АТФ в эритроцитах». Proc. Natl. Акад. Sci. Соединенные Штаты Америки. 86 (5): 1662–1666. Bibcode:1989PNAS ... 86.1662R. Дои:10.1073 / pnas.86.5.1662. ЧВК 286759. PMID 2922403.
- ^ Sessler, J.L .; Cyr, M .; Линч, В. (1990). "Синтетические и структурные исследования сапфирина, пентапирролового соединения с 22-пи-электронами" расширенного порфирина."". Варенье. Chem. Soc. 112 (7): 2810. Дои:10.1021 / ja00163a059.
- ^ Juwarker, H .; Чон, К.С. (2010). «Фолдамеры с анионным управлением». Chem. Soc. Rev. 39 (10): 3664–3674. Дои:10.1039 / b926162c. PMID 20730154.
- ^ Angelici, G .; Bhattacharjee, N .; Рой, О .; Faure, S .; Didierjean, C .; Jouffret, L .; Jolibois, F .; Perrin, L .; Тайллефюмье, К. (2016). "Слабая основная цепь CH ⋯ O = C и боковая цепь тBu ⋯тВзаимодействия Bu London способствуют свертыванию спирали ахирального NтБу пептоиды ». Химические коммуникации. 52 (24): 4573–4576. Дои:10.1039 / C6CC00375C. PMID 26940758.
- ^ Дельсук, Николас; Массип, Стефан; Леже, Жан-Мишель; Кауфманн, Брайс; Хук, Иван (9 марта 2011 г.). «Относительные спирали-спиральные конформации в разветвленных ароматических олигоамидных фолдамерах». Журнал Американского химического общества. 133 (9): 3165–3172. Дои:10.1021 / ja110677a. PMID 21306159.
- ^ Дизайн de novo и активность in vivo конформационно ограниченных антимикробных фолдамеров ариламида. Чой. 2009 г.
дальнейшее чтение
- Иван Гюк; Стефан Хехт (2007). Фолдамеры: структура, свойства и применение. Вайнхайм: Wiley-VCH. ISBN 978-3-527-31563-5.
- Гудман С.М., Чой С., Шандлер С., ДеГрадо В.Ф. (2007). «Фолдамеры как универсальные рамки для дизайна и развития функций». Nat. Chem. Биол. 3 (5): 252–62. Дои:10.1038 / nchembio876. ЧВК 3810020. PMID 17438550.
Отзывы
- ^ Геллман, С. (1998). «Фолдамеры: манифест» (PDF). Соотв. Chem. Res. 31 (4): 173–180. Дои:10.1021 / ar960298r. Архивировано из оригинал (PDF) на 2008-05-13.
- ^ Чжан Д.В., Чжао X, Хоу Дж.Л., Ли З.Т. (2012). «Ароматические амидные фолдамеры: структуры, свойства и функции». Chem. Rev. 112 (10): 5271–5316. Дои:10.1021 / cr300116k. PMID 22871167.
- ^ Juwarker, H .; Чон, К.С. (2010). «Фолдамеры с анионным управлением». Chem. Soc. Rev. 39 (10): 3664–3674. Дои:10.1039 / b926162c. PMID 20730154.