Иммунный контрольно-пропускной пункт - Immune checkpoint
Эта статья слишком полагается на Рекомендации к основные источники. (Ноябрь 2018) (Узнайте, как и когда удалить этот шаблон сообщения) |


Иммунные контрольные точки являются регуляторами иммунная система. Эти пути имеют решающее значение для терпимость, что предотвращает беспорядочную атаку иммунной системы клеток. Однако некоторые виды рака могут защитить себя от нападения, стимулируя иммунные контрольные точки.[1]
Молекулы ингибиторных контрольных точек являются мишенями для иммунотерапия рака из-за их потенциала для использования при нескольких типах рака. В настоящее время одобрено ингибиторы контрольных точек блокировать CTLA4 и ПД-1 и PD-L1. За связанные открытия фундаментальной науки Джеймс П. Эллисон и Тасуку Хондзё выиграл Премия Тан в области биофармацевтической науки и Нобелевская премия по физиологии и медицине в 2018 году.[2][3]
Стимулирующие молекулы контрольных точек
Четыре молекулы стимулирующих контрольных точек являются членами суперсемейство рецепторов фактора некроза опухолей (TNF) -CD27, CD40, OX40, GITR и CD137. Еще две молекулы стимулирующих контрольных точек относятся к суперсемейству B7-CD28 - собственно CD28 и ICOS.
- CD27: Эта молекула поддерживает антиген-специфическую экспансию наивных Т-клеток и жизненно важна для генерации Т-клеточной памяти.[4] CD27 также является маркером памяти В-клеток.[5] Активность CD27 регулируется временной доступностью его лиганда, CD70, на лимфоцитах и дендритных клетках.[6] Известно, что костимуляция CD27 подавляет Чт17 функция эффекторных клеток.[7] Американская биотехнологическая компания Celldex Therapeutics работает над CDX-1127, агонистическим анти-CD27. моноклональное антитело[8] которые на животных моделях показали свою эффективность в контексте стимуляции рецепторов Т-клеток.[9]
- CD28: Эта молекула конститутивно экспрессируется почти на всех CD4 + Т-клетках человека и примерно на половине всех Т-лимфоцитов CD8. Связывание с двумя его лигандами CD80 и CD86, экспрессируемый на дендритных клетках, вызывает экспансию Т-клеток. CD28 был целью TGN1412 «суперагонист», который вызвал серьезные воспалительные реакции в первом исследовании с участием человека в Лондоне в марте 2006 года.[10]
- CD40: Эта молекула содержится в различных клетках иммунной системы, включая антигенпрезентирующие клетки имеет CD40L, иначе известный как CD154 и временно экспрессируется на поверхности активированных CD4 + Т-клеток в качестве лиганда. Известно, что передача сигнала CD40 «лицензирует» дендритные клетки для созревания и тем самым запускает активацию и дифференцировку Т-клеток.[11] Ныне несуществующая биотехнологическая компания из Сиэтла под названием VLST получила лицензию на моноклональные антитела к агонистам CD40 от Pfizer в 2012 году. Швейцарская фармацевтическая компания. Рош приобрел этот проект после закрытия VLST в 2013 году.[12]
- CD122: Эта молекула, которая является Рецептор интерлейкина-2 бета-субъединица, как известно, увеличивает пролиферацию эффекторных Т-клеток CD8 +.[13] Американская биотехнологическая компания Nektar Therapeutics работает над NKTR-214, иммуностимулирующим цитокином, связанным с CD122.[14] Результаты этапа I объявлены в ноябре 2016 года.[15]
- CD137: Когда эта молекула, также называемая 4-1BB, связывается лигандом CD137, результатом является пролиферация Т-клеток. Также известно, что передача сигналов, опосредованная CD137, защищает Т-клетки, и в частности CD8 + Т-клетки, от гибели клеток, вызванной активацией.[16] Немецкая биотехнологическая компания Pieris Pharmaceuticals разработала инженерный липокалин который является би-специфичным для CD137 и HER2.[17]
- OX40: Эта молекула, также называемая CD134, имеет OX40L или CD252 в качестве лиганда. Как и CD27, OX40 способствует размножению эффекторных Т-клеток и Т-клеток памяти, однако он также известен своей способностью подавлять дифференцировку и активность Т-регуляторных клеток, а также регулировать выработку цитокинов.[18] Ценность OX40 как лекарственной мишени в первую очередь заключается в том, что, будучи временно экспрессируемым после взаимодействия с Т-клеточным рецептором, он активируется только на самых недавно активированных антигеном Т-клетках в воспалительных поражениях.[19] Было показано, что моноклональные антитела против OX40 имеют клиническое применение при запущенном раке.[20] Фармацевтическая компания АстраЗенека в разработке находятся три препарата, нацеленных на OX40: MEDI0562 - гуманизированный агонист OX40; MEDI6469, мышиный агонист OX4; и MEDI6383, агонист OX40[21]
- GITR: сокращение от Glucocorticoid-Induced TNFR family Родственный ген, вызывает экспансию Т-клеток, включая экспансию Treg.[22] Лиганд GITR в основном экспрессируется на антигенпрезентирующие клетки.[23] Было показано, что антитела к GITR способствуют противоопухолевому ответу за счет потери стабильности линии Treg.[24] Биотехнологическая компания TG Therapeutics работает над антителами против GITR.[25]
- ICOS: Эта молекула, сокращенно от Inducible T-cell costimulator, также называемая CD278, экспрессируется на активированных Т-клетках. Его лиганд - ICOSL, экспрессируется в основном на В-клетках и дендритных клетках. Эта молекула играет важную роль в эффекторной функции Т-клеток.[26] Американская биотехнологическая компания Jounce Therapeutics разрабатывает агонист ICOS.
Тормозные молекулы контрольной точки
- A2AR: Рецептор аденозина A2A считается важной контрольной точкой в терапии рака, потому что аденозин в иммунном микроокружении, приводящий к активации рецептора A2a, является петлей отрицательной иммунной обратной связи, а в микроокружении опухоли есть относительно высокие концентрации аденозина.[27]
- B7-H3: также называемый CD276, первоначально предполагалось, что это костимуляторная молекула[28] но теперь считается со-ингибитором.[29] Американская биотехнологическая компания MacroGenics работает над MGA271 - Fc-оптимизированным моноклональным антителом, нацеленным на B7-H3.[30] Рецепторы B7-H3 еще не идентифицированы.[31]
- B7-H4: также называется VTCN1, экспрессируется опухолевыми клетками и ассоциированными с опухолью макрофагами и играет роль в ускользании от опухоли.[32]
- BTLA: Эта молекула, сокращение от аттенюатора лимфоцитов B и T и также называемая CD272, имеет HVEM (медиатор проникновения герпесвируса) в качестве лиганда. Поверхностная экспрессия BTLA постепенно снижается во время дифференцировки CD8 + T-клеток человека от фенотипа наивных до эффекторных клеток, однако опухолеспецифические человеческие CD8 + T-клетки экспрессируют высокие уровни BTLA.[33]
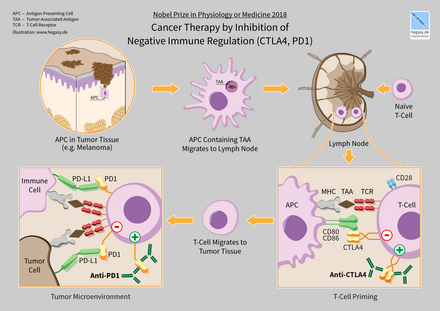
- CTLA-4: сокращение от Cytotoxic T-Lymphocyte-Associated protein 4, также называемого CD152, является мишенью Бристоль-Майерс Сквибб лекарство от меланомы Yervoy, получившее одобрение FDA в марте 2011 года. Экспрессия CTLA-4 на Treg-клетках служит для контроля пролиферации T-клеток.[34][35]
- Я ДЕЛАЮ: сокращение от индолеамин-2,3-диоксигеназа, это катаболический фермент триптофана с иммуно-ингибирующими свойствами. Другой важной молекулой является ТДО, триптофан-2,3-диоксигеназа. Известно, что IDO подавляет Т- и NK-клетки, генерирует и активирует Treg и миелоидные супрессорные клетки и способствует ангиогенезу опухоли.[36][35]
- КИР: сокращение от Killer-cell Immunoglobulin-like Receptor, является рецептором для MHC Класс I молекулы на Естественные клетки-киллеры. Bristol-Myers Squibb работает над Lirilumab, моноклональным антителом к KIR.
- LAG3: сокращенно от Lymphocyte Activation Gene-3, подавляет иммунный ответ путем воздействия на Treg.[37] а также прямое воздействие на CD8 + Т-клетки.[38][35] Bristol-Myers Squibb находится в фазе I с моноклональным антителом против LAG3 под названием BMS-986016.[39]
- NOX2: сокращение от никотинамидадениндинуклеотидфосфат НАДФН изоформа 2 оксидазы, является ферментом миелоидные клетки который генерирует иммунодепрессивный активные формы кислорода. Генетическое и фармакологическое ингибирование NOX2 в миелоидных клетках улучшает противоопухолевые функции соседних NK-клетки и Т-клетки а также триггеры аутоиммунитет у человека и экспериментальных животных. NOX2 является целью Ceplene который получил одобрение для использования в острый миелоидный лейкоз в пределах Европа. [40][35]
- ПД-1: сокращенно от рецептора Programmed Death 1 (PD-1), имеет два лиганда, PD-L1 и PD-L2. Этот контрольно-пропускной пункт является мишенью для препарата Кейтруда, выпускаемого Merck & Co., который получил одобрение FDA в сентябре 2014 года. Контрольно-пропускной пункт также является целью препарата Bavencio EMD Serono (Merck KGaA), который получил одобрение FDA в 2017 году. Преимущество нацеливания на PD-1 состоит в том, что он может восстанавливать иммунную функцию в микросреде опухоли.[41][35]
- ТИМ-3: сокращение от Т-клеточного домена иммуноглобулина и домена муцина 3, экспрессируется на активированных человеческих CD4 + Т-клетках и регулирует цитокины Th1 и Th17.[42] TIM-3 действует как негативный регулятор функции Th1 / Tc1, вызывая гибель клеток при взаимодействии с его лигандом, галектин-9.[43][35]
- ВИСТА: Сокращение от V-домена Ig супрессор активации Т-клеток, VISTA в первую очередь экспрессируется на гемопоэтических клетках.[44] поэтому последовательная экспрессия VISTA на лейкоцитах в опухолях может позволить блокаде VISTA быть эффективной в широком диапазоне солидных опухолей.[45][35]
- SIGLEC7 (Связывающий сиаловую кислоту лектин иммуноглобулина 7, также обозначаемый как CD328) и SIGLEC9 (Связывающий сиаловую кислоту лектин иммуноглобулина 9, также обозначаемый как CD329) представляют собой белки, обнаруженные на поверхности различных иммунных клеток, включая естественные клетки-киллеры и макрофаги (SIGLEC7 ) и нейтрофилов, макрофагов, дендритных клеток и активированных Т-клеток (SIGLEC9 ).[46] SIGLEC 7 и 9 подавляют иммунную функцию этих клеток, связываясь с терминальной сиаловой кислотой на гликанах, которые покрывают поверхность клеток.[47][48]
Ингибиторы иммунных контрольных точек
Лекарства или лекарственные препараты-кандидаты, которые ингибируют / блокируют молекулы ингибиторной контрольной точки, иногда называют ингибиторы контрольных точек; эту идею часто называют блокадой иммунных контрольных точек или просто блокадой контрольных точек.[49][35] Препараты-ингибиторы контрольных точек стали свидетелями роста фармацевтических исследований рака, проводимых такими компаниями, как Bristol-Myers Squibb, Merck, Merck KGaA, Roche и АстраЗенека.[50] Palleon Pharmaceuticals разрабатывает новую область препаратов-ингибиторов контрольных точек, которые работают над ингибированием SIGLEC 7 и SIGLEC 9 как нового класса рецепторов для терапевтических средств на основе антител.
Рекомендации
- ^ Pardoll DM (март 2012 г.). «Блокада иммунных контрольных точек в иммунотерапии рака». Обзоры природы. Рак. 12 (4): 252–64. Дои:10.1038 / nrc3239. ЧВК 4856023. PMID 22437870.
- ^ «Премия Тан 2014 года в области биофармацевтики». В архиве с оригинала на 20.10.2017. Получено 2016-06-18.
- ^ Девлин, Ханна (2018-10-01). «Джеймс П. Эллисон и Тасуку Хондзё получили Нобелевскую премию по медицине». хранитель. Получено 2018-10-01.
- ^ Хендрикс Дж; Грейвштейн Л.А.; Tesselaar K; ван Лиер РА; Шумахер Т.Н.; Борст Дж. (1 ноября 2000 г.). «CD27 необходим для генерации и длительного поддержания Т-клеточного иммунитета». Нат Иммунол. 1 (5): 433–40. Дои:10.1038/80877. PMID 11062504.
- ^ Агемацу К. (1 апреля 2000 г.). «В-клетки памяти и CD27». Гистология и гистопатология. 15 (2): 573–6. PMID 10809378.
- ^ Борст Дж., Хендрикс Дж., Сяо Й. (1 июня 2005 г.). «CD27 и CD70 в активации Т-клеток и В-клеток». Курр Опин Иммунол. 17 (3): 275–81. Дои:10.1016 / j.coi.2005.04.004. PMID 15886117.
- ^ Коке Дж. М., Миддендорп С., Ван дер Хорст Дж., Кинд Дж., Вераар Е. А., Сяо Й., Якобс Х., Борст Дж. (24 января 2013 г.). «Костимулирующий путь CD27 и CD70 ингибирует эффекторную функцию Т-хелперных 17 клеток и ослабляет связанный с ними аутоиммунитет». Иммунитет. 38 (1): 53–65. Дои:10.1016 / j.immuni.2012.09.009. PMID 23159439.
- ^ «CDX-1127 - моноклональные антитела, нацеленные на CD27». Celldex Therapeutics.
- ^ He LZ, Prostak N, Thomas LJ, Vitale L, Weidlick J, Crocker A, Pilsmaker CD, Round SM, Tutt A, Glennie MJ, Marsh H, Keler T (15 октября 2013 г.). «Агонистическое моноклональное антитело против CD27 человека индуцирует активацию Т-клеток и противоопухолевый иммунитет у мышей, трансгенных по CD27 человека». J Immunol. 191 (8): 4174–83. Дои:10.4049 / jimmunol.1300409. PMID 24026078.
- ^ Иствуд Д., Финдли Л., Пул С., Берд К., Вадхва М., Мур М., Бернс С., Торп Р., Стеббингс Р. (1 октября 2010 г.). «Неудача в испытании моноклонального антитела TGN1412, объясненная видовыми различиями в экспрессии CD28 на CD4 + эффекторных Т-клетках памяти». Br J Pharmacol. 161 (3): 512–526. Дои:10.1111 / j.1476-5381.2010.00922.x. ЧВК 2990151. PMID 20880392.
- ^ О'Салливан Б., Томас Р. (1 января 2003 г.). «CD40 и функция дендритных клеток». Крит Рев Иммунол. 23 (1): 83–107. Дои:10.1615 / critrevimmunol.v23.i12.50. PMID 12906261.
- ^ Зимм, Анджела (12 апреля 2014 г.). "Чудо-больных раком" заново изучили в поисках ключей к разгадке болезни ". Bloomberg. Получено 25 июн 2015.
- ^ Бойман О., Спрент Дж. (17 февраля 2012 г.). «Роль интерлейкина-2 в гомеостазе и активации иммунной системы». Нат Рев Иммунол. 12 (3): 180–190. Дои:10.1038 / nri3156. PMID 22343569.
- ^ «Нектар и онкологический центр Андерсона объявляют о сотрудничестве в рамках фазы 1/2 клинических исследований NKTR-214, иммуностимулирующего цитокина, связанного с CD122». Nektar Therapeutics. 2 июня 2015 г. Архивировано с оригинал 19 декабря 2017 г.. Получено 25 июн 2015.
- ^ Иммунотерапия, NKTR-214, показывает активность против солидных опухолей в клинических испытаниях
- ^ Mittler RS, Foell J, McCausland M, Strahotin S, Niu L, Bapat A, Hewes LB (1 июня 2004 г.). «Антитела к CD137 в лечении аутоиммунных заболеваний и рака». Иммунол Рес. 29 (1): 197–208. Дои:10.1385 / ir: 29: 1-3: 197. PMID 15181282.
- ^ «Компания Pieris Pharmaceuticals представит данные о новой программе биспецифической иммуноонкологии против CD137 и HER2 на Всемирной конференции здравоохранения UBS». Pieris Pharmaceuticals. 19 мая 2015. Получено 5 июн 2015.
- ^ Крофт М., Со Т., Дуан В., Соруш П. (1 мая 2009 г.). «Значение OX40 и OX40L для биологии Т-клеток и иммунных заболеваний». Иммунол Рев. 229 (1): 173–91. Дои:10.1111 / j.1600-065x.2009.00766.x. ЧВК 2729757. PMID 19426222.
- ^ Вайнберг А.Д., Моррис Н.П., Ковачович-Банковски М., Урба В.Дж., Курти Б.Д. (1 ноября 2011 г.). «Наука стала трансляционной: история агонистов OX40». Иммунол Рев. 244 (1): 218–31. Дои:10.1111 / j.1600-065x.2011.01069.x. ЧВК 3622727. PMID 22017441.
- ^ Curti BD; Ковачович-Банковски М; Моррис Н; Уокер Э; Чисхолм Л; Floyd K; Уокер Дж; Гонсалес I; Meeuwsen T; Fox BA; Moudgil T; Миллер В; Хейли Д; Коффи Т; Фишер Б; Деланти-Миллер Л; Рымарчик Н; Келли Т; Crocenzi T; Бернштейн Э; Sanborn R; Urba WJ; Вайнберг А.Д. (15 декабря 2013 г.). «OX40 является мощной иммуностимулирующей мишенью для пациентов с поздней стадией рака». Рак Res. 73 (24): 7189–98. Дои:10.1158 / 0008-5472.can-12-4174. ЧВК 3922072. PMID 24177180.
- ^ «Результат за 1 квартал 2015 года». AstraZeneca. 24 апреля 2015 г.. Получено 5 июн 2015.
- ^ Рончетти С., Золло О, Брусколи С., Агостини М., Бьянкини Р., Ночентини Дж., Айрольди Е., Риккарди С. (1 марта 2004 г.). «GITR, член суперсемейства рецепторов TNF, костимулирует субпопуляции Т-лимфоцитов мышей». Eur J Immunol. 34 (3): 613–22. Дои:10.1002 / eji.200324804. PMID 14991590.
- ^ Ночентини Г., Ронкетти С., Кузцокреа С., Риккарди С. (1 мая 2007 г.). «GITR / GITRL: больше, чем костимуляторная система эффекторных Т-клеток». Eur J Immunol. 37 (5): 1165–9. Дои:10.1002 / eji.200636933. PMID 17407102.
- ^ Шаер Д.А., Будху С., Лю С., Брайсон С., Маландро Н., Коэн А., Чжун Х, Ян Х, Хоутон А.Н., Мергуб Т., Вулчок Дж.Д. (1 ноября 2013 г.). «Активация пути GITR отменяет подавление опухолевого иммунитета из-за потери стабильности клонов регуляторных Т-клеток». Cancer Immunol Res. 1 (5): 320–31. Дои:10.1158 / 2326-6066.cir-13-0086. ЧВК 3885345. PMID 24416730.
- ^ «TG Therapeutics вступает в глобальное сотрудничество с Checkpoint Therapeutics для разработки и коммерциализации новых целевых антител для иммуноонкологии». TG Therapeutics. 4 марта 2015 г.. Получено 5 июн 2015.
- ^ Бурмейстер Й., Лишке Т., Далер А.С., Маги Х.В., Лам К.П., Койл А.Дж., Крочек Р.А., Хатлофф А. (15 января 2008 г.). «ICOS контролирует размер пула эффекторных и регуляторных Т-клеток». J Immunol. 180 (2): 774–782. Дои:10.4049 / jimmunol.180.2.774. PMID 18178815.
- ^ Леоне Р.Д., Ло Ю.С., Пауэлл Д.Д. (8 апреля 2015 г.). «Антагонисты A2aR: блокада контрольных точек нового поколения для иммунотерапии рака». Comput Struct Biotechnol J. 13: 265–72. Дои:10.1016 / j.csbj.2015.03.008. ЧВК 4415113. PMID 25941561.
- ^ Чаповал А.И., Ни Дж., Лау Дж. С., Уилкокс Р. А., Флис Д. Б., Лю Д., Донг Х., Сика Г. Л., Чжу Г., Тамада К., Чен Л. (1 марта 2001 г.). «B7-H3: костимулирующая молекула для активации Т-клеток и продукции IFN-гамма». Нат Иммунол. 2 (3): 269–74. Дои:10.1038/85339. PMID 11224528.
- ^ Лейтнер Дж., Клаузер К., Пикл В.Ф., Штёкль Дж., Майдик О, Бардет А.Ф., Крейл Д.П., Донг К., Ямазаки Т., Злабингер Г., Пфистершаммер К., Штайнбергер П. (1 июля 2009 г.). «B7-H3 - мощный ингибитор активации Т-клеток человека: нет доказательств взаимодействия B7-H3 и TREML2». Eur J Immunol. 39 (7): 1754–64. Дои:10.1002 / eji.200839028. ЧВК 2978551. PMID 19544488.
- ^ «MacroGenics представляет обновленную информацию о корпоративном прогрессе и финансовых результатах за первый квартал 2015 года». MacroGenics. 6 мая 2015. Получено 5 июн 2015.
- ^ Мао И, Ли В., Чен К., Се И, Лю Цюй, Яо М., Дуань В., Чжоу Х, Лян Р., Тао М. (20 февраля 2015 г.). «B7-H1 и B7-H3 являются независимыми предикторами плохого прогноза у пациентов с немелкоклеточным раком легкого». Oncotarget. 6 (5): 3452–61. Дои:10.18632 / oncotarget.3097. ЧВК 4413666. PMID 25609202.
- ^ Дангадж Д., Ланитис Е., Чжао А., Джоши С., Ченг Й., Сандальцопулос Р., Ра Х. Дж., Данет-Деснойерс Г., Пауэлл Д. Д. мл., Шоллер Н. (1 августа 2013 г.). «Новые рекомбинантные человеческие антитела против b7-h4 преодолевают ускользание от опухолевого иммунитета, чтобы усилить противоопухолевые реакции Т-клеток». Рак Res. 73 (15): 4820–9. Дои:10.1158 / 0008-5472.can-12-3457. ЧВК 3732560. PMID 23722540.
- ^ Дерре Л., Соперники Дж. П., Джандус С., Пастор С., Римольди Д., Ромеро П., Михиелин О., Олив Д., Шпайзер, ДЕ (1 января 2010 г.). «BTLA опосредует ингибирование опухолеспецифических CD8 + Т-клеток человека, которое может быть частично отменено вакцинацией». J Clin Invest. 120 (1): 157–67. Дои:10.1172 / jci40070. ЧВК 2799219. PMID 20038811.

- ^ Колар П., Книке К., Хегель Дж. К., Квандт Д., Бурместер Г. Р., Хофф Х., Бруннер-Вайнциерл М.С. (1 января 2009 г.). «CTLA-4 (CD152) контролирует гомеостаз и подавляющую способность регуляторных Т-клеток у мышей». Ревматоидный артрит. 60 (1): 123–32. Дои:10.1002 / арт.24181. PMID 19116935.
- ^ а б c d е ж грамм час Синь Николай Л; Teng, Michele W L; Мок, Тони С. К.; Су, Росс А. (2017). «De-novo и приобретенная устойчивость к нацеливанию на иммунные контрольные точки». Ланцет онкологии. 18 (12): e731 – e741. Дои:10.1016 / с1470-2045 (17) 30607-1. PMID 29208439.
- ^ Прендергаст Г.С., Смит К., Томас С., Мандик-Наяк Л., Лори-Клейнтоп Л., Мец Р., Мюллер А.Дж. (1 июля 2014 г.). «Индолеамин-2,3-диоксигеназные пути патогенного воспаления и иммунного спасения при раке». Рак Immunol Immunother. 63 (7): 721–35. Дои:10.1007 / s00262-014-1549-4. ЧВК 4384696. PMID 24711084.
- ^ Huang CT; Workman CJ; Летает D; Pan X; Марсон А.Л .; Чжоу Г; Hipkiss EL; Рави С; Ковальский J; Левицкий HI; Пауэлл Дж. Д.; Pardoll DM; Drake CG; Вигнали Д.А. (1 октября 2004 г.). «Роль LAG-3 в регуляторных Т-клетках». Иммунитет. 21 (4): :503–13. Дои:10.1016 / j.immuni.2004.08.010. PMID 15485628.
- ^ Гроссо Дж. Ф., Келлехер С. К., Харрис Т. Дж., Марис С. К., Хипкисс Е. Л., Де Марцо А., Андерс Р., Нетто Дж., Гетнет Д., Бруно Т. К., Голдберг М. В., Пардолл Д. М., Дрейк К. Г. (1 ноября 2007 г.). «LAG-3 регулирует накопление CD8 + Т-клеток и эффекторную функцию в мышиной системе само- и толерантности к опухоли». J Clin Invest. 117 (11): 3383–92. Дои:10.1172 / jci31184. ЧВК 2000807. PMID 17932562.
- ^ Номер клинического исследования NCT01968109 за «Исследование безопасности Anti-LAG-3 с анти-PD-1 и без него при лечении солидных опухолей» при ClinicalTrials.gov
- ^ Martner A, Aydin E, Hellstrand K (1 октября 2018 г.). «NOX2 при аутоиммунитете, росте опухоли и метастазировании». Джей Патол. 247 (2): 151–154. Дои:10.1002 / path.5175. ЧВК 6587556. PMID 30270440.
- ^ Филипс Г.К., Аткинс М. (1 января 2015 г.). «Терапевтическое применение антител против PD-1 и PD-L1». Инт Иммунол. 27 (1): 39–46. Дои:10.1093 / intimm / dxu095. PMID 25323844.
- ^ Гастингс В.Д., Андерсон Д.Е., Кассам Н., Когучи К., Гринфилд Е.А., Кент С.К., Чжэн XX, Стром Т.Б., Хафлер Д.А., Кучру В.К. (1 сентября 2009 г.). «TIM-3 экспрессируется на активированных CD4 + Т-клетках человека и регулирует цитокины Th1 и Th17». Eur J Immunol. 39 (9): 2492–501. Дои:10.1002 / eji.200939274. ЧВК 2759376. PMID 19676072.
- ^ Чжу С., Андерсон А.С., Кучро В.К. (11 августа 2010 г.). TIM-3 и его регулирующая роль в иммунных ответах. Curr Top Microbiol Immunol. Актуальные темы микробиологии и иммунологии. 350. С. 1–15. Дои:10.1007/82_2010_84. ISBN 978-3-642-19544-0. PMID 20700701.
- ^ Ван Л., Рубинштейн Р., Лайнс Дж. Л., Васюк А., Ахонен С., Го Й, Лу Л. Ф., Гондек Д., Ван И, Фава Р. А., Фисер А., Альмо С., Ноэль Р. Дж. (14 марта 2011 г.). «VISTA, новый лиганд суперсемейства Ig мыши, который негативно регулирует Т-клеточные ответы». J Exp Med. 208 (3): 577–92. Дои:10.1084 / jem.20100619. ЧВК 3058578. PMID 21383057.
- ^ Lines JL, Pantazi E, Mak J, Sempere LF, Wang L, O'Connell S, Ceeraz S, Suriawinata AA, Yan S, Ernstoff MS, Noelle R (1 апреля 2014 г.). «VISTA - это молекула иммунной контрольной точки для человеческих Т-клеток». Рак Res. 74 (7): 1924–32. Дои:10.1158 / 0008-5472.CAN-13-1504. ЧВК 3979527. PMID 24691993.
- ^ Ляубли, Хайнц; Циппелиус, Альфред; Варки, Аджит; Speiser, Daniel E .; Стеннер, Франк; Эгли, Адриан; Сайедбаша, Мохаммедьясин; Амос, Кристофер I .; Хан, Ёнхун (2018-11-01). «Самоассоциированные молекулярные паттерны опосредуют уклонение от противоракового иммунитета, задействуя Siglec на Т-клетках». Журнал клинических исследований. 128 (11): 4912–4923. Дои:10.1172 / JCI120612. ISSN 0021-9738. ЧВК 6205408. PMID 30130255.
- ^ Варки, Аджит; Полсон, Джеймс С .; Крокер, Пол Р. (2007). «Сиглеки и их роль в иммунной системе». Nature Reviews Иммунология. 7 (4): 255–266. Дои:10.1038 / nri2056. ISSN 1474-1741. PMID 17380156.
- ^ Полсон, Джеймс С .; Crocker, Paul R .; Маколи, Мэтью С. (2014). «Сиглек-опосредованная регуляция функции иммунных клеток при заболевании». Nature Reviews Иммунология. 14 (10): 653–666. Дои:10.1038 / nri3737. ISSN 1474-1741. ЧВК 4191907. PMID 25234143.
- ^ Пардолл, Дрю М. (22 марта 2012 г.). «Блокада иммунных контрольных точек в иммунотерапии рака». Обзоры природы Рак. 12 (4): 252–264. Дои:10.1038 / nrc3239. ЧВК 4856023. PMID 22437870.
- ^ «Лекарства от рака становятся лучше и дороже». Экономист. 2017-05-04. Получено 2017-05-19.
